1. 서 론
2. 실험 방법
2.1 사용된 시료 및 노화 기법
2.2 표면 분석 실험
2.3 열분석 실험 셋업 및 반응인자 추출
2.4 ZPP의 Lifespan 계산
3. 실험 결과
3.1 ZPP 표면 분석 결과
3.2 DSC를 통한 열분석 결과
3.3 노화 조건에 따른 ZPP의 반응 키네틱스 분석
3.4 피크 분리 수행 결과
3.5 추출한 reaction kinetics를 활용한 ZPP의 반응 모사 결과
3.6 ZPP의 예상수명 계산
4. 결 론
1. 서 론
고에너지 물질이 시간이 지남에 따라 노화로 인하여 화합물 내부적으로 산화, 가수분해와 같은 화학반응 및 구조적 결함과 같은 현상들이 발생하게 되고, 이에 따라 목표 성능이 심각하게 감소할 수 있다. 노화는 일반적으로 느린 속도로 진행되는 화학반응의 한 종류로서 노화로 인한 명확한 변화를 파악하려면 짧게는 몇 개월에서 길게는 몇십 년의 기간이 소요될 수 있다. 고에너지 물질에 관한 노화 연구는 현재까지 활발히 진행되고 있는데, 이 중에는 20년 이상 장기간 자연 노화된 시료들에 집중하여 로켓추진제를 포함한 각종 고에너지 물질에 대한 노화 효과를 명확히 밝혀낸 바 있다[1], [2], [3]. 그러나 노화 시료를 마련하기 위해서는 상당한 시간이 소요되기 때문에, 이를 해결하기 위해 높은 온도 조건에서 시료를 보관하여 노화 진행을 보다 가속하는 ‘열 노화’ 혹은 ‘가속 노화’를 통해 고에너지 물질에 대한 노화 효과를 파악하고[4], [5], [6], [7], [8], [9], [10], [11], [12], [13], 노화된 시료의 수명을 예측하는 연구가 진행된 바 있다[9], [14].
그런데 해당 연구들은 실제 환경 조건에 중요한 역할을 하는 습도의 개념을 자세하게 고려하지 않았다는 한계가 존재한다. 비록 조립 공정에서 파이로테크닉, 추진제와 같은 고에너지 물질들이 치밀한 밀봉과정을 통해 충전된다고 하더라도, 해당 물질들이 밀봉되기 전에 외부 환경에 노출될 가능성은 충분히 존재한다[15]. 뿐만 아니라, 밀봉된 완제품이 오랫동안 보관되다 보면 내부적으로 자체적인 결함이 발생하거나 수분이 중간에 유입되어 작동하지 않는 경우가 나타날 수도 있으므로, 고에너지 물질에 대한 노화 분석과 정확한 노화 효과 파악에 있어서 상대습도의 개념이 필수적으로 고려되어야만 한다.
파이로테크닉 개시제의 성능에 있어 노화의 영향을 이해하기 위해서, 본 연구에서는 NASA 표준 개시제로 널리 활용되며 높은 열적 안정성과 긴 수명을 보유하고 있는 Zirconium Potassium Perchlorate(ZPP) 에 대하여 노화 연구를 수행하였다. ZPP는 지르코늄(Zirconium, Zr)을 연료로, 과염소산칼륨(Potassium perchlorate, KClO4)을 산화제로 하며 해당 두 물질을 바인더인 Viton-b로 결합한 화합물이라고 할 수 있다[15], [16], [17]. ZPP와 같은 고에너지 물질들은 연료와 산화제의 산화-환원 과정을 통해 나타나는 발열반응을 이용하여 급격한 압력이나 빛, 소리를 방출하고, 이를 통해 목표성능을 달성하게 된다. 그런데 노화는 ZPP의 화학적 조성 변화를 유발하여 연료의 산화를 통해 이루어지는 발열반응 특성에 변화를 일으키기 때문에, 이에 따른 열역학적 특성 변화와 성능 감소가 우려되고 있다.
실제로 이러한 파이로테크닉 물질의 노화에 있어서 상대습도를 고려함으로써 현실적인 환경 조건을 반영하려고 노력한 연구들이 진행된 바 있다[6], [7], [11], [18]. Lee et al. [22]의 연구에서도 마찬가지로 ZPP의 노화에 관하여 100% 상대습도 조건을 고려하여, ZPP의 노화 메커니즘이 연료인 지르코늄의 산화를 기본으로 이루어진다는 것을 밝혀내었다. 하지만, 상대습도 100%라는 극한의 환경 조건에 대해서만 연구가 진행되었다는 점과 ZPP의 반응역학에 대한 분석이 이루어지지 않았다는 한계가 있다.
본 연구에서는 이전 연구에서는 밝혀지지 않았던 사항들을 새롭게 밝혀내어, ZPP 개시제에 대하여 더욱 자세하고 명확한 노화의 영향과 성능 변화를 파악하였다. 먼저, 상대습도를 0%, 30%, 70%, 100%로 다양하게 설정하여 습도 레벨에 따른 노화 효과를 확인해볼 수 있었다. 뿐만 아니라, 널리 쓰이는 표면분석기법 중 하나인 X-ray photoelectron spectroscopy(XPS) 기법을 활용하여 습도 환경 및 노화 기간에 따른 산화제와 연료의 화학적 조성 차이 또한 확인해볼 수 있었다[29].
그리고 각 습도가 다른 네 가지 유형의 노화 시료에 대하여 대표적인 열량실험인 differential scanning calorimetry (DSC) 를 활용하여 열분석을 수행하였으며 이를 통해 얻은 실험 데이터를 기반으로 Friedman isoconversional method를 적용하여 ZPP의 전반적인 발열반응에 대한 운동 파라미터의 변화를 확인해볼 수 있었다. 나아가 습도에 따른 반응 정도의 차이를 확연하게 확인하기 위하여 앞서 얻은 운동파라미터들을 하우스 코드에 대입하여 0-D 전산모사를 수행하였다. 뿐만 아니라 실험을 통해 추출한 운동 파라미터와 van’t Hoff equation을 활용하여 ZPP의 상대적인 수명 또한 예측해보았으며, 이를 실험적으로 얻은 대표적인 성능이라고 할 수 있는 발열량 추세와 결합하여 성능과 수명 관계를 확립하였다. 이렇게 다양한 실험 기법과 시뮬레이션을 통하여 다습한 조건이 ZPP의 열역학적 특성 변화를 불러일으킬 수 있으며, 높은 상대 습도 조건으로 갈수록 ZPP의 지르코늄의 산화로 인하여 급격한 수명 감소를 초래한다는 사실을 확인해볼 수 있었다.
2. 실험 방법
2.1 사용된 시료 및 노화 기법
2.1.1 시료 종류
본 연구에서는 분말 ZPP를 열분석 실험에 사용하였다. 이때, 입자의 크기에 따라 ZPP와 같은 고에너지 물질의 발열 특성에 차이가 발생할 수 있으므로, 이를 사전에 방지하기 위해서 열분석 수행에 앞서 200 mesh sieve에 ZPP 분말을 걸러줌으로써 입자 크기가 약 75 µm 이하로 구성되도록 하였다. 그리고 ZPP의 각 구성성분과 비율, 제조사 및 판매사 정보는 Table 1에 제시되어있다.
Table 1.
Specific information of ZPP chemical formula
2.1.2 가속노화 방법
ZPP 물질은 온도를 71°C로 고정한 건조 오븐 내에 저장되어 온도의 영향을 파악하고자 하였다. 그리고 각 습도 조건은 각 시료를 4.7 L의 밀폐 용기 내에 보관하여 제어를 가능하게 하였다. 71°C 조건에서 수증기압과 이상기체법칙을 적용하여 주어진 공간에 대한 상대습도에 해당하는 정제수의 양을 밀폐 용기 내에 투입하여 조절할 수 있었다.
2.1.3 상세 노화 조건
본 연구에서는 온도 및 상대습도와 같은 환경 변인을 달리해가며 노화시킨 ZPP시료를 사용하였다. Table 2에 나타난 바와 같이 본 연구에서 설정한 노화 조건은 71°C의 온도와 0% RH 레벨을 유지한 가속 노화 조건과 온도는 71°C로 유지한 채로 3개의 다른 상대습도 조건(30% RH, 70% RH, 100% RH)을 적용한 수분 노화 조건으로 구성이 되어있다. 이때, 71°C의 온도 조건은 aerospace industry guideline[30]을 따른 것으로 해당 규정을 노화 조건에 반영함으로써 더욱 정확한 노화 분석을 수행하고자 하였다. 그리고 국내 평균 습도가 연중 60~75% 범위에 해당하며, 상대적으로 습한 7월과 8월은 70~85% 정도, 건조한 3월과 4월은 50~70%의 습도를 보인다고 보고된다. 본 연구에서는 국내 평균 습도 값인 70% RH뿐만 아니라 더 낮은 습도 범위인 0%, 30%와 더불어 매우 습한 조건인 100% RH까지 고려함으로써, 수분함량이 ZPP시료의 화학적 조성 및 열적 성능에 끼치는 영향을 보다 폭넓게 파악하고자 하였다.
Table 2.
Aging conditions of the utilized ZPP samples
본 연구에서 ZPP는 노화 조건에 따라 비 노화 시료인 ‘Unaged’, 열적 노화된 ‘Thermal aging’, 마지막으로 수분 노화된 시료를 의미하는 ‘Hygrothermal aging’ 총 3가지 그룹으로 분류된다. 이때, 수분 노화된 시료는 상대습도가 30%, 70%, 100%로 더욱 세분화하였다. 본 연구에서는 앞으로 편의를 위해 각 시료를 Table 2의 맨 왼쪽란에 표기되어있는 이름으로 언급하였다. 다시 말하자면, 노화되지 않은 ZPP는 ‘0’으로 가속 노화된 ZPP는 ‘T_#n’, 30% RH 조건에서 수분 노화된 ZPP는 ‘H30_#n’, 70% RH 조건에서 수분 노화된 ZPP는 ‘H70_#n’, 마지막으로 100% RH 조건에서 수분 노화된 ZPP는 ‘H100_#n’으로 표기하였다. 이때, 라벨에서 마지막에 표기되는 숫자는 노화 기간을 의미한다.
그리고 Table 2에 나타나 있듯이 가속 노화된 시료와 수분 노화된 ZPP 시료의 노화 기간이 정확하게 일치하지 않는 모습을 볼 수 있다. 가속 노화 그룹의 시료(T_4M~12M)들이 상대적으로 수분 노화된 시료들(H30_2W~16W, H70_2W~16W, H100_2W~12W)보다 더 오랫동안 노화되었으며, 수분 노화된 시료 중에서도 100% 상대습도 조건에서 노화된 시료(H100_2W~12W)들은 수분 노화된 다른 시료들과 비교해보았을 때 상이한 노화 기간을 가진다. 이렇게 각 노화 그룹마다 약간의 노화 기간의 차이로 인하여, ZPP 시료의 노화 분석에 있어 정확한 정량적 분석을 수행하기에 어려울 수 있을 것이다. 하지만 습도 레벨 차이에 따른 상대적인 비교와 각 노화 군에서 노화 기간이 증가함에 따라 나타난 화학적, 열적 성능변화들을 통합하여 더욱 상세한 결과 기술하였으며, 이를 통해 수분 함량이 ZPP에 끼치는 치명적인 영향을 파악해낼 수 있었다.
2.2 표면 분석 실험
다양한 환경 조건에 노화된 ZPP 혼합물들의 화학적 결합 상태와 더불어 자세한 정성 및 정량 분석을 위해 대표적인 표면 분석 기법이라고 할 수 있는 XPS 기법을 통해 각 노화 조건에 해당하는 ZPP 시료에 대한 표면분석을 수행하였다. 상세한 XPS spectra는 초고진공 상태로(UHV) AXIS-SUPRA 광전자 분광계(Kratos, UK)를 사용하여 측정되었다. 이때, 해당 장비에는 마이크로 초점 단색 Al Kα X선 소스(1486.6 eV)와 반구형 분석기(WX-600)가 장착되었다. 샘플 분석 및 load lock chamber의 기본 압력은 각각 5 × 10−10 및 5 × 10−8Torr 미만으로 설정되었다.
2.3 열분석 실험 셋업 및 반응인자 추출
2.3.1 DSC 열량 분석
DSC 열량 분석을 통하여 노화된 ZPP 개시제에 대한 열역학적 특성을 파악하였고, 각 시료가 나타내는 열적 반응 프로세스에 대한 분석을 진행하였다. 실험의 정확도와 kinetics 분석의 높은 신뢰성을 보장하기 위하여 본 연구는 International Confederation for Thermal Analysis and Calorimetry(ICTAC) Kinetic Committee’s recommendations [31]를 따라 실험을 진행하였다.
DSC 실험의 경우 Mettler Toledo 사의 DSC-3+ 기종을 사용하였다. 열량 분석의 method 설정에 있어서 승온 속도는 1, 2, 3, 4°C/min의 총 네 가지 승온 속도를 사용하였는데, 이처럼 느린 속도의 승온 속도를 채택한 이유는 낮은 승온 속도에서 각 하위 발열 반응들을 명확하게 관찰할 수 있기 때문이다. 다시 말해 ZPP의 발열반응을 구성하는 다양한 열역학적 반응프로세스들을 고려하기 위함이다[15]. 그리고 반응 온도는 30°C~600°C로 설정하였으며, 85 mL/min의 Nitrogen purge flow 환경을 통하여 외부 공기 및 불순물이 유입을 차단하고, 오직 ZPP 물질만을 통해 연소 반응이 일어날 수 있도록 하였다.
그리고 샘플 질량 같은 경우, 설정한 양에 따라 DSC 결과에 크고 작은 영향들을 미칠 수 있다[31]. 예를 들어, 만약 샘플 질량을 과다하게 설정하거나 혹은 승온 속도를 너무 빠르게 설정하였을 때 발열반응이 수행되는 도중에 자기 가열 효과(self-heating effect)가 발생하여 부정확한 결과가 초래될 수 있다[32], [33]. 반면, 샘플 질량이 너무 적은 상황일 때에는 DSC의 열 유량 신호가 노이즈 신호와 혼재되어 제대로 구분이 어려워지는 문제가 발생하기도 한다. 따라서 이러한 문제들을 사전에 방지하기 위해서 사전 실험을 수행하여 본 연구에서 설정한 승온 속도에 최적화된 샘플 질량들을 결정할 수 있었다. 결과적으로 2~3 mg의 ZPP 시료가 본 연구에서 설정한 승온 속도 조건에서 자기 가열 효과 없이 적절한 DSC 결과를 얻어낼 수 있음을 확인하였다.
실험을 통해 얻은 DSC 열분석도 결과들에서 대부분의 ZPP 시료들이 일정한 반복성을 보여주었지만 그럼에도 불구하고 시료 측정 시에 포함되는 오차나 DSC 열 측정 센서의 정확도, 시료의 uniformity 등과 같은 다양한 원인으로 인하여 간혹 부정확한 결과들이 도출되기도 하였다. 따라서 본 연구에서는 노이즈나 불명확한 신호를 최대한 제거하기 위하여 약 2~3 mg의 ZPP 파우더 시료를 40 µL standard aluminium crucible pan의 바닥에 평평하게 고루 분포하도록 하여 한쪽으로 열이 치우치는 열 응집 현상이 발생하지 않도록 하였다. 그리고 최소 3회 이상의 반복실험을 수행하여 수행된 실험마다 오차를 줄이고 반복성을 입증하기 위해 노력하였다.
2.3.2 화학반응 인자 분석
반응 kinetics 분석에 있어 중요한 역할을 수행하는 대표적인 세 가지 종류의 파라미터로 활성화 에너지(Eα), 빈도 인자(Aα), 반응 모델(f(α)이 있으며, 이 파라미터들을 통틀어 ‘Kinetic triplet’이라고 일컫는다[34]. 본 연구에서는 해당 파라미터 중에서 활성화 에너지를 추출하였고, 이 과정에서 AKTS software[35]를 사용하여 계산을 진행하였다. 이때, 활성화 에너지는 반응 정도를 나타내는 파라미터인 반응률 ‘α’에 따른 파라미터의 추이를 확인할 수 있는 등전환법을 적용하여 얻을 수 있었는데, 일반적으로 널리 쓰이는 미분 기반의 등전환법인 ‘Friedman isoconversional method[36]’와 적분 기반의 등전환법인 ‘Ozawa isoconversional method [37]’ 총 2가지 기법을 적용하여 각 노화된 ZPP에 대한 값을 서로 비교해보았다. 두 방법 모두 reaction progress를 나타내는 α가 반응전인 ‘α = 0’에서부터 ‘α = 1’에 도달할 때까지 순간적인 활성화 에너지를 결정하지만 식 (1)과 식 (2)와 같이 계산적인 접근 방법에 차이가 있다.
이때, 아래 첨자 i는 승온 속도 조건(βi = 1, 2, 3, 4°C/min)을 의미하며 α는 반응의 전환 정도를 나타내는 파라미터이다[35]. 그리고 f(α), Aα, Eα, Tα, R은 각각 반응 모델, 반응 정도에 따른 활성화 에너지(kJ/mol)와 빈도 인자(1/s), 온도(K), 기체상수를 의미한다[35]. 본 연구에서는 비등온 조건으로 DSC 실험을 수행하였기 때문에, kinetic parameter를 구하는 계산 또한 비등온 조건을 적용하여 파라미터들을 계산하였다. 그런데 반응 초반과 후반에서 해당하는 파라미터 값의 경우, 반응의 불안정성이 상당히 크고 오차도 크기 때문에 0.1 < α < 0.9에 대한 파라미터 값에 대해서만 고려하였다.
2.3.3 피크 분리 기법
본 연구에서 DSC 실험으로 구한 열 분석도를 기반으로 AKTS software[34] 사에서 제공하는 Fraser-Suzuki 함수 기반의 peak deconvolution을 사용하여 중첩된 반응 피크를 분리하였다[38], [39]. 피크 분리기법은 열량 분석실험 데이터 중에서 3°C/min의 승온 속도 조건에서 수행된 ZPP 샘플에 적용되었다.
2.4 ZPP의 Lifespan 계산
노화된 ZPP 시료의 수명은 식 (3)과 같이 가속 노화된 고체 추진제의 usage time을 구할 때 일반적으로 사용되는 van’t Hoff 방정식을 통해 계산되었다. 해당 방정식은 화학 성분의 변화를 일으키는 노화에 특히 적합하다고 알려진 식으로 본 연구에서 ZPP의 수명 계산을 수행하는 데 있어 적합할 것으로 판단하였다.
위 식에서 tE는 예측된 시료의 기대 수명(단위: 년)을 의미하고 TE는 시료의 보관 온도(°C), tT는 시료의 노화 기간(단위: 일), TT는 시료의 노화 온도(°C), AF는 Acceleration Factor의 준말로 매 ΔTF에 따른 반응속도의 변화를 의미한다. 이때, 본 연구에서는 TE와 ΔTF는 각각 25°C와 10°C로 설정하였다. 이때, ZPP의 lifespan은 실험을 통해 얻은 발열량과 계산을 통해 구한 기대수명과의 관계를 통해 결정이 된다. 그리고 식 (4)에서 나타나 있듯이 AF는 Arrhenius equation을 기반으로 계산되는 상수이며, 이 계수에 가장 적합한 범위는 일반적으로 2~4[9], [40]라고 알려져 있다. 본 연구에서는 ZPP의 수명을 보다 정확하게 산출하기 위해서 각 노화된 ZPP 실험 데이터를 해당 식에 적용할 때, 계산된 AF 값이 해당 범위 내에 포함되는 값만을 채택하였다.
3. 실험 결과
3.1 ZPP 표면 분석 결과
3.1.1 XPS 기법을 통한 정성분석 결과
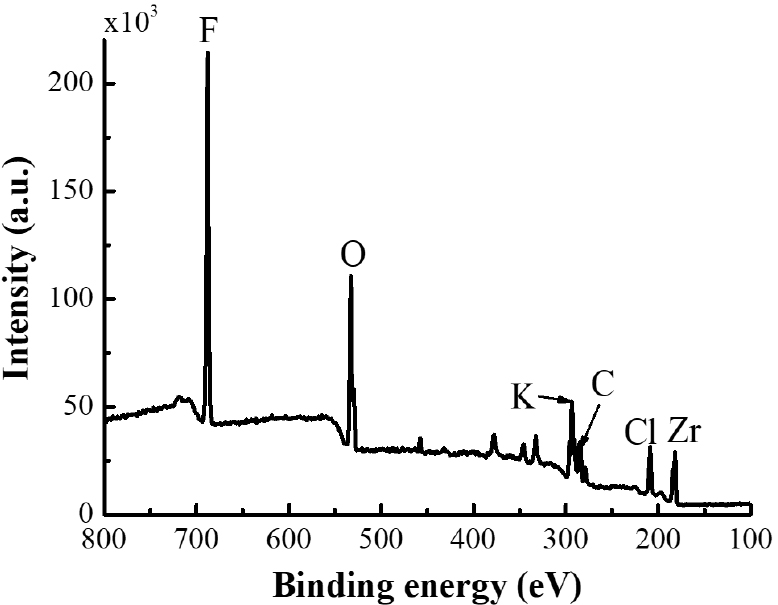
XPS 기법을 통해 우선 노화되지 않은 ZPP 시료(Baseline)에 대하여 정성분석을 수행해본 결과 Fig. 1과 같은 결과를 얻을 수 있었다. ZPP는 Zr, KClO4, Viton-b([-C7H2F12-]n)로 이루어져 있는데, 우선 표면에 코팅되어있는 Viton-b의 성분인 F 성분이 가장 높은 세기로 검출되었다. 뿐만 아니라, ZPP의 구성성분인 Zr, K, Cl, O, F 또한 모두 확인이 가능하였다.
3.1.2 XPS 기법을 통한 정량분석 결과
노화 기간과 상대습도 조건에 따른 ZPP표면의 화학적 성분 변화를 파악하기 위해 XPS 정량분석이 수행되었으며, 해당 시료들은 Table 2 우측의 ‘XPS 수행 여부’란에 ‘O’로 표시되어있다.
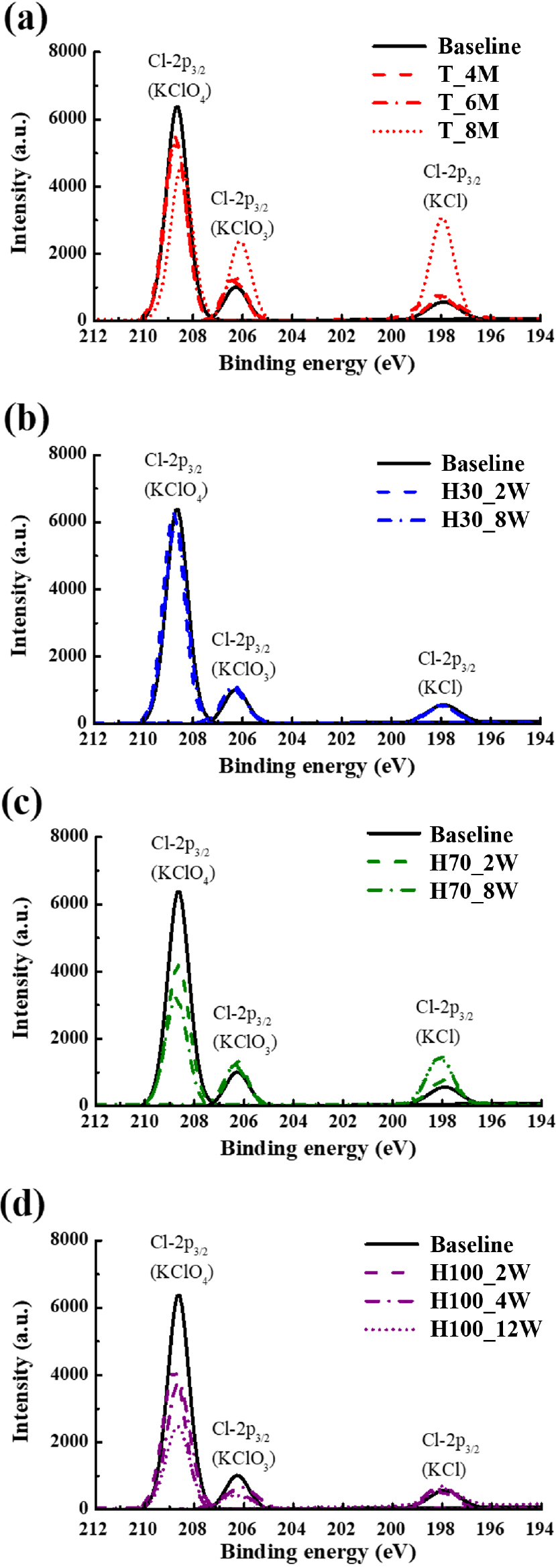
산화제인 KClO4의 정량분석 결과는 Fig. 2에 나타나 있으며 연료인 Zr의 정량분석 결과는 Fig. 3에 제시되어있다. 이때, 산화제에 대한 정량분석을 수행하는 데 있어 ‘Cl’ 신호에 관한 결과만 제시하였는데, 그 이유로는 ‘K’ 신호에서는 노화된 ZPP시료에 대하여 오직 KClO4 신호의 감소만 나타날 뿐 다른 분해 생성물에 대한 추가적인 신호는 드러나지 않았기 때문이다. 하지만 ‘Cl’ 신호에서는 KClO4의 분해반응뿐만 아니라 분해반응을 통해 생성된 물질들도 확인할 수 있었기 때문에, ‘Cl’ 신호가 산화제의 정량분석에 있어 적합할 것으로 판단되어 채택하였다. 그리고 본 연구에서는 99% 순도의 KClO4가 포함된 비노화 ZPP시료를 사용하였지만, Fig. 2(a)에서 볼 수 있듯이 KClO4 신호(208.70eV) 뿐만 아니라 소량의 KClO3 (206.50eV)와 KCl 신호(198.00eV)가 검출되었다. 따라서 비노화 시료일지라도 미량의 분해된 산화물이 존재할 수 있음을 알 수 있다. 따라서 노화 분석을 진행하는 데 있어서 KClO4뿐만 아니라 해당 산화 생성물의 비율 또한 상대적인 비교가 가능하도록 하였다.
우선, Fig. 2(a-d)에서는 산화제 성분에 대한 표면분석 결과를 보여주고 있는데, 각 노화 조건마다 다른 결과를 가짐을 확인해볼 수 있었다. 가속노화된 ZPP 시료의 경우 Fig. 2(a)와 같이 1년 이상 노화된 경우 상당량의 KClO4가 KClO3와 KCl로 분해되는 현상을 확인해볼 수 있었다. 이를 통해 높은 온도 조건이 ZPP 내의 KClO4 분해반응을 보다 촉진하는 역할을 함을 알 수 있다. 반면, 수분 노화된 ZPP의 경우를 보면 30% RH의 낮은 상대습도 조건(Fig. 2(b))에서는 산화제 성분이 비교적 유지되는 경향성을 보였지만, 상대습도 레벨이 높아질수록(70% RH, 100% RH) KClO4 분해 현상이 가속되는 현상을 볼 수 있다. 그런데 가속노화 시료와는 달리 산화 분해물인 KClO3와 KCl 함량이 증가하지 않았으며, 100% RH의 경우(Fig. 2(d)) 노화 기간이 증가함에 따라 KClO4뿐만 아니라 KClO3 함량도 감소하는 경향성을 확인해볼 수 있었다.
이는 수분 노화의 경우 산화제인 KClO4의 분해가 KClO3 혹은 KCl의 생성으로 이어지지 않으며 다른 새로운 분해 생성물로 합성이 되는 것을 추정해볼 수 있다. 이때, XPS의 경우 수소 원자 H가 포함된 신호는 계측이 불가한데, 이를 토대로 습도가 높은 환경에서는 KClO4가 H2O에서 분해된 수소와 반응하여 수산화물 형태의 새로운 분해 생성물을 만들어내는 것을 추측해볼 수 있다.
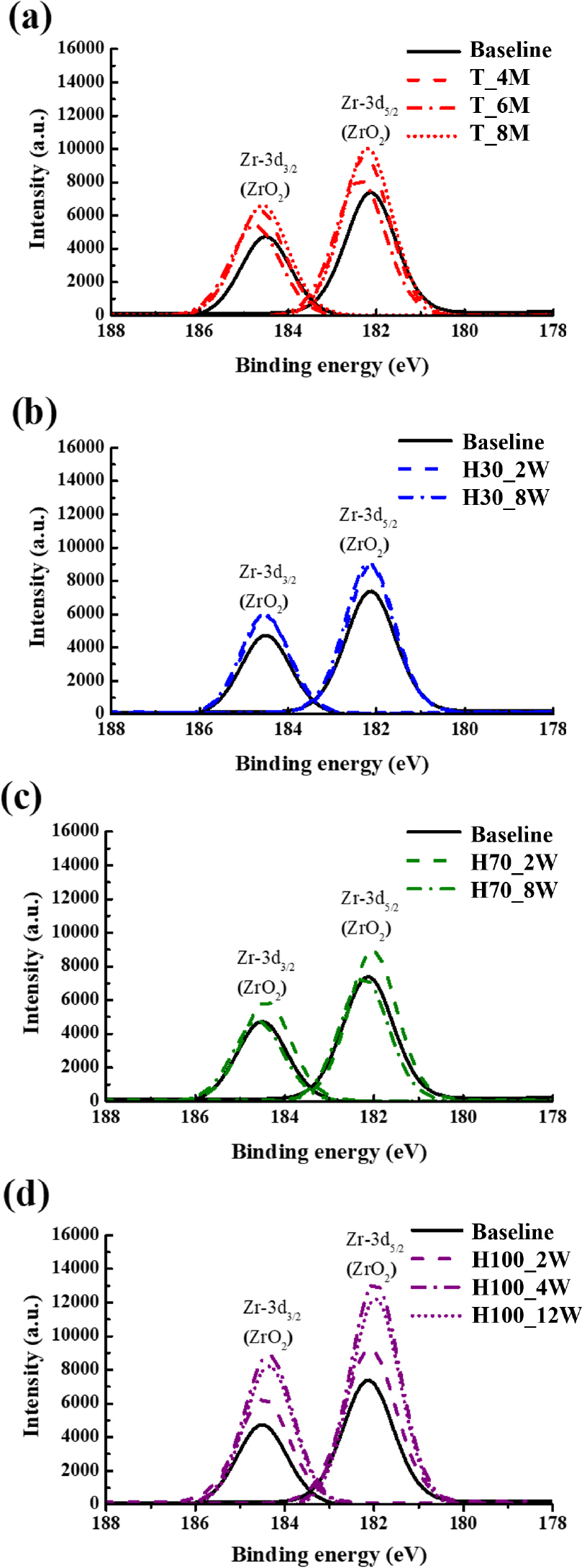
연료인 Zr의 표면분석 결과는 Fig. 3에서 확인해볼 수 있는데, 산화제의 경우와 마찬가지로 Fig. 3(a)은 가속노화된 경우, Fig. 3(b-d)은 각각 상대습도가 30%, 70%, 100%인 환경에서 노화된 시료에 관한 결과를 나타낸다. 순수한 Zr의 경우 반응성이 높고 민감한 물질로 알려져, 상온에 노출될 경우 Zr 입자 표면에 ZrO2 막이 자연스럽게 형성된다고 알려져 있다[41]. 이때 노화가 진행될수록 ZPP내의 Zr는 공기 중의 산소 또는 내부의 KClO4와 반응하여 표면의 산화막을 더욱더 두껍게 형성하게 될 것이다. 그래프에 도시된 ZrO2 신호(182.20eV, 184.50eV)는 상대습도 레벨과 노화 기간이 증가함에 따라 급격하게 증가하는 경향을 보였다. 특히, 상대습도가 100%인 조건에서 ZrO2 함량이 모든 노화군을 통틀어서 가장 높았으며, 이는 이전에 수행되었던 ZPP 노화 연구 결과[20], [25]와도 일치하는 경향성을 보여준다.
이렇게 산화제와 연료에 대하여 수행한 XPS 결과를 토대로 70% 이상의 높은 상대습도 조건과 긴 노화 기간이 ZPP 내부의 화학적 조성 변화에 상당한 영향을 줄 수 있다는 중요한 결과를 얻을 수 있었다. 특히, 가속노화된 경우 산화제인 KClO4가 KClO3와 KCl로 분해되는 경향성이 뚜렷하였으며, 수분 노화된 경우 산화지르코늄 생성에 더 큰 영향을 미치는 것을 확인해볼 수 있었다.
3.2 DSC를 통한 열분석 결과
3.2.1 DSC 열분석도
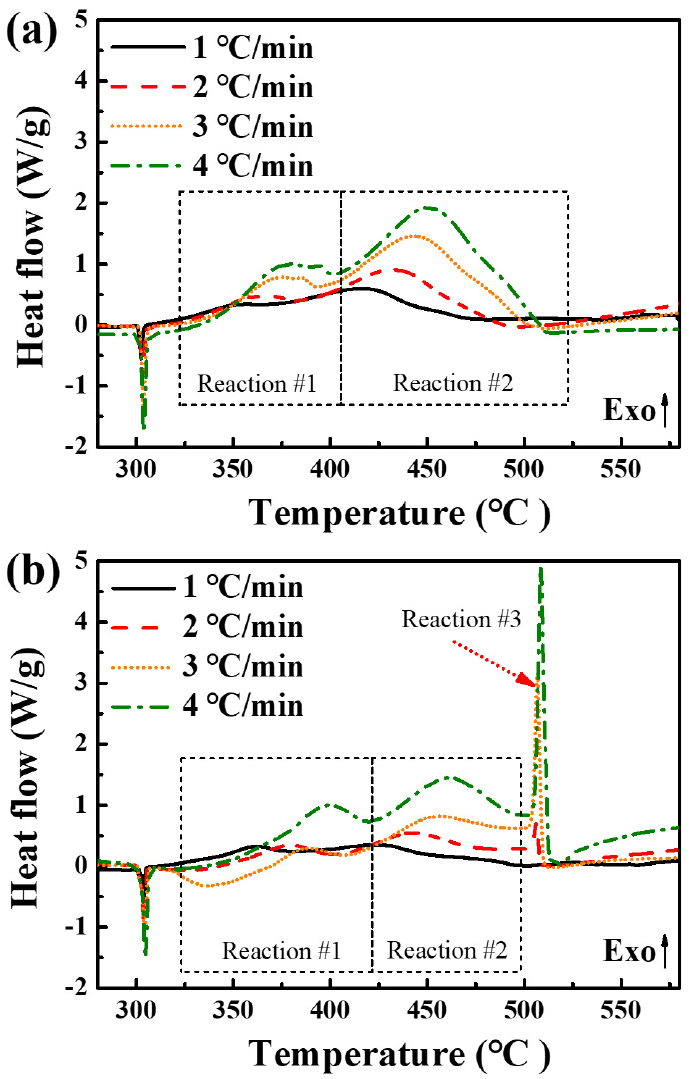
DSC 열량 분석 결과 노화되지 않은 ZPP와 장기간 수분 노화된 ZPP 사이에서 명확한 발열반응의 차이를 볼 수 있었다. Fig. 4(a)와 같이 노화되지 않은 일반 ZPP 시료(Baseline)에 대한 열분석도를 확인해보면, 300°C 부근에서 산화제인 KClO4의 α-β 상변화 과정[8]을 나타내는 흡열반응 이후 두 가지 이상의 발열반응이 넓은 온도영역에서 겹쳐져 나타난 것을 볼 수 있다.
겹쳐진 발열반응은 다시 첫 번째(Reaction #1)와 두 번째(Reaction #2) 발열 현상으로 분류해볼 수 있는데, 약 320~400°C 부근에서 나타나는 첫 번째 발열반응은 Viton-b의 분해반응과 더불어 이를 통해 발생한 산화제와 연료 초기 연소반응이라고 할 수 있다[42]. Sanborn et al. [4]의 연구에 의하면 Viton-b는 약 400°C 근처에서 완전히 분해되며, 이러한 바인더의 분해반응이 산화제와 연료간의 발열 현상의 개시제로서 임무를 수행할 수 있음을 밝혔다. 그 후에 이어지는 두 번째 발열반응은 Viton-b를 제외한 Zr, KClO4 간의 주 연소반응이라고 할 수 있다[42].
반면에 100% RH 조건에서 16주간 수분 노화된 ZPP 시료인 H100_12W의 결과(Fig. 4(b))를 보면, Baseline의 결과와 비교해보았을 때 500°C 부근에서 새로운 발열피크가 등장한 것을 볼 수 있다. 해당 반응은 연료인 Zr와 반응하지 못하고 남아있던 KClO4의 분해반응[8]을 나타내는데, 이는 연소 반응이 진행되기 전 이미 H100_12W 시료 내부에 상당량의 산화된 연료인 ZrO2 성분이 존재함을 보여주는 결과라고 할 수 있다. 이는 앞서 확인해보았던 표면분석 결과와도 일치하며, 높은 상대습도 조건이 연료인 Zr의 산화에 결정적인 영향을 할 수 있음을 의미하는 결과이기도 하다.
각각의 노화된 시료 간에 열분석 결과를 비교해보았을 때, 100% RH 환경에서 노화된 시료들 모두 잔여 KClO4 분해 현상이 발생하였다. 그리고 70% RH 환경에서 16주간 노화된 ZPP 시료 또한 해당 반응을 나타내는 것을 확인해볼 수 있었다. 따라서 높은 습도 환경이 연료인 Zr 산화 촉진을 유발할 수 있으며, 100% RH 환경이 아니더라도 수분 환경에 장기간 노출될 시에 다습한 환경에서 보관된 것과 같은 결과가 초래될 수 있음을 알 수 있다.
3.2.2 노화로 인한 발열량 변화
본 연구에서 ZPP에서 나타난 발열반응에 대한 발열량 계산은 DSC 신호(D(t)) 에서 반응이 개시되는 시점(ti)에서부터 반응이 종결되는 시점(te)까지 sigmoid tangential 타입의 baseline(B(t))을 설정해준 뒤, 해당 시간 동안의 DSC signal과 baseline 사이의 구간을 적분하여 발열량(∆H)을 계산하였으며 식 (5)와 같이 나타낼 수 있다[5], [34].
해당 과정을 통해 얻은 발열량 값은 각 시료 당 네 종류의 승온 속도에서 실험된 데이터에 대한 평균값이며, 편차와 함께 Table 3에 나타내었다.
Table 3.
Heat of reactions for all types of ZPP samples
Baseline의 경우 발열량은 평균 2721J/g이었으며 승온 속도에 따라 213J/g의 편차를 보였다. 가속노화된 ZPP (T_4M~12M)의 경우 노화 기간이 늘어남에 따라 발열량도 감소하는 경향을 보였는데, 노화 기간이 8달이 넘어가자 약 80%로 유지되던 발열량이 10% 더 감소한 70%로 감소하였다. 1년 동안 가속노화된 시료(T_12M)의 경우, 초기보다 35%가량 감소한 65%의 발열량만을 보유하고 있었다.
30% 상대습도 조건에서 16주 동안 노화된 ZPP 시료(H30_16W)의 경우 Baseline의 발열량의 약 80%인 약 2152J/g의 발열량을 가졌다. 30% RH 조건에서 노화된 시료와 가속노화된 ZPP와 비교해보았을 때, 발열량의 감소 추이는 비슷하였으나 수분 노화된 시료의 경우 승온 속도에 따른 발열량 편차가 큰 경향을 보였다. 그리고 70% RH, 100% RH 조건에서 수분 노화된 시료의 경우 각각 16주 차(H70_16W)와 6주 차(H100_6W)부터 발열량이 급격하게 감소하기 시작하였다. 상대습도가 높아짐에 따라 발열량이 급격하게 감소하는 시점이 앞당겨졌는데, 이는 수분 함량이 높은 환경이 ZPP 내의 연료 산화를 더욱 촉진해 열 성능 저하를 초래한다고 해석해볼 수 있다.
3.3 노화 조건에 따른 ZPP의 반응 키네틱스 분석
3.3.1 비노화 ZPP에 대한 화학반응 인자
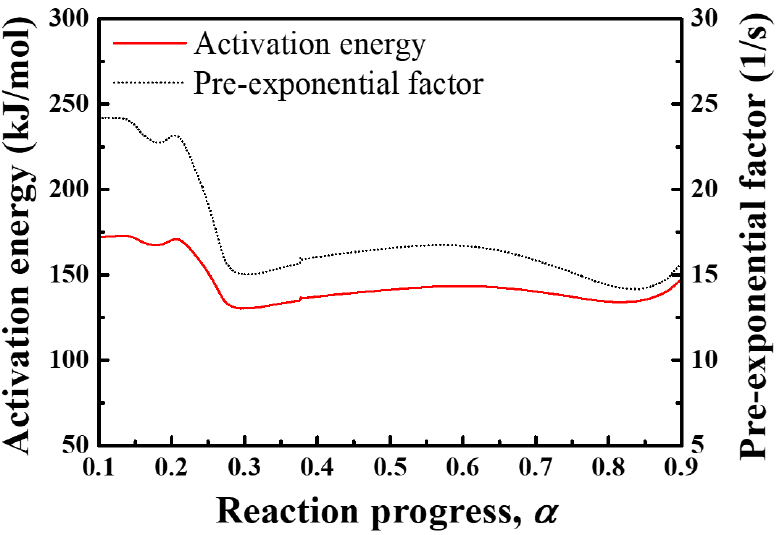
서로 다른 네 개의 승온 속도 조건의 DSC 실험 데이터를 Friedman isoconversional method[36]에 적용하여 반응률 α에 따른 활성화 에너지와 빈도 인자를 추출할 수 있었으며, 결과는 Fig. 5와 같다.
첫 번째 발열반응 구간인 반응 초반(0.1 < α < 0.3)에서 약 175 kJ/mol의 활성화 에너지와 약 21~24/s의 빈도 인자를 갖다가 두 번째 발열반응 구간에서 활성화 에너지와 빈도 인자가 각각 약 125 kJ/mol, 15~17/s로 줄어들었다. 이는 반응 초반에 Viton-b가 분해되면서 반응을 개시하고 이어지는 반응을 촉진하기 때문에 연료와 산화제 간의 연소반응에 요구되는 활성화 에너지가 낮아지게 된다.
3.3.2 노화로 인한 화학반응 인자 변화
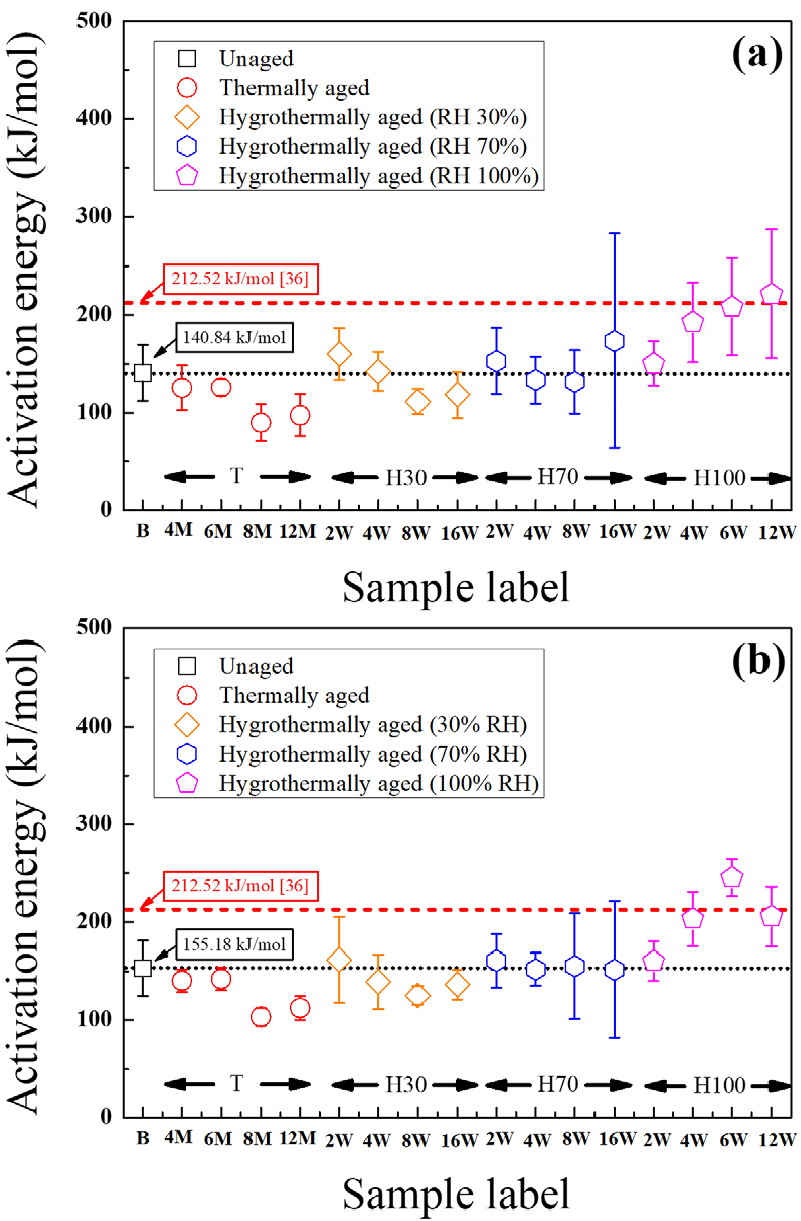
앞서 제시한 비노화 ZPP에 대해서 수행한 것과 같은 등전환 방법을 통해 나머지 16개의 노화된 시료들에 대해서도 kinetic parameter들을 추출하였으며, Fig. 6에 그 결과가 제시되어있다. α가 0.1부터 0.9까지의 범위에서 각 시료에 대한 활성화 에너지의 평균값은 기호로, 표준편차는 막대로 표시하였다. 이때, 본 연구에서는 미분 기반의 추출법인 Friedman method[36]와 적분 기반의 추출법인 Ozawa method[37] 두 종류를 사용하여 도출한 결과들을 모두 제시하였다. 이는 DSC 실험 결과가 노이즈에 민감하고 감도가 높기 때문에 계산된 kinetic parameter 값 자체에 큰 편차가 나타날 수 있다. 따라서 적분 기반의 계산 방법인 Ozawa method도 동시에 계산을 진행하여 두 가지 계산 방법으로부터 얻은 파라미터 간의 변동성을 비교해봄으로써 더욱 자세하고 명확하게 반응역학 분석을 수행하고자 하였다.
Fig. 6(a)은 Friedman 등전환법에 기초하여[35], [36], [37] 도출된 활성화 에너지를 보여주고 있는데, Baseline의 경우 140.84 kJ/mol의 평균값을 가졌다. 이때, 선행 연구를 통해 계산된 ZPP의 활성화 에너지는 빨간색 dash line으로 나타나 있으며, 212.52 kJ/mol의 값을 가짐을 알 수 있다[32]. 본 연구에서 제시한 ZPP의 활성화 에너지와 선행연구에서 제시된 활성화 에너지에서 차이가 발생하는 이유로는 선행연구에서는 654.17-684.89 K의 제한된 온도영역만을 반응 구간으로 고려한 것을 원인으로 제시할 수 있다. 뿐만 아니라, 활성화 에너지를 계산할 때 등전환법이 아닌 ASTM E698-99 method를 적용하여 계산하였기 때문에 다른 값을 가짐을 추측해볼 수 있다.
각 노화된 시료들에 대한 활성화 에너지 결과를 보면, 전체적으로 상대습도 레벨이 증가할수록 활성화 에너지도 증가하는 경향성을 확인해볼 수 있었다. 뿐만 아니라 여러 반응이 중첩되어 발열 현상이 진행되다 보니, 활성화 에너지가 반응이 종결될 때까지 변동되는 현상이 나타나 시료마다 어느 정도의 편차를 가지게 되는 것을 알 수 있다[43].
이때, 가속노화된 샘플의 경우, 노화 기간이 늘어남에 따라 활성화 에너지가 점차 감소하는 경향성을 보였는데, 이는 산화제인 KClO4의 분해 현상으로 인해 생성된 KClO3 성분으로 설명이 가능하다. 보다 반응성이 좋은 KClO3로 인하여 낮은 온도에서도 더 쉽게 산소로 분리가 이루어지는데, 이는 연료와 산화제 간에 반응이 개시되기 위해 요구되는 energy barrier를 낮추는 역할을 한다. 따라서 가속노화 시료에서 점차적으로 활성화 에너지가 낮아지는 경향성이 나타나게 되는 것이라고 할 수 있다[44], [45], [46].
30% RH 조건에서 노화된 시료(H30_2W~16W)에서도 마찬가지의 이유로 초기에는 높아진 활성화 에너지를 갖다가 노화 기간이 길어질수록 활성화 에너지가 다소 낮아지게 되는 모습을 확인해볼 수 있다. 반면, 70% RH 이상의 조건(H70_2W~16W)에서는 활성화 에너지가 노화 기간에 비례하여 증가하는 모습을 볼 수 있는데, 이는 노화로 인한 산화제 분해 현상보다 연료 산화가 더욱 우세하게 발생하기 때문이다. 산화지르코늄이 생성됨에 따라 ZPP는 더욱 안정적인 상태에 위치하게 되고 이에 따라 활성화 에너지도 계속해서 증가하게 되는 것이다.
한편, 노화 기간이 길어짐에 따라 ZPP 시료에 대한 활성화 에너지 변동성이 더욱 증가하는 현상 또한 확인해볼 수 있었다. 이러한 kinetic parameter의 높은 편차는 ZPP의 발열 반응이 진행될 때 복잡한 여러 개의 반응이 동시에 나타난다는 것을 의미한다[44], [47]. 이때, 노화될수록 편차가 커지는 현상은 노화로 인하여 ZPP내에 다양한 reactants 및 products가 생성되고 이로 인하여 반응 메커니즘이 더욱더 복잡해지기 때문이다.
Fig. 6(b)에서 제시된 Ozawa method를 적용하여 활성화 에너지를 계산한 결과도 Friedman method를 통해 구한 것과 비슷한 변화를 확인해볼 수 있었다. 그런데 Ozawa method를 적용한 결과가 Friedman method에서 추출한 활성화 에너지보다 대체로 낮은 편차를 보였다. 이는 미분 방식의 실험측정기반의 DSC 결과를 적분 방식으로 kinetic parameter를 추출하면서 실험과정에서 발생한 노이즈를 상쇄시키는 효과로 해석해볼 수 있다.
3.4 피크 분리 수행 결과
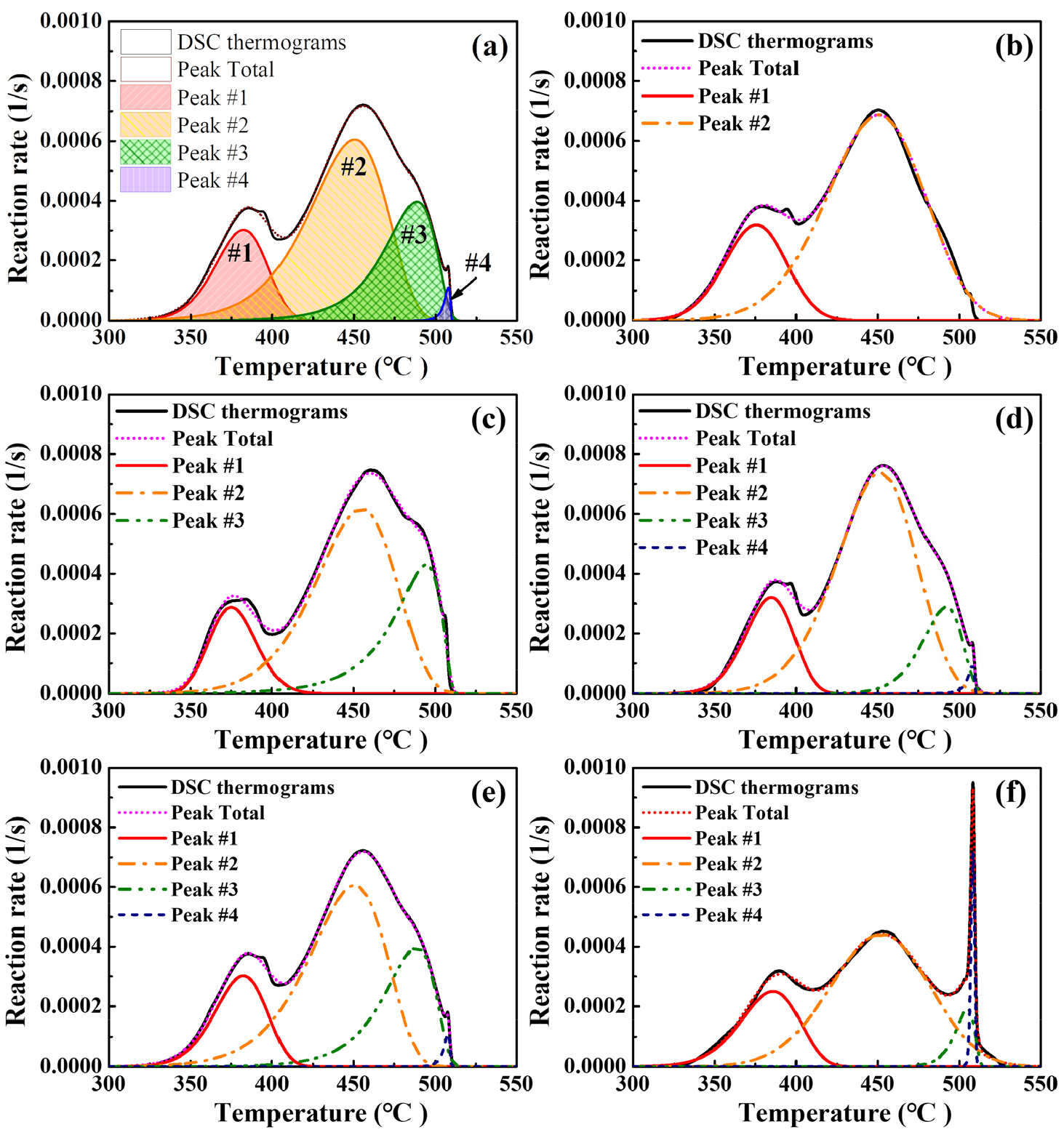
DSC 열량 분석을 통해 얻은 실험 결과들 모두 발열반응 영역에서 여러 개의 하위피크가 중첩되어있는 형태를 가지는 것을 확인해볼 수 있었다. 본 연구에서는 이렇게 여러 개의 세부 반응으로 중첩되어있는 발열반응에 peak separation 기법을 적용하여 더욱 세밀한 반응 분석을 통해 각 하위 반응 중에서 노화에 취약한 반응들을 확인해보고자 하였다. 이때, peak separation 분석 결과는 승온 속도 3°C/min에서 수행된 DSC 열분석도 데이터를 사용하였다. ZPP의 경우 선행연구들과 실험을 통해 얻은 결과들을 종합해본 결과, Table 4와 같이 총 4개의 하위반응으로 구성됨을 확인해볼 수 있었다[8], [42], [48]. Fig. 7(a)에서 각각의 세부 반응이 나타나는 온도 범위와 개형을 확인해볼 수 있으며, 해당 결과는 ‘H70_8W’의 결과로 네 가지의 모든 반응이 나타나있어 개념도로써 활용하였다.
Table 4.
Sub-reactions of the ZPP exothermic reaction
이때, 반응 생성물인 ZrO2와 KCl은 하위반응에 참여하지 않는데, 그 이유로는 KCl은 770°C 이상에서 분해할 수 있기 때문이다. 한편, ZrO2는 적어도 1,100°C 이하의 온도에서는 화학적 구조를 유지하는 안정한 물질로 알려져 있으므로, 본 연구에서 설정한 온도영역에서는 반응에 참여할 수 없다.
Fig. 7은 노화되지 않은 ZPP(Fig. 7(b))를 포함하여 가속노화된 ZPP(Fig. 7(c)), 수분 노화된 ZPP(Fig. 7(d-f))에 대한 peak separation 분석 결과를 보여주고 있다. Fig. 7(a)에서는 본 논문에서 다루는 ZPP 발열반응을 이루는 네 종류의 반응을 그래프로 도시한 것이다.
Baseline의 경우, 앞서 DSC 열분석을 통해 확인해본 결과와 마찬가지로 primary thermal reaction과 secondary thermal reaction으로 이루어져 있는 것을 알 수 있다. 그런데 ZPP에 가속 노화를 가했을 때, Fig. 7(c)과 같이 KClO3의 분해반응을 의미하는 Peak #3가 새롭게 등장한 것을 볼 수 있다. 이는 다른 시료들의 결과와 비교해보았을 때에도 상당한 양의 KClO3가 KClO4로부터 생성되었으며 연소반응과정에서도 지배적인 역할을 수행하는 것을 알 수 있다.
Fig. 7(d-f)은 각각 30% RH, 70% RH, 100% RH 조건에서 수분 노화된 ZPP의 peak separation 결과를 보여준다. 이때, 세 가지 경우 모두 수분 환경에 의해 연료 산화가 빠르게 진행되어, 반응에 참여하지 못한 잔여 산화제가 발생하는 것을 Peak #4의 존재로 추정할 수 있다.
뿐만 아니라, 상대습도 레벨이 증가할수록 산화제인 KClO4와 연료인 Zr 간의 연소반응이 약해지고, 노화로 인한 생성된 KClO3 분해반응과 잔류 KClO4의 분해반응이 더욱 강해지는 현상을 특징적으로 확인해볼 수 있었다.
3.5 추출한 reaction kinetics를 활용한 ZPP의 반응 모사 결과
Fig. 8은 반응의 진행 정도를 나타내는 α가 반응 시작 전인 α = 0부터 반응 완료를 나타내는 α = 1에 도달했을 때, 노화 조건마다 어떠한 양상을 보이는지 모사한 결과를 나타낸다. 계산은 식 (6)를 바탕으로 진행되었으며, 이때 반영된 활성화 에너지와 빈도 인자는 Friedman 등전환법을 통해 추출한 값을 적용하였다. 따라서 노화되지 않은 ZPP를 포함하여 네 개의 다른 조건에서 노화된 시료들에 대해서 시간에 따른 반응 진행양상을 확인해볼 수 있었다.
위 식에서 R은 이상기체 상수, Tα는 절대온도(단위 K), Eα는 활성화 에너지(단위 kJ/mol), Aα는 빈도 인자(단위 1/s)를 의미하며 각 파라미터의 아래 첨자 α는 각 반응률에 해당하는 파라미터 값을 나타낸다.
Constant volume condition을 가정하여 모사를 진행하였으며, 일정한 압력 조건에서 ZPP의 비열과 밀도는 각각 250 J/kg-K, 4,600 kg/m3를 적용하여 계산을 수행하였다[49].
그리고 해당 시료들의 반응을 개시를 위해 초기조건으로 1,100 K의 온도를 가해주었다. 해당 온도를 설정한 이유로는, 1,100 K에서 모든 시료가 즉시 반응이 개시될 뿐만 아니라 반응이 끝까지 완료되었기 때문이다.
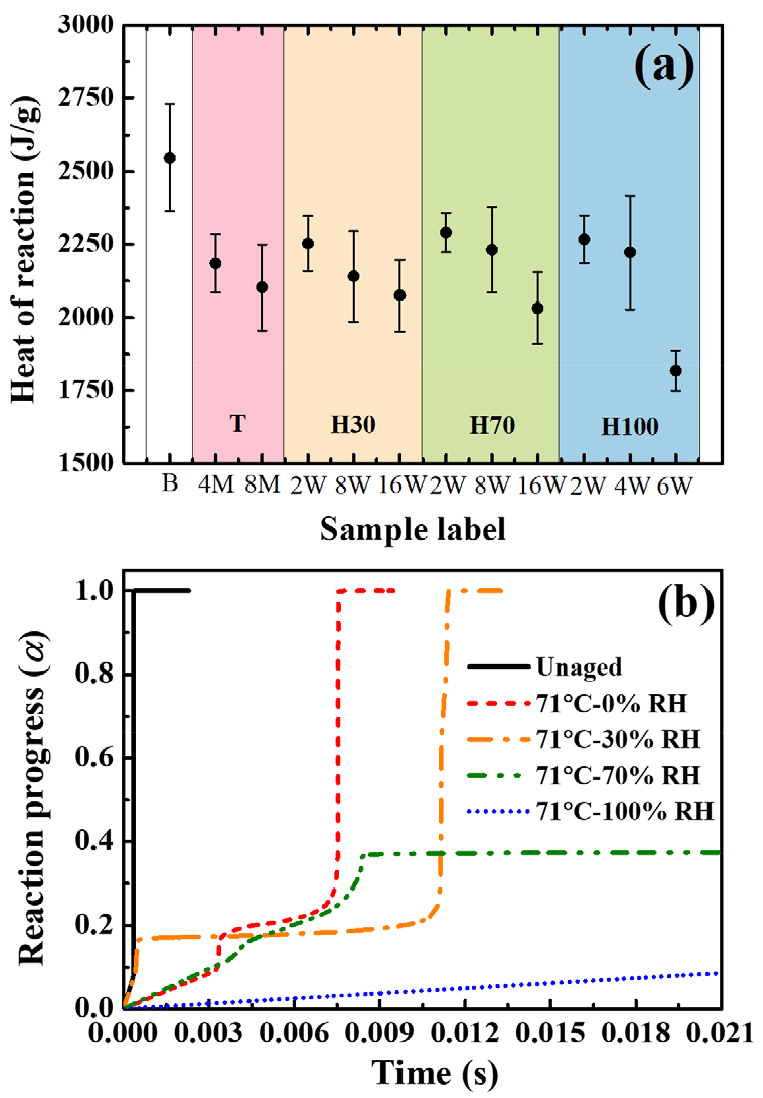
Fig. 8(b)은 본 연구에서 수행한 모사 결과를 보여주고 있는데, 상대습도 레벨이 점차 증가함에 따라 반응률이 지연되는 모습을 확인해볼 수 있었다. 특히 70% RH 노화 조건에서는 반응이 완전히 진행되지 못하고 약 40% 정도의 반응까지만 완료되었으며, 100% RH 조건에서는 반응 진행이 채 10%도 안 되게 매우 더디게 증가하는 모습을 볼 수 있었다. 따라서 높은 수분 환경이 ZPP의 열 성능을 매우 악화시킬 수 있으며 심지어는 발사체의 불발까지 초래할 수 있음을 추정해볼 수 있다.
Fig. 8(a)에 제시되어있는 발열량 데이터를 비교해보면, 노화 주차 16주를 기준으로 비 노화 시료를 포함하여 가속노화(T)와 30% RH 조건(H30)에서 노화된 ZPP 시료들은 약 2,100 kJ/g에 상당하는 열을 방출하였다. 그런데 그 이상의 습도 조건에서 노화된 시료들(H70, H100)은 약 1,800 kJ/g의 반응열만을 보유하였다.
이때, Fig. 8(a)에서 발열량이 2,000 kJ/g 이하로 줄어든 70% RH와 100% RH 노화 조건에서는 반응이 매우 지연되거나 더 나아가지 못하는 모습을 보였는데, 이는 높은 수분 함량으로 인하여 연료의 상당량이 산화되고 ZPP의 화학적 조성이 변질되어 설계된 열 성능을 제대로 발휘하지 못하는 것으로 해석해볼 수 있다.
3.6 ZPP의 예상수명 계산
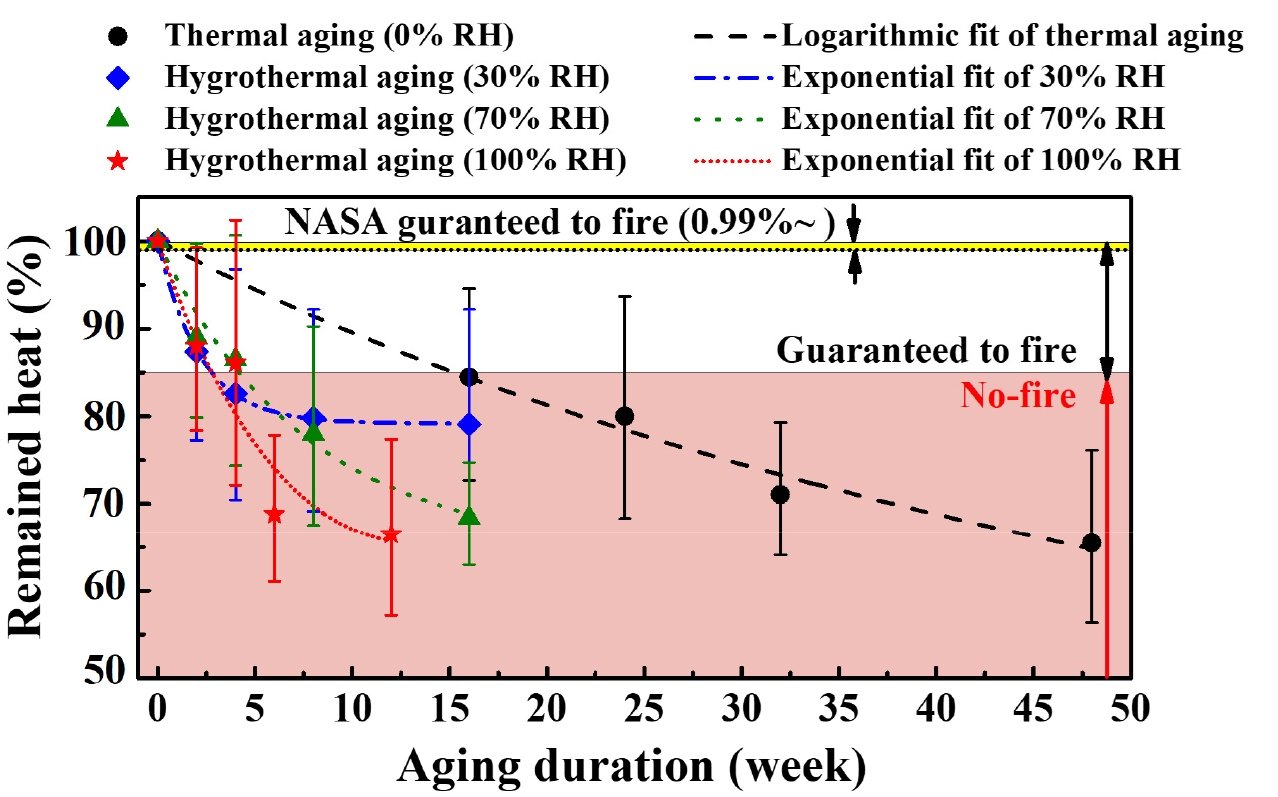
ZPP는 열화에 상당히 강하다고 알려진 파이로테크닉 물질 중 하나이지만, 수분 환경이 ZPP에 끼치는 영향은 아직 정확히 밝혀진 바 없다. 따라서 본 연구에서 다룬 다양한 수분 노화 조건들에 대한 ZPP의 실험적 특성을 바탕으로 수명을 예측해봄으로써 ZPP 자체적인 취약한 특성을 파악하고 이를 활용하여 효과적인 보관과 성능향상에 도움을 주고자 하였다. Fig. 9는 네 가지의 노화 조건과 노화 기간에 따른 발열량 감소양상과 이에 해당하는 모델을 제시하고 있다. 여기서 잔여 발열량 즉, remained heat은 노화되지 않은 ZPP가 보유한 발열량에 대비하여 노화된 ZPP 시료의 발열량이 얼마나 남아있는지를 뜻하며, ΔHaged /ΔHunaged와 같이 나타낼 수 있다.
각 노화 샘플에 대한 수명을 언급하기에 앞서, 각 노화 조건에 따른 ZPP 시료에서 다른 발열량 감소패턴을 확인해볼 수 있었다. 가속노화된 시료의 경우 식 (7)과 같이 logarithmic decay pattern으로 발열량이 서서히 줄어드는 반면, 수분 노화된 ZPP의 경우 식 (8)과 식 (9)과 같이 exponential curve를 따라 열이 감소하는 형태를 보였다. 이때, 상대습도 레벨이 증가할수록 더욱더 급격하게 열이 감소하는 모습을 확인해볼 수 있었다.
이때, 위 식에서 t는 노화 주차를 의미하며 φ0,
φ1, φ2는 fitting 상수를 의미한다. 본 연구에서 위와 같은 노화 모델을 선정한 기준으로는 root mean square error가 가장 작은 값을 가지는 경험 식을 채택하였다.
보통 ZPP와 같은 파이로테크닉 개시제가 전체 시스템을 고려하여 설계될 때, 발열량의 마진을 적어도 두 배가량 설정하여 생산[50]이 된다고 알려져 있다. 하지만 온도와 습도 조건과 더불어 기계적 특성을 포함한 다양한 환경 조건이 관여한다고 가정하면, 더 큰 성능 악화를 초래할 수 있다. Burgess et al.[51]에 따르면, UV radiation을 통해 물질 내에서 radical들이 생성될 수 있을 뿐만 아니라 이렇게 흡수한 빛으로 인하여 explosive 혹은 polymer와 같은 물질들에 불순물이 생겨날 수 있다고 경고하였다. 또한, Thompson et al.[52]은 thermal cycling tests를 통해 explosives의 성능감소와 더불어 물리적 특성의 변화도 확인하였다. 따라서 노화에 있어 주요한 파라미터가 온도와 습도이긴 하지만 그 외의 다른 다양한 변수들도 관여할 수 있으므로 예외상황은 언제나 존재한다고 볼 수 있다.
따라서 본 연구에서는 ZPP가 약 85% 이상의 발열량을 보유하고 있으면 성능을 보장한다고 설정하였으며, 그 이하의 조건에서는 불발될 것이라고 가정하였다. 따라서 Fig. 9에서 ‘Guaranteed to fire’ 영역 내에 있는 노화된 시료들에 대한 kinetic parameter들을 식 (4)에 대입하여 AF 값을 계산하고 이를 식 (3)에 대입하여 최종적으로 예상되는 ZPP의 수명을 얻을 수 있었다.
Table 5에 계산한 수명이 제시되어 있는데, Friedman method를 이용하여 얻은 활성화 에너지를 대입했을 때와 Ozawa method를 통해 구한 활성화 에너지를 대입했을 때 구한 수명 간에 차이가 존재했다. Friedman method를 기준으로 하였을 때, 일반 ZPP의 수명은 약 277.48년이었으며 넉 달 동안 가속노화(T)를 시켰을 때는 잔여 수명이 약 120년으로 계산되었다. 이때, 수분 노화된 시료의 수명을 보면 가속노화된 시료와 비교해보았을 때 30% RH 조건(H30)에서는 수명이 68.15년, 70% RH 조건(H70)에서는 48.49년, 100% RH 조건(H100)에서는 43.04년으로 현저하게 줄어들었음을 확인해볼 수 있다.
Table 5.
Acceleration factor and Lifespan for the aging groups
따라서 습도가 높은 환경이 ZPP의 수명 단축에 상당한 영향을 끼치고 있다는 사실을 확인해볼 수 있었다. Ozawa method 기준으로 분석을 진행해보면, 수명이 대체적으로 Friedman method를 통해 구한 수명보다 큰 값을 가졌다. 수명 간에 약간의 차이는 있었지만, 노화가 될 시에 수명이 감소하는 패턴은 일치하는 모습을 볼 수 있었다. 특히 수분노화 된 시료 중에서 상대습도가 높아질수록 수명이 점차 감소한다는 경향성은 동일하게 보여주고 있다.
이 때, NASA에서 제공한 ZPP cartridge의 사용기한은 약 10년으로 권장되는데[53], 이는 ZPP가 본 발열량의 99% 이상을 보유하고 있을 때의 기준으로 꽤 엄격하게 요구되고 있다. 해당 기준은 ZPP를 포함한 최종 제품 출하에 있어서 최대의 신뢰도를 만족하기 위해 선정된 기준으로, 본 연구에서 설정한 85%의 발열량 기준보다 상당히 큰 값을 가지는 것을 알 수 있다. 따라서 목적 및 용도에 따라 요구되는 발열량의 한도는 달라질 수 있으며, 그에 따라 ZPP의 사용 기한 및 수명도 변동될 것이다.
4. 결 론
파이로테크닉 추진제 및 개시제의 수명 및 성능 유지와 관련하여 가장 큰 문제 중 하나가 해당 물질의 혼합 및 장전 과정에서 공기에 노출될 염려가 있다는 것과 이로 인하여 노화 과정에서 금속 연료의 산화 및 화학 조성의 변화를 통해 전체적인 수명의 단축을 초래할 수 있다는 것이다.
본 연구에서는 열에 의한 가속 노화뿐만 아니라 세 가지의 상대습도 조건을 고려하여, 수분 함량에 따라 ZPP 성분의 열적 성능과 화학적 조성이 어떻게 변화하는지 파악해볼 수 있었다. 그리고 실험 데이터를 기반으로 화학반응 인자들을 추출하여 반응 모사를 수행하고, 각 조건에 대한 ZPP의 수명을 예측해보았다.
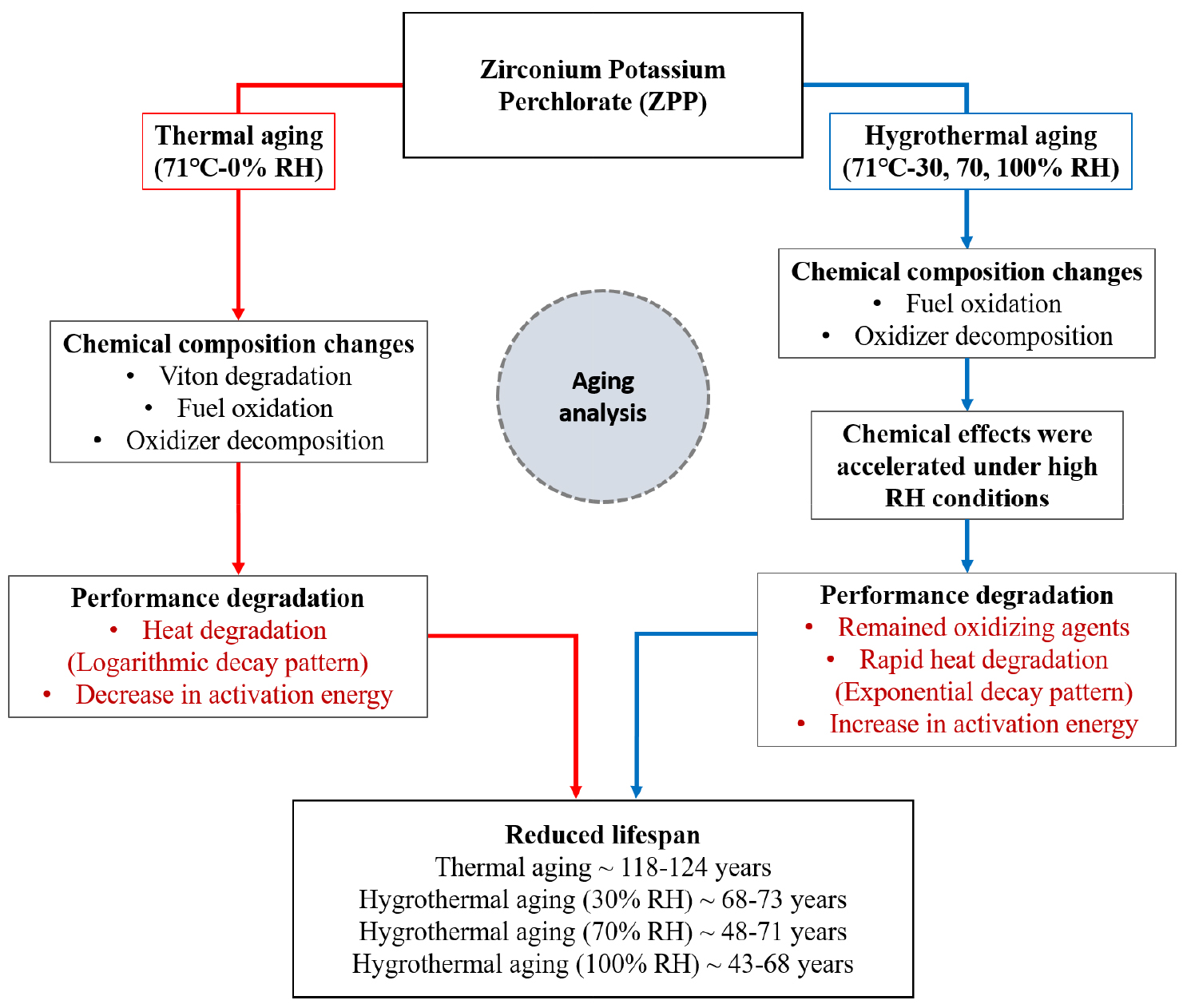
이를 통해, Fig. 10과 같이 노화중 수분이 관여할 시에 ZPP의 설계된 화학량론 조성의 변화를 초래하며, 이에 따라 나타나는 발열량 및 반응온도 및 활성화 에너지의 차이를 유발하여 성능 저하로 이끌 수 있음을 확인하였다. 가속노화의 경우 바인더 열화와 연료 산화와 산화제 분해 현상이 나타났으며, 수분 노화도 마찬가지로 연료 산화와 산화제 분해가 발생하였지만 연료 산화 효과가 더욱 강하게 발생하였다.
일반적으로, 노화가 진행되면 연료 입자 표면을 둘러싸고 있는 산화막의 두께가 점점 증가하여 산화제와의 반응 저해를 초래하며, 이에 따라 활성화 에너지는 높아지는 특성을 보이게 된다. 본 연구에서는 이렇게 활성화 에너지가 증가하는 현상을 특히 높은 상대습도 조건에서 수분 노화된 ZPP 시료들에서 찾아볼 수 있었다.
대부분의 경우, 노화 기간이 길어짐에 따라 활성화 에너지가 감소하다가 증가하는 경향을 보였는데, 이는 산화제의 분해현상과 연료의 산화 반응이 중첩되어 나타난 결과와 연관지어 해석해볼 수 있다. 다시 말해 초기에는 산화제 분해현상으로 인하여 활성화 에너지가 감소하다가 노화 기간이 점차 길어질수록 연료 산화가 더욱 두드러져 활성화 에너지 값이 증가하게 되는 것이다. 한편, 노화 기간이 길어짐에 따라 활성화 에너지의 편차 또한 증가하는 모습을 확인해볼 수 있었는데, 이는 노화 과정에서 ZPP 내부에 생성된 분해물로 인하여 ZPP의 연소반응이 더욱 복잡하게 진행된다는 것을 뜻한다.
열성능 측면에서 ZPP의 노화 분석을 접근해보았을 때, 상대습도와 노화 기간이 증가함에 따라 발열량은 급격하게 감소하는 경향을 드러냈다. 이는 앞서 언급한 것처럼, 수분함량이 ZPP 내부의 금속연료의 산화와 산화제 분해를 가속하는 역할을 수행하며 결국에는 조성의 변화를 초래하여 열 성능의 저하라는 결과를 이끌어내게 된다. 이때 가속노화된 시료는 logarithmic decay model을 따르지만, 수분 노화된 시료는 exponential decay model을 따라 발열량 감소 경향에 있어 뚜렷한 패턴의 차이 또한 확인해볼 수 있었다.
그리고 Friedman과 Ozawa method를 통해 추출한 kinetic parameter들을 van’t Hoff equation에 대입하여, 잔여 발열량이 85%일 때를 마진으로 설계하였을 때 ZPP에 대한 예상 수명을 계산해보았다. Fig. 10에서도 나타나 있듯이, 두 방법 모두 노화된 시료에서 수명이 감소하는 경향성을 보였으며 상대습도 레벨이 증가할수록 수명도 급격하게 감소하는 것을 확인해볼 수 있었다. 노화되지 않은 ZPP의 경우 수명이 약 270년 이상으로 예측이 되었는데, 실제 환경을 고려하면 온도나 습도뿐만 아니라 진동이나 충격, thermal cycling 등과 같은 외부에서 다양한 요소들이 개입될 확률이 높으므로 실제 수명은 이보다 더 단축된 값을 가질 수 있다.
결과적으로, 본 연구를 통해서 ZPP 개시제의 경우 수분 환경에 매우 취약한 특성을 가진다는 것을 확인해볼 수 있었으며, 설계된 성능을 확보하고 유지하기 위해서는 건조된 환경에서의 보관이 권장된다. 비록 본 연구에서는 자연 노화된 시료가 아닌 인공적으로 가속 노화된 시료들을 사용하였기 때문에 정확한 노화 특성 제공에 있어 약간의 어려움이 있을 수 있다. 하지만, 적어도 온도와 습도가 ZPP의 화학적 조성과 열적 성능에 끼치는 영향에서는 명확한 결과를 제시해내었다고 할 수 있다. 따라서 본 연구의 결과를 참고하면 주요 환경 특성인 ‘온도’와 ‘습도’가 ZPP와 같이 금속연료와 산화제, 폴리머 바인더로 이루어진 유사한 조성을 가진 물질에 대한 노화 효과에 대해 유사한 결과를 이끌어낼 수 있을 것이다. 이는 추후 추진제 및 파이로테크닉 관련 개시제 설계에 있어 활용될 수 있을 것이라 기대되는 바이다.