1. 서 론
2. 수치해석 방법
2.1 수치해석 모델
2.2 경계조건
2.3 화학반응 메커니즘
3. 결과 및 고찰
3.1 물성치 평가
3.2 열유동 및 연료 전환율
3.3 흡열량
4. 결 론
1. 서 론
로켓 및 스크램제트 등의 추진 및 발전 시스템에서 연소기는 종종 고온, 고압에서 작동한다. 내구성 유지와 엔진 성능 향상을 위해 연소기의 온도 조절은 중요하다. 탄화수소 계열의 연료를 사용한 재생냉각은 연소기 벽면 온도를 낮추기 위한 대표적인 해결책 중 하나이다. 재생냉각 기술을 효과적으로 적용하기 위해서는 초임계압 상태에서의 연료에 대한 물성치, 유동, 전환율, 열전달, 흡열량 등에 대한 정보가 필요하다[1]. 따라서, 탄화수소 연료의 열분해 반응에 대한 실험데이터와 이를 바탕으로 검증된 화학반응 기구(kinetic mechanism)를 통한 수치해석 결과를 분석함으로써 필요한 데이터를 확보하고 분석하는 과정이 요구된다.
재생냉각에 사용되는 대표적인 항공유로는 Jet A-1, JP-7, JP-8 등의 연료들이 있다. 이러한 연료들은 수백가지 화학성분으로 구성된 혼합물로 열분해 경로를 모두 파악하는 것은 현실적으로 불가능하다. 이를 해결하기 위해 이전 연구들에서 탄화수소 연료와 유사한 탄소 개수 및 특성을 갖고 있는 대표 화학종을 선정하여 실험 및 수치해석을 수행하였다[2,3,4,5,6,7]. 또한 선정된 연료를 수치해석에 적용하기 위해서는 압력과 온도 등에 대한 열분해 반응이 고려된 화학반응 메커니즘이 필요하다. 특히, Ward 등[2]은 항공유의 주성분인 n-decane과 n-dodecane을 통해 one-step global 모델인 proportional product distribution (PPD) 모델을 개발하였으며, 이 PPD 모델은 열분해 반응을, 초기 전환율 20% 이하에서 효과적으로 모사하는 모델이다. Zhu 등[3]은 n-decane의 열분해 반응 실험을 통하여 초기 전환율 13% 이하에서 잘 일치하는 PPD 모델을 개발하였다. 개발한 PPD 모델에 실제 초임계압 물성치를 삽입하여 계산하였다. Xu 등[4]은 초기 분해 반응식에 중요 화학종들의 반응단계를 추가하여 만든 상세화학반응식을 이용하여 RP-3 열분해 반응 수치해석에 적용하였다. 이후에도 여러 연구에서 같은 방식의 열분해 메커니즘을 개발하고 검증하였다. 하지만, 여전히 다양한 조건(연료 유량등)에서의 열분해 반응 특성에 대한 정보가 부족한 실정이다.
본 연구에서는 초임계압에서 n-dodecane의 열분해 반응 특성을 파악하고자 2차원 형상의 원통관 내에서 연료의 질량 유량(mass flow rate)을 변경하며 수치해석을 수행하였다. 열분해 반응의 유무에 따른 반응유동장의 차이를 파악하기 위해 먼저, 화학반응을 고려하지 않고 n-dodecane의 순수 유동 계산을 수행하였다. 다음으로, 초기 열분해 반응을 고려한, Zhang 등[5]이 개발한 n-dodecane용 PPD 모델을 적용하여 수치해석을 수행하였다. PPD 모델의 개발/검증에 주로 사용되는 미세채널(micro channel) 형상을 2차원 형상으로 단순화하여 수치해석을 수행하였다. 수치해석 결과로부터 열분해 반응으로 인한 n-dodecane의 유동 변화, 흡열량, 물성치 등의 변화를 파악하고, 이러한 변화에 미치는 질량 유량의 효과를 조사하고자 한다.
2. 수치해석 방법
2.1 수치해석 모델
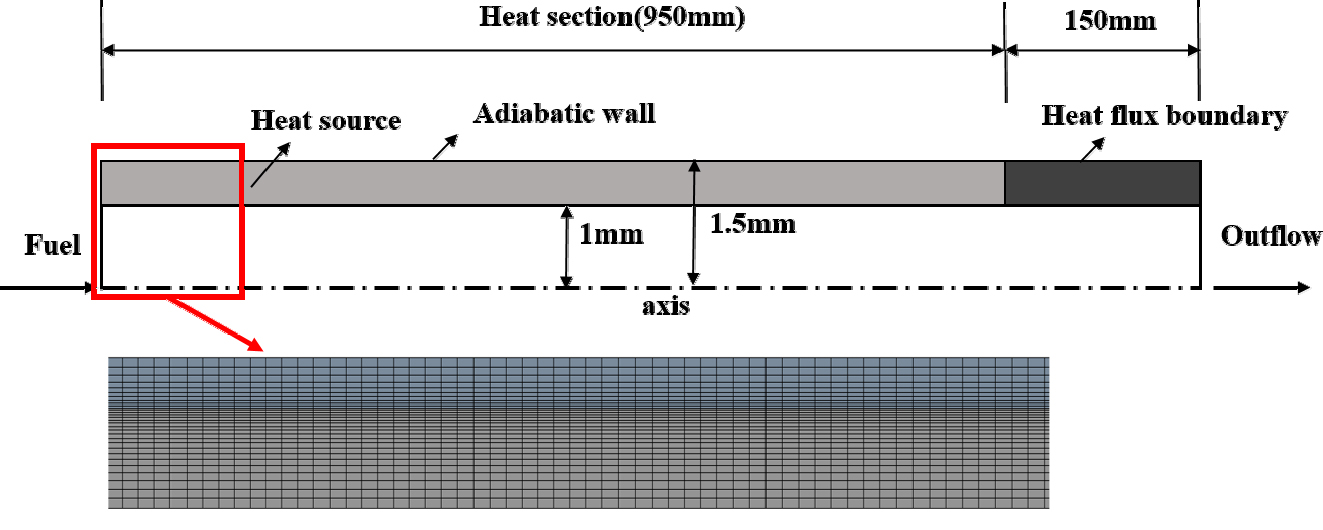
PPD 모델을 수립하기 위해 미세채널(micro channel) 실험과 유사한 원통관을 2차원 축대칭 형상으로 단순화하여 수치해석을 수행하였다. 원통관의 형상과 격자계를 Fig. 1에 나타내었으며, 사용된 총 격자수는 66,000개이다. 정렬격자계를 사용하였으며, 벽면과 유체사이의 열전달을 정확히 모사하기 위해 벽근처의 격자를 세밀하게 형성하였다.
2차원 정상상태 지배방정식을 채택하였으며, 연속방정식, 운동방정식, 에너지방정식, 화학종방정식, 그리고 상태방정식을 풀이를 통하여 반응 열유동 해석을 수행하였다[3]. 난류 모델은 SST k-ω 모델을 사용하였으며, 열분해 화학반응을 모사하기 위해 유한화학반응과 에디소산(finite-rate/eddy-dissapation) 모델을 적용하였다. 공간 차분으로는 2차 상류도식(2nd order upwind scheme)을 사용하였다. 해당 모델은 직경 2 mm, 길이 1,100 mm의 가늘고 긴 원통관으로 부력효과가 작기에 이를 고려하지 않았다. 유동 및 열분해를 모사하기 위해 범용 열유체 해석코드를 사용하였다.
2.2 경계조건
수치해석의 경계조건을 Table 1에 나타내었다. 작동압력과 입구 유체온도는 n-dodecane의 초임계 압력(1.806 MPa)과 온도(658.1 K)보다 높게 설정하였다. 입구에서는 특정 질량 유량의 n-dodecane을 주입하였다. 벽면 열경계 조건으로는 Zhang 등[5]의 수치해석 형상 모델이 변경된 점(3차원 → 2차원)을 고려하여, 열분해 초기반응에서 n-dodecane의 전환율을 잘 나타낼 수 있는 580 W의 열량을 고체 벽 내부에 균일하게 부여하였다.
Table 1.
Conditions for numerical simulations in the cylindrical tube
| Variables/parameters | Value |
| Pressure (MPa) | 3 |
| Inlet temperature (K) | 665 |
| Mass flow rate (Kg/h) | 3 ~ 4 |
| Heat input in the wall (W) | 580 |
2.3 화학반응 메커니즘
열분해 반응이 고려된 n-dodecane의 PPD 모델을 적용하여 수치해석을 수행하였다. 사용한 PPD model은 Zhang 등[5]에 의해 마이크로 반응기 실험을 통해 수립되고 검증되었다. 그 연구에서는 온도 조건으로 723.15~1003.15 K 범위에서 그리고 3 MPa의 동일 압력에서 실험을 수행하였다. 초기 반응율 13%까지의 1-step PPD 모델과 이후 13~73% 반응율에 대한 2-step PPD 모델을 수립하여 제시하였다. 본 논문에서는 초기 반응율 13%까지 검증된 1-step PPD 모델을 채택하였으며 모델 반응식은 다음과 같다.
반응 속도 상수는 아레니우스 식(Arrhenius form)으로 표현하여 다음과 같이 나타내었다.
위 식에서 A와 Ea는 각각 pre-exponential factor와 활성화 에너지(activation energy)를 나타낸다. 초기 분해반응에 대한 반응속도 상수는 first-order kinetics로 구했으며, Ea는 225.8 kJ/mol이며, A는 2.466×1014 s-1이다.
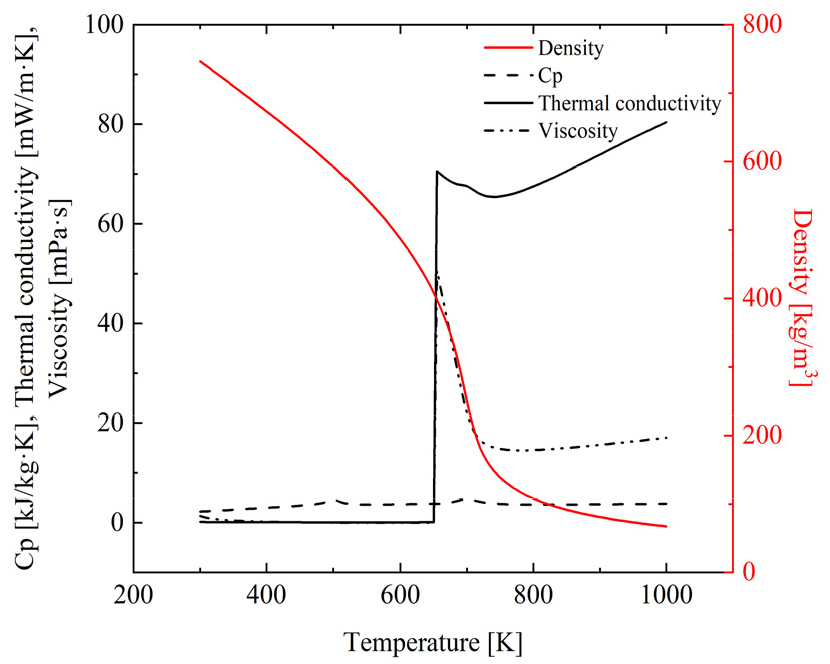
초임계압 탄화수소의 물성치를 모사하기 위해 NIST의 REFPROP 프로그램[9]을 이용하였다. 관심 범위내 온도와 압력에서 유체의 밀도, 점성, 비열, 열전도도 데이터를 추출하여, 각각의 화학종에 대한 열역학적 물성치 값을 다항식 곡선피팅(polynomial fitting)으로 나타내어 계산에 사용하였다. REFPROP을 통해 얻은 n-dodecane의 열역학적 물성치는 Fig. 2를 통해 나타내었다.
3. 결과 및 고찰
3.1 물성치 평가
다양한 질량 유량 조건에 대해서 열분해 반응의 수치해석을 수행하였다. REFPROP을 이용하여 PPD model의 모든 화학종에 대한 물성치를 초임계 상태 조건에서 계산하였으며, 이를 통해 열분해 반응에 따라 변화하는 물성치를 고려하였다.
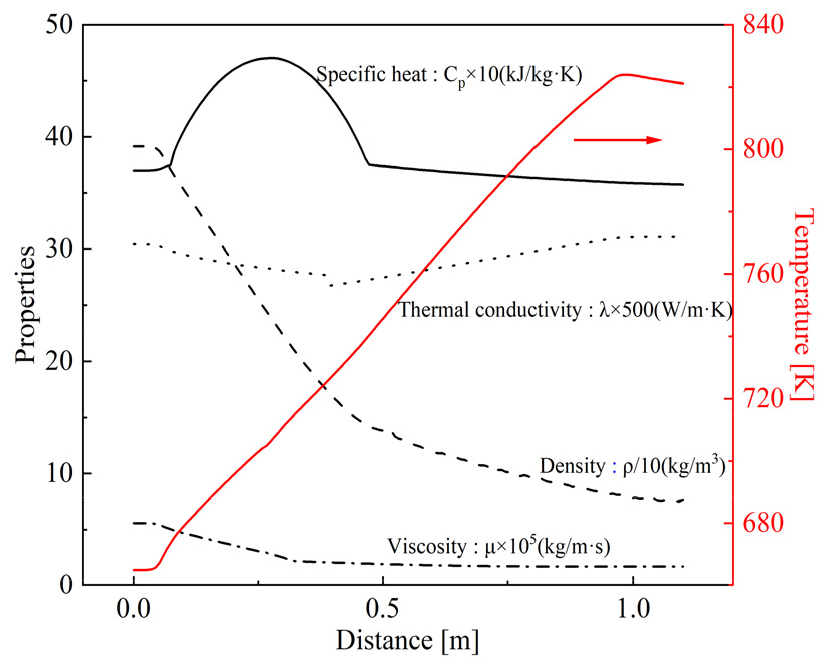
Fig. 3는 원통관 내에서 축방향으로 n-dodecane의 열분해 반응이 진행됨에 따라 변화하는 혼합물의 온도 밀도, 비열, 점성, 열전도도를 나타낸 것이다. 반응이 진행됨에 따라 큰 분자량을 가진 화학종에서 작은 분자량의 화학종으로 분해되므로 밀도와 점성이 감소함을 볼 수 있다. 비열의 경우 0.2 m 부근에서 급격하게 상승하는 것을 볼 수 있다. 이 위치에서 n-dodecane의 열분해 반응으로 생성된 혼합물의 유사 임계온도(pseudo-critical temperature)에 도달하기 때문이다.
3.2 열유동 및 연료 전환율
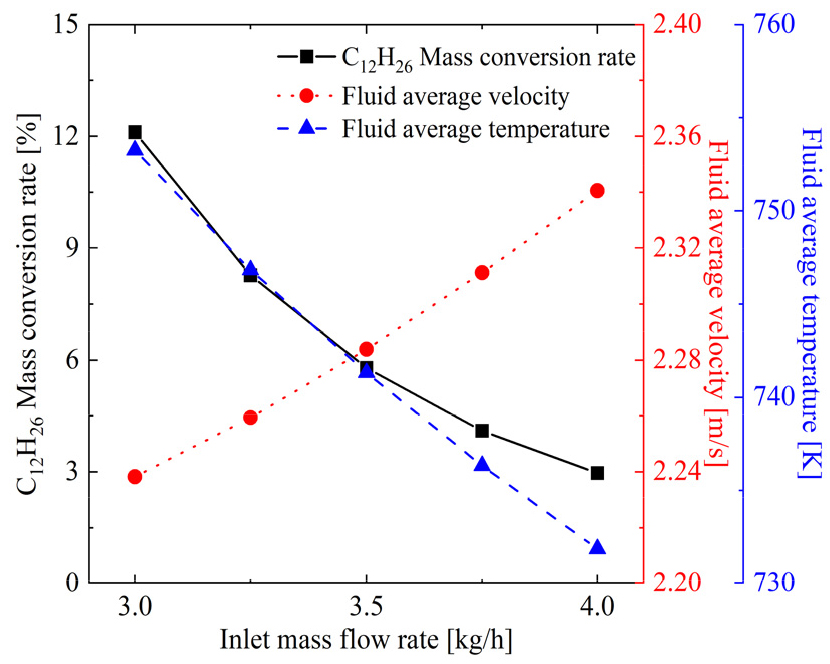
앞서 언급한 바와 같이, 580 W의 열생성이 있는 벽에 의해 결정되는 벽면 온도에서 그리고 3~4 kg/h의 질량유량 범위 내에서 계산을 수행하였다. Fig. 4은 질량 유량의 변화에 따른 n-dodecane 전환율과, (단면적 평균) 유체 속도, 온도를 나타낸 것이다. 유체의 평균 온도는 질량 유량이 낮을수록 높다. 이는 벽면에 가해지는 열 조건이 일정하여 낮은 질량 유량일수록 유체의 온도가 높게 나타난다. 전환율 또한 낮은 질량유량에서 가장 높게 나타나며, 유체의 평균 속도는 질량 유량이 높을수록 증가하였다.
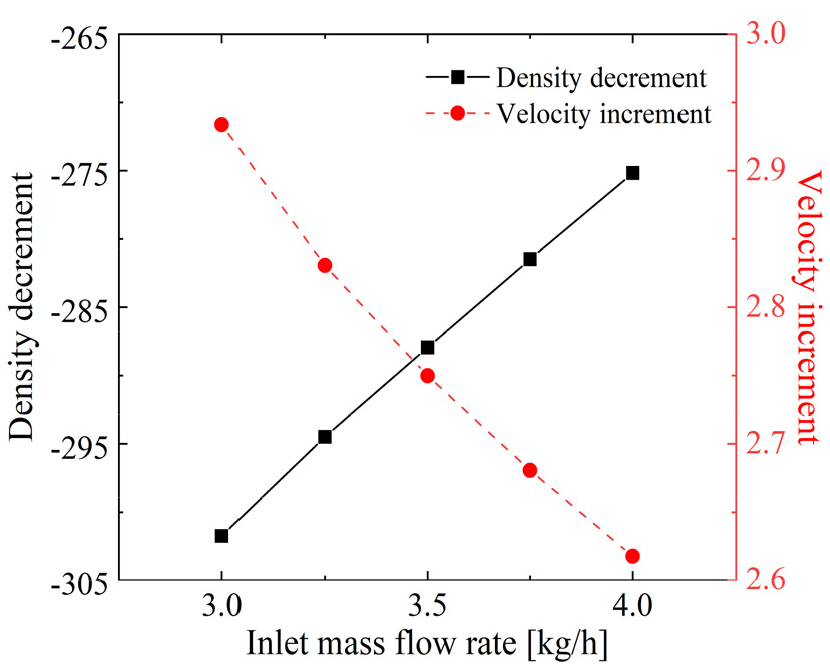
Fig. 5는 원통관을 통해 흐르는 유체의 속도와 밀도의 변화량을 알아보기 위해, 입구와 출구에서 단면적 평균을 통해 구한 평균 속도와 밀도의 차이를 각각 나타낸 것이다. 열분해 반응으로 인해 전환율이 높을수록 작은 분자량의 생성물로 활발히 전환되어 밀도의 감소량이 크고, 밀도가 감소한 만큼 속도의 증가량이 상승하는 것을 알 수 있다. 밀도에 영향을 줄 수 있는 온도 또한 Fig. 4에 나타난 것과 같이 낮은 질량유량에서 높게 유지되기 때문에 밀도의 감소량이 크다.
PPD 모델을 통하여 n-dodecane 열분해 반응을 수치해석 결과로 생성된 화학종들의 농도를 확인할 수 있다. Fig. 6에 n-dodecane의 초기 열분해 실험결과[5]와 본 수치해석 결과를 비교하여 나타내었다. 생성된 화학종들의 질량분율이 연료의 전환율에 따라 증가하는 경향성이 서로 잘 일치한다.
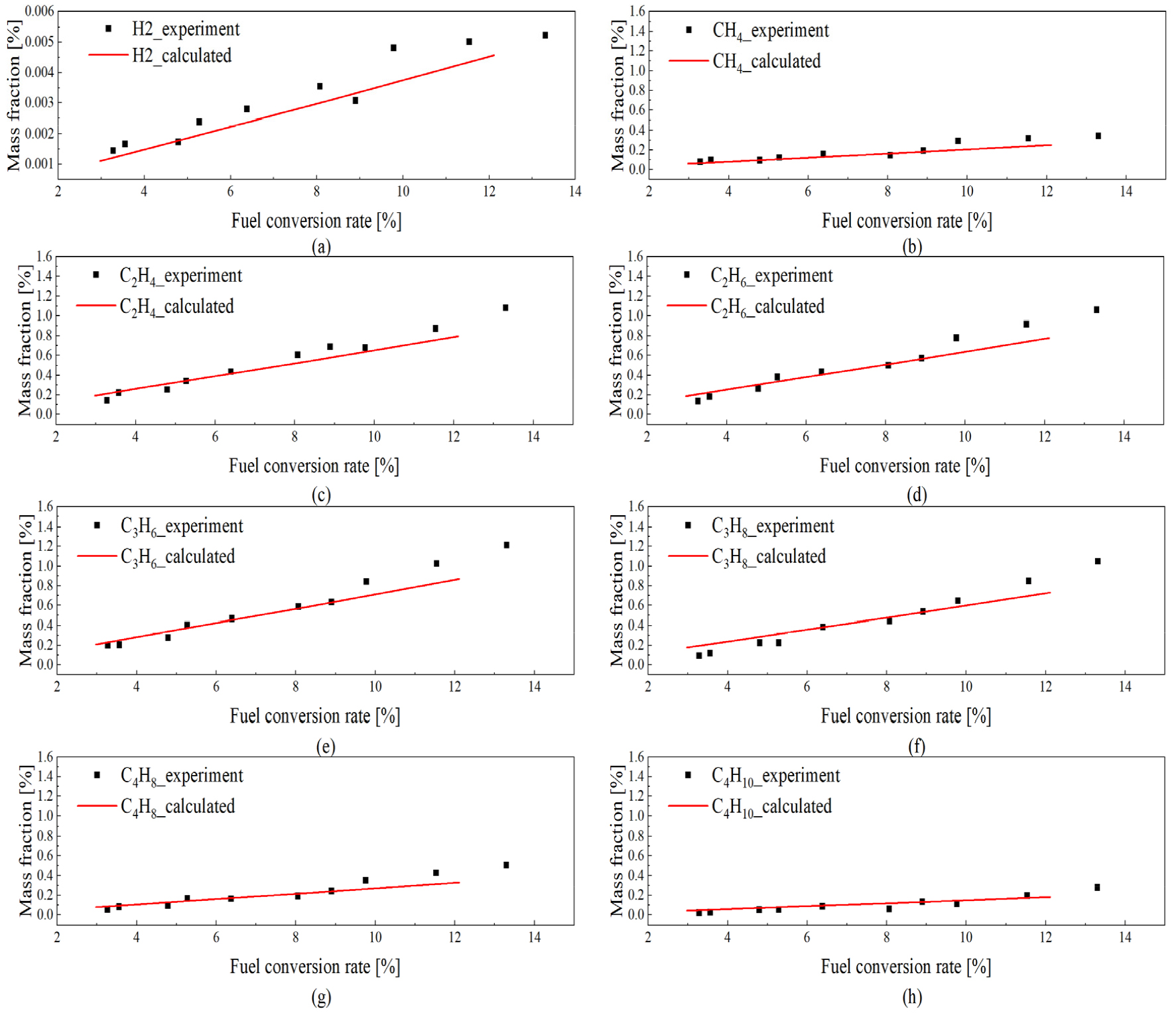
Fig. 6.
Comparison of mass fractions of product species from experiments[5] and numerical simulations. (a) H2, (b) CH4, (c) C2H4, (d) C2H6, (e) C3H6, (f) C3H8, (g) C4H8, and (h) C4H10.
3.3 흡열량
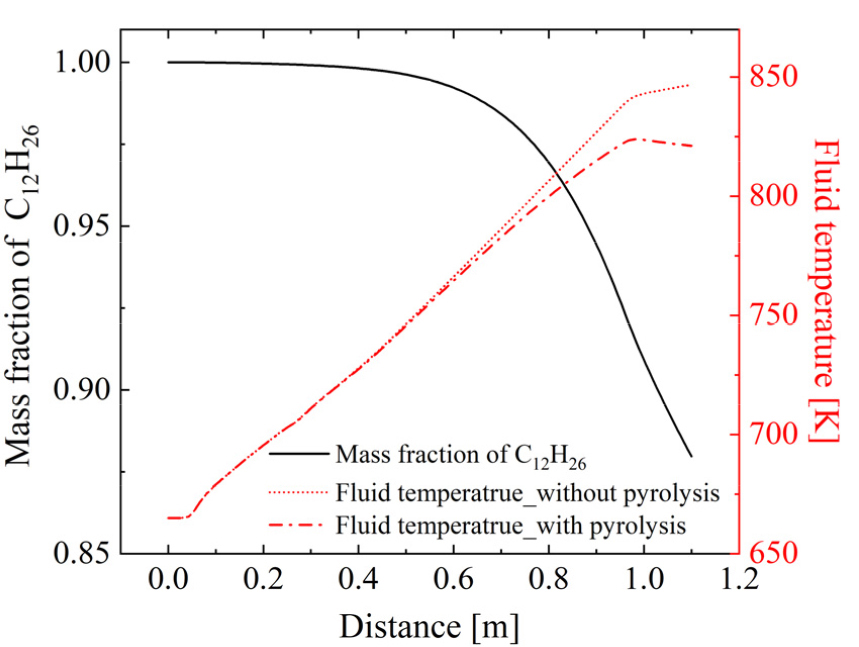
연료의 열분해 반응의 효과를 파악하기 위해 원통관내 유체의 온도를 비교하였다. 질량유량 3 kg/h 조건에서 미세채널내의 n-dodecane의 질량분율과 열분해 반응 유무에 따라 나타난 유체 중심의 온도를 Fig. 7에 나타내었다. 전환율이 급격하게 증가하는 약 0.5 m 부근부터 PPD 모델의 유/무에 따른 온도의 차이가 증가하는 것을 확인할 수 있다. PPD 모델을 사용한 경우 열분해 반응이 일어나며 유체의 온도가 비교적 낮다.
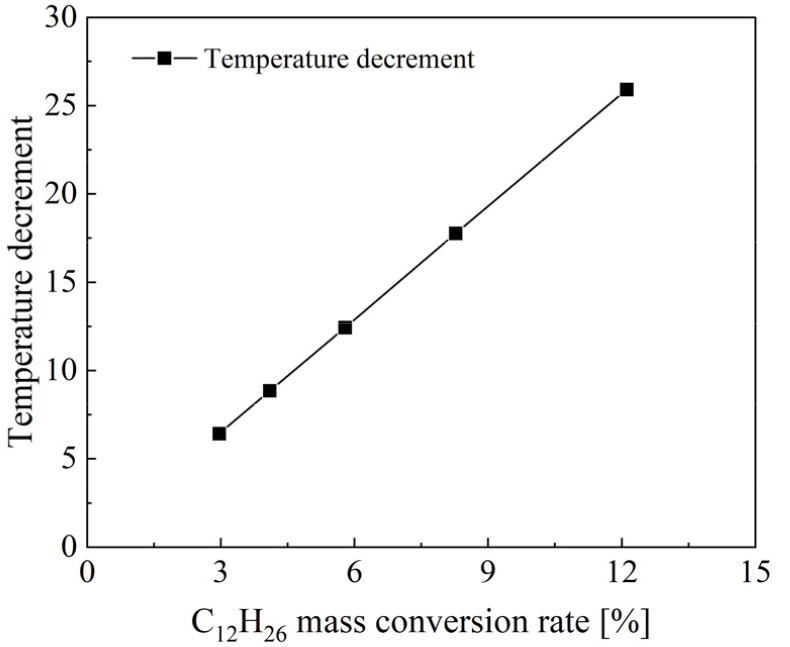
열분해 반응에 따른 유체 온도 감소로 원통관 입출구 온도차이가 발생하는데, 3~4 kg/h 질량유량 조건에서 연료의 전환율에 따른 온도 감소크기를 Fig. 8에 나타내었다. 온도의 감소크기는 열분해 반응 유무에 따른 출구 면적에서의 평균 온도값의 차이를 나타낸다. 전환율이 증가할수록 입출구 온도 차이가 커지는 것을 확인할 수 있다. 이러한 현상은 열분해 반응으로 흡열반응이 일어나는 것을 의미하며, 전환율이 커질수록 흡열반응이 증진되는 경향을 보인다.
흡열반응에 의한 반응열(heat of reaction)을 정량적으로 평가하여 나타내었다. 반응열을 구하는 식은 다음과 같다[7,8].
여기서 Shor은 반응열을 나타내며, hj는 화학종 j의 형성 엔탈피, Mj는 분자량, Rj는 생성율(production rate)이다. Shor가 음수일 경우 종합적으로 흡열반응이 일어남을 의미한다.
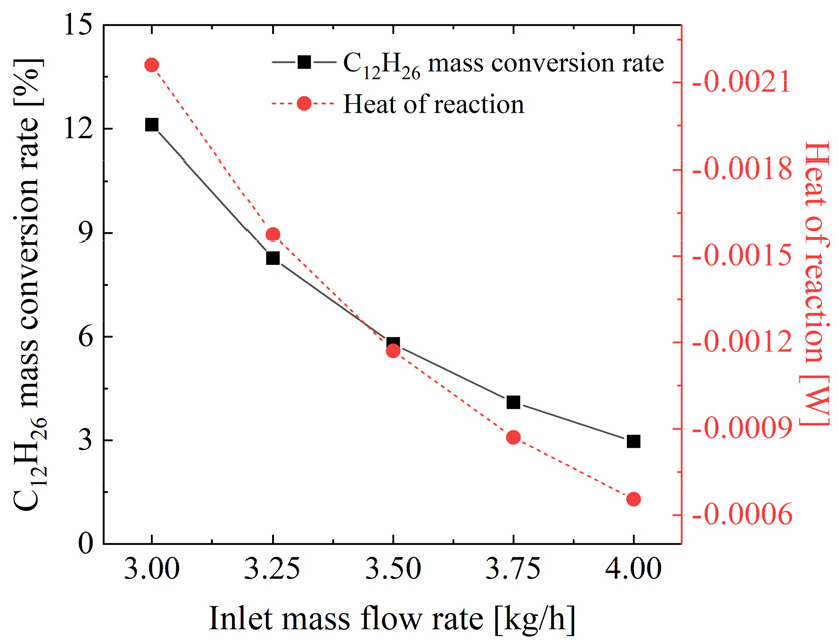
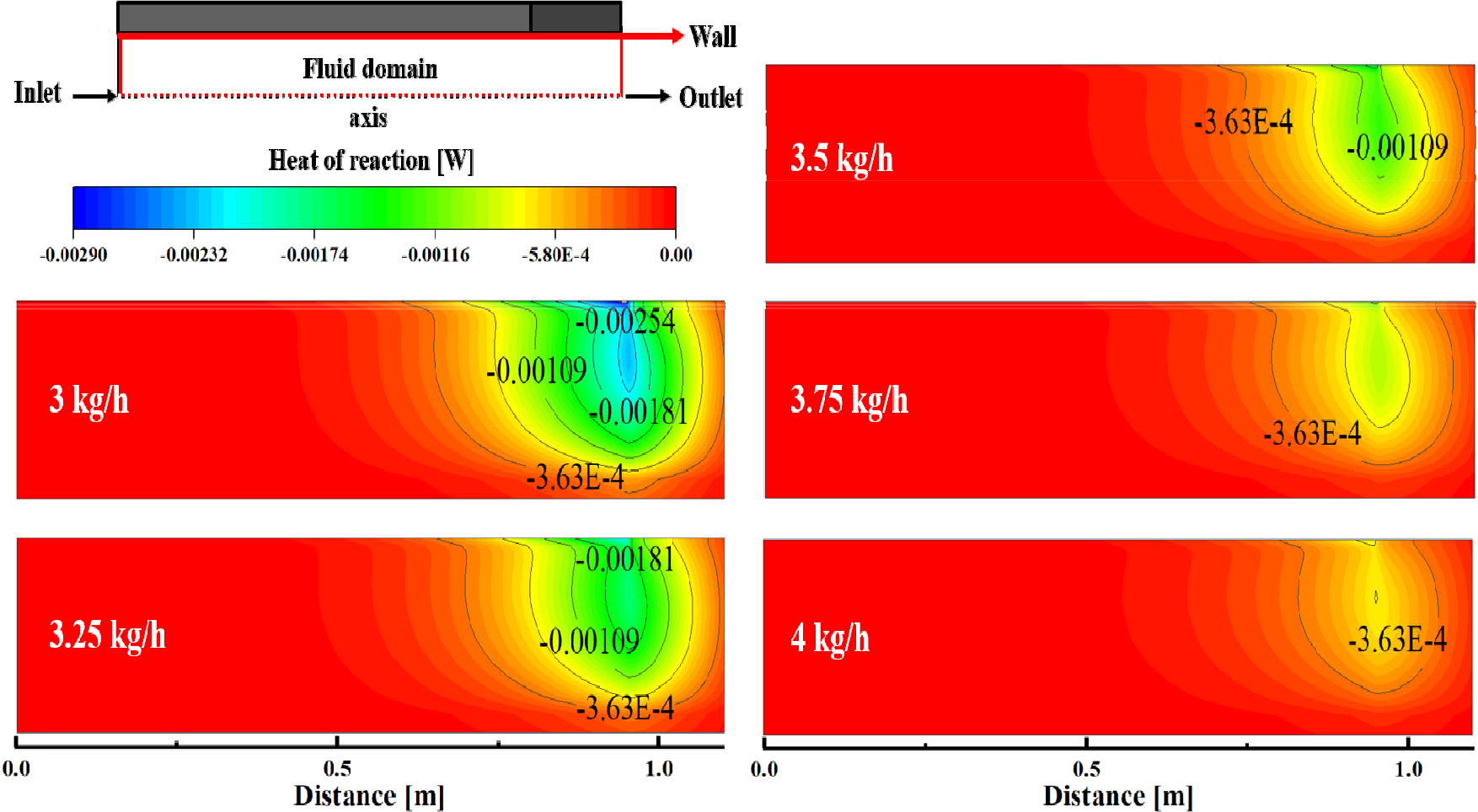
질량 유량 변화에 따른 연료의 전환율과 반응열을 Fig. 9에 나타내었다. 반응열은 흡열반응이 활발하게 나타나는 0.95 m 위치에서 면적에 대한 평균(area-weighted average) 값으로 나타내었다. 질량유량이 증가함에 따라 전환율과 반응열이 감소하는 경향이 나타났으며, 두 인자의 감소 경향성은 서로 유사하였다.
미세채널내 유체 유동 영역에서 구한 반응열 등고선을 Fig. 10에 나타내었다. 이 그림으로부터 상당한 흡열반응이 발생하는 영역을 확인할 수 있다. Fig. 7에서 언급한 n-dodecane의 전환율이 급격히 상승하는 0.5 m 이후이면서 벽면에 가까운 영역에서 흡열반응이 증가하기 시작하였다.
4. 결 론
본 연구에서는 입구에서의 연료 질량 유량 변화에 따른 원통관내 초임계 상태에서 n-dodecane의 열분해 반응을 파악하기 위해 수치해석을 수행하였다. 질량 유량의 조건은 3~4 kg/h 범위에서 0.25 kg/h 간격으로 설정하였고, 1단계 총괄 반응식인 PPD model을 적용하였다. 초임계 상태 열역학적 물성치를 예측하기 위해 REFPROP으로 예측한 데이터를 사용하였다.
미세채널내 n-dodecane의 질량 유량 증가에 따라 연료의 전환율, 흡열량과 유체 온도는 감소하였고, 반대로 유체 속도는 증가하였다. 또한, 열분해 반응에 따른 열역학적 물성치의 변화를 확인할 수 있었으며, 열분해 반응에 의해 고분자량을 갖는 연료가 분해되어 분자량이 작은 생성물이 형성되어 유체의 밀도가 크게 감소하였다.
열분해 반응 메커니즘의 유/무에 따라 유체 온도가 달라지며 동일한 질량유량과 벽면 열 조건에서 열분해 반응이 존재할 경우 유체의 온도가 더 낮아졌다.
추후 추진기관 및 연소기에 탄화수소 연료를 이용한 재생냉각 시스템을 적용하고 설계할 때, 본 연구 결과로 산출된 연료 유량에 따른 연료전환율과 흡열량 등의 결과를 사용할 수 있을 것으로 판단된다. 본 연구에서는 간단한 PPD model로 수치해석을 수행하였으나 추후 정확도 향상을 위한 분해 모델링 개선 연구를 고려할 예정이다.