1. 서 론
2. 실험 및 수치해석 방법
2.1 실험장치 및 방법
2.2 수치해석 방법
3. 결과 및 논의
3.1 SNG 예혼합화염의 안정화 선도
3.2 희박 소화경계에서 비대칭 화염 구조
3.3 희박 비대칭 화염의 소화 메커니즘
4. 결 론
1. 서 론
현재 에너지 생산의 대부분을 차지하고 있는 화석연료 고갈과 및 지구온난화 문제 해결에 대한 정책이 세계적인 이슈로 대두되면서, 발전 시스템에 적용되는 연소기는 기존의 천연가스를 비롯한 다양한 연료를 사용할 수 있는 연료 유연성(flexibility)에 대한 요구가 증가하고 있다. 합성천연가스인 SNG(synthetic natural gas) 연료는 석탄의 가스화(gasification) 공정을 통해 생성된 청정연료로 석탄의 장점인 경제성, 풍부한 매장량과 동시에 기체연료의 이점인 적은 이산화탄소 배출의 장점을 지니고 있다[1]. 이러한 SNG는 고온 열분해 과정을 통해 수소와 일산화탄소가 주성분인 합성가스(syngas)로 개질된 후 메탄화(methanation) 공정을 거쳐 기존 연소기와의 호환성을 위해 프로판(C3H8)을 혼합하여 발열량 지수인 웨버 지수(Wobbe index)를 동일하게 맞추어 생산된다. 하지만, 위 공정을 통해 생산된 SNG의 다양한 혼합물(CH4, C3H8, C2H6, H2, CO 등) 구성은 비교적 복잡한 화염 특성을 유도하기 때문에, 연료 유연성을 가진 실제 발전용 가스터빈과 산업용 연소시스템을 설계함에 있어서 이와 같은 혼합연료의 기초 연소 특성을 파악하는 연구들이 요구된다[2,3,4,5].
난류 예혼합 화염은 임의로 움직이는 층류화염 편의 앙상블로 평균 구조를 구성하게 되며, 순간적으로는 층류 화염구조로 이해가 가능하다[6]. 많은 수의 화염 편(flame let)의 존재는 화염 간의 상호작용을 불가피한 문제로 만들게 되며, 기초적인 화염의 상호작용 특성을 연구하기 위해 대향류 예혼합 화염을 이용하게 된다. 예혼합 화염의 상호작용은 상류(upstream) 또는 후류(downstream)에서 발생하는 두가지의 뚜렷한 현상으로 구분이 된다.
상류 상호작용은 두 예혼합 화염 편이 서로를 향해 전파(propagate)하고, 그들 사이에 있는 혼합기를 소모하면서 발생한다. 특히 탄화수소 연료를 사용한 화염의 상류에서 발생하는 상호작용 현상은 유효 루이스 수(effective Lewis number, 이하 Leeff)와 밀접한 관련이 있다고 보고되었다[7]. 혼합기의 반응률은 Leeff > 1 조건에서 열적 상호작용으로 발생한 초과 단열화염온도를 통해서 강화되고, Leeff < 1 경우에는 단열화염온도보다 낮은 온도를 가지게 되어 감소하게된다. 이러한 결과는 상류에서 발생하는 열적 상호작용의 중요성을 강조한다.
후류 상호작용은 두 화염 편이 서로 멀어지는 방향으로 전파하게 되며, 각 노즐에서 분출되는 혼합기를 소모하며 연소한다. 탄화수소 및 수소 연료의 희박-희박(과농-과농) 예혼합 화염 사이에 발생하는 후류 상호작용 문제에서 부족한 반응물 개념(deficient reactant concept) 루이스 수의 역할은 화염의 소멸 메커니즘을 설명하기 위해서 사용된다. 실험 및 이론적 연구로 후류에서 화염의 높은 질량 확산으로 인한 화학적 상호작용이 강할 때는 기울어진 소화경계를, 약해질 때는 직각의 소화경계가 각각 LeD가 1보다 작거나 클 때 나타난다[8,9,10]. 또한 Le < (>) 1 인 경우 신장률의 증가에 따라 화염의 온도는 증가(감소) 하고, 화염의 위치는 정체면으로부터 붙어진(띄워진) 거리에서 발생하는 특성이 있다. 나아가 대향류 예혼합화염의 후류에서 상호작용이 강해지는 경우, 약한 화염이 강한 화염의 열적 및 화학적인 공유를 통해 기생하는 생존 특성들이 나타나고, 약한 상호작용일 경우 각각 독립된 예혼합화염의 특성을 가진다.
이러한 형태로 예혼합화염의 후류 상호작용은, 선호확산 및 확산도 차이, 화염의 신장률 그리고 열 손실의 영향을 받고 있는 상류 상호작용의 직접적인 영향을 받게된다. 따라서, 열적 및 화학적 후류 상호작용을 하고있는 화염의 소화 메커니즘을 완전히 이해하기 위해서는 후류와 상류 상호작용의 관계를 고려함이 필수적이다는 것을 알 수 있다. 상류 및 하류에서 화학적 및 열적으로 상호작용하는 화염의 소화 메커니즘은 복잡한 관계 특성으로 인해 아직 명확하게 설명되지 않았다. 따라서, 본 연구에서는 상호작용하는 SNG - air 예혼합화염 사이에서 발생하는 화염의 연소반응을 파악하고 소화 특성을 이해하는 것을 목적으로 한다.
사용된 모사 SNG 연료에서 11% 수소 함량을 가진 희박 SNG-air의 반응물은 부족한 반응물 개념(deficient reactant concept)으로 루이스 수가 1보다 작은 것을 고려하였을 때, 희박조건의 화염은 강한 상호작용을 나타낼 것으로 예상된다. 또한, 희박 – 희박 비대칭 화염의 형상에서 발생하는 약한 화염(weaker flame)은 상호작용 과정에서 생존을 위해 정체면(stagnation plane, 이하 S.P)를 넘어 강한 화염(strong flame)의 영역, 다시 말해 좌표축(coordinate sense) 기준으로 음의 화염속도(negative flame speed)를 나타내게 되는데, 정체면을 기준으로 각 위치에 존재하는 양의 화염속도(positive flame speed)와 함께 각 조건의 화염 구조와 소화 거동 특성을 주요 소멸 반응식과 전도 열전달을 통해서 살펴보고자 한다. 수치해석은 3가지의 상세반응 메커니즘 중 희박 가연 한계를 가장 잘 추종하는 메커니즘을 선택하여 화염 특성을 분석하였다. 전체 신장률(global strain rate, 이하 ag)과 연료의 체적비를 이용해 도출한 안정화 선도(stability map)를 통해 전체적인 화염의 소화 거동의 특징을 설명하고, 강한 상호작용이 예상되는 관심 영역인 희박-희박한 조건에서 비대칭 화염 구조와 소화 원인을 관찰하기로 한다.
2. 실험 및 수치해석 방법
2.1 실험장치 및 방법
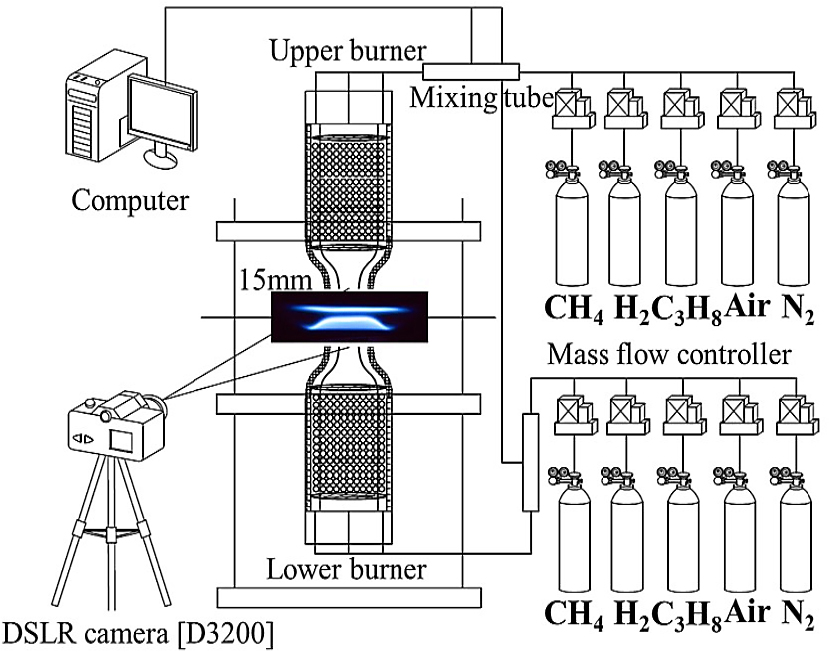
대향류 버너는 평면 화염을 정체점을 기준으로 단열 벽면을 형성함으로써 화염 간의 열 손실을 최소화하면서 화염의 거동과 구조를 이해하는 방법으로 널리 사용된다. 또한 최소 열 손실을 이용하여 화염의 기초 특성인 단열화염 온도조건에서 층류 연소속도를 쉽게 구할 수 있는 장점이 있다[11]. Fig. 1은 연구에 사용된 실험장치의 개략도이다. 각 연료는 긴 혼합튜브를 통해 충분히 혼합되도록 하였으며, 버너 출구에서 균일한 유동장 형성을 위해 노즐 상류 측에 알루미늄 볼과 메쉬층(mesh layer)을 설치한 후 수축형 노즐(contraction type nozzle)을 사용하였다. 노즐의 수축비는 0.054이고, 지름은 14 mm이며 양 노즐 간의 간격은 15 mm이다. 사용된 연료는 CH4, C3H8, H2를 각각 80, 9, 11%의 체적비의 조성비로 구성된 실험실에서 제작한 모사 SNG 가스이다. 이 경우 혼합연료의 정확한 조성비를 위해 유량은 최소 통제 가능량이 CH4의 체적비 기준으로 0.007%인 질량유량계(MFC, Accuracy ± 1% all range)를 정밀 교정기(Defender 510H, Accuracy 1%)의 검증을 통해 사용하였다. 사용된 각 가스의 순도는 99.995%이고 공기는 99.95%의 고순도 압축용 공기를 산화제로 사용하였다. 외부 유동의 교란과 과농(rich) 조건 시 발생하는 측면에서의 화염을 제거하기 위해 15 mm로 확장된 동축(coaxial) 노즐을 이용하여 예혼합기와 동일한 유량의 질소(N2)를 사용하여 커튼 유동장(curtain flow)을 형성하였으며, 버너 주위는 아크릴 쉴드(shield) 벽을 만들어 외부 유동을 통제한 후 실험을 진행하였다. 소화 거동과 관련된 실험 결과는 수치해석에 사용될 상세 반응기구(detail kinetic mechanism)를 검증하기 위하여 희박조건의 소화 경계 상에서 비교된다.
또한 상호작용하는 화염의 이미지는 DSLR(Nikon-D3200) 카메라를 이용하였으며, 동일한 조건의 화염 발광 강도를 취득하기 위하여 ISO 200, 셔터속도 1/3초로 고정한 후 F number를 조정하여 취득하였다. 취득한 직접 화염 사진은 Matlab base code[12]를 이용하여 32bit로 변환 후 0 ~ 255의 임계값을 통해 스케일링 된다. 이후 노즐 간의 간격인 15 mm를 1,008개의 픽셀(pixel)로 일정하게 나누어 최대 강도 지점을 화염대로 정의하였다. 이렇게 정의된 화염의 위치는 수치해석을 통한 화염대 위치와 비교된다.
2.2 수치해석 방법
정체면을 기준으로 1차원 상사성 모델을 적용하여 만들어진 OPPDIF 코드는 Kee [13]에 의해 개발되고, Lutz [14]에 의하여 확장되었다. 해석 방법은 에너지, 질량, 화학종, 운동량 보존식이 사용되었다. Plug-flow 속도 경계층 조건이 사용되었고, Mixture-averaged diffusivity를 이용하여 계산을 진행했다. 사용된 분위기 조건은 0.1 MPa, 298 K로 고정하였고, 노즐 간격인 15 mm에서 발생하는 복잡한 상호작용 현상을 해석하기 위해서 격자(grid)는 최소 800개 이상을 사용하였다.
사용된 지배방정식은 Transport-based [15]와 CHEMKIN- based 코드[16]를 이용하여 풀었다. 실제 화염의 복사열 손실을 모사하기 위하여 광학적으로 얇은 모델[17] 적용하였으며, CH4, CO, CO2, H2O의 특성 값을 부여하여 모사하였다. 이에 기초한 복사 열 유속 등은 다음 식 (1)으로 정의된다. 여기서 는 스테판 볼츠만 상수(Stefan-Boltzmann constant)를, KP는 화학종 i의 플랑크 흡수 계수(Plank absorption coefficient)를 나타낸다. T와 Tꝏ는 국소 및 주변 온도이고 Pi는 초기압력이다.
사용된 변수로는 전체 신장률인 ag와 혼합기 내 CH4의 체적비(ΩCH4)를 이용하여 상호작용하는 SNG-공기 화염의 안정화 선도와 화염 구조를 해석하는 데 사용하였으며, 변수들에 대한 정의는 식 (2)와 (3)과 같다. 식 (2)의 V는 위아래 노즐에서 분사되는 연소 혼합물의 축 방향 속도(axial velocity)를, X는 노즐 간의 거리로 정의되며, 하첨자 U, L은 각각 상부와 하부 노즐을 의미한다. 식 (3)에서 는 화학종의 체적비(volumetric ratio), 는 의 몰 분율(mole fraction)이며, 본 연구에 사용되는 변수 조건을 Table 1에 정리하여 나타내었다.
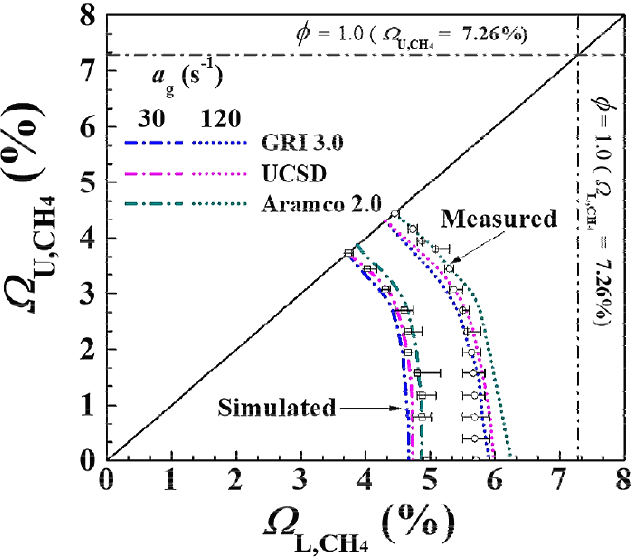
다양한 연료의 조합으로 만들어진 SNG C-11의 복합적인 특성으로 인하여 단일연료에 맞추어진 상세 반응 메커니즘을 그대로 인용하기에는 타당하지 않다. 그러므로 이중 화염 간의 상호작용을 포함한 복합 연료의 소화 거동 현상을 해석하기 위해 총 3가지의 상세반응기구를 이용하여 검증을 진행하였다. CH4 연소해석에 적합하다고 알려진 GRI 3.0[18]과 C1-C3 계열의 탄화수소반응을 포함한 UC San Diego(이하 UCSD Mech.)[19] 그리고 비교적 최근에 개발된 Aramco 2.0[20]을 사용하여 실험과 비교하여 선정하였다. 반응기구 선정을 위한 비교 실험은 신뢰도를 위해 총 7번의 반복 실험을 통해 검증하였으며 취득한 소화경계와 각 반응기구별 계산 결과와의 비교를 Fig. 2에 도시하였다.
Table 1.
Experimental and numerical condition
| Fuel (Simulated SNG) | CH4, C3H8, H2 (99.995%) |
| Composition ratio (%) | 80 : 9 : 11 |
| Oxidizer | Air (21% O2, 79% N2) |
| Distance of nozzle, X (mm) | 15 |
| Global strain rate, ag (s-1) | 30, 120, 300, 500, 650, 740 |
실험 및 수치해석 결과는 ag = 30, 120 s-1에서 희박 소화 경계를 이용하여 비교하였는데, 희박 소화 경계에서 발생하는 평균 오차율은 각각 GRI 3.0, UCSD Mech., Aramco 2.0 에서 2.88%, 2.14%, 3.51%로 나타났다. 모든 반응기구의 결과가 실험적 소화경계와 비교적 일치하였지만, 화학적 상호작용이 강해지는 조건을 나타내는 소화경계의 기울기를 평균적으로 가장 잘 모사한 UCSD Mech.이 만족스러운 결과를 나타냈다. 이러한 결과를 통해서 본 논문에서는 UCSD Mech.를 수치해석의 반응기구로 사용하였다.
3. 결과 및 논의
3.1 SNG 예혼합화염의 안정화 선도
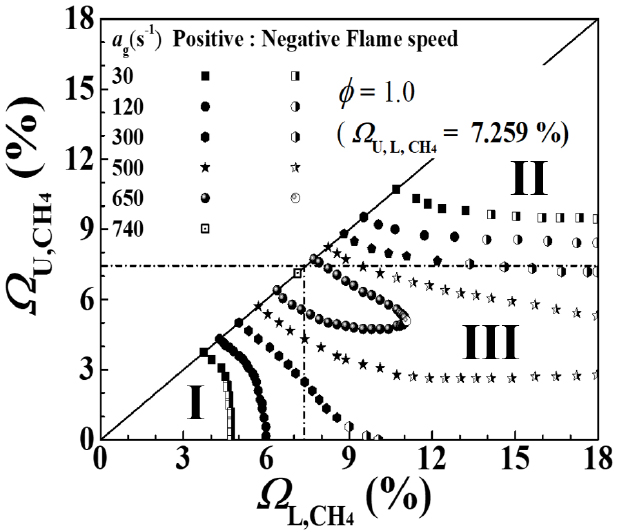
다양한 신장률(ag)과 CH4의 체적비(ΩCH4)을 이용하여 SNG 예혼합화염의 안정화 선도를 Fig.3에 나타내었다. ΩU,CH4과 ΩL,CH4은 각각 위, 아래 노즐의 해당하는 조건을 나타낸다. 실선은 화염의 강도가 동일한 대칭 화염의 조건이고, 점선은 이론당량비(stoichiometry) 조건(𝜙 = 1.0), 즉 ΩL,U,CH4 = 7.26%를 의미한다. 채워진 심볼은 좌표축을 기준으로 양의 화염속도(P.F)를 의미하고, 비워진 심볼은 음의 화염속도(N.F)를 의미한다. Fig. 3에서 도시된 화염의 안정화 선도는 3가지의 상호작용하는 화염으로 분류할 수 있다. 영역 I과 II는 ΩU,CH4 < 7.26%, ΩL,CH4 < 7.26% 과 ΩU,CH4 > 7.26%, ΩL,CH4 > 7.26% 에 해당하며 각각 상호작용하는 희박 이중 화염, 과농 이중 화염으로 분리되고, 영역 III은 ΩU,CH4 < 7.26%, ΩL,CH4 > 7.26% 으로 나누어지며, 희박 및 과농 화염에서 생성된 O2와 H2, CO 확산화염이 다른 하나의 화염과 병합된 삼중 화염에 해당한다.
화염 안정화 선도의 현상을 이해하기에 앞서, 층류 화염속도를 신장률과 부족반응물 루이스 수(LeD) 관계에 대해서 이해하여야 한다. 수소 또는 탄화수소 계열의 연료에서 자유 전파하는 예혼합화염의 층류 화염속도는 LeD < 1(> 1) 조건일 경우 신장률의 증가에 따라 증가(감소) 한다. 하지만, 이러한 개념이 상호작용하는 화염에는 적용이 되지 않는다는 것을 상기하여야한다.
이전 연구에 따르면, 상호작용하는 탄화수소 계열의 예혼합화염은 LeD < 1(> 1) 조건일 때, 기울어진(사각형) 소화 경계를 보여주며 강한(약한) 상호작용을 나타낸다고 보고되었다 더불어 ag의 증가로 좁아진 후류를 통해 전달된 CO, H, O와 OH를 통해서 LeD > 1에도 불구하고 상호작용이 발생함을 보고하였다[21,22,23,24.25].
다종 연료의 루이스 수는 이종 연료를 고려해야 하므로 유효 루이스 수(Leeff)를 이용하여 해석해야 한다. SNG 예혼합기의 체적 기준 유효 루이스 수에서 0.65 ≤ Leeff ≤ 1.16 범위를 가진다[21]. 그리고 부족반응물 개념 하, CH4는 0.96 ≤ LeD ≤ 1.0, C3H8은 1.85 ≤ LeD ≤ 1.72 그리고 H2는 0.45 ≤ LeD ≤ 0.66의 범위를 가지게 된다. 그렇다면 SNG의 안정화 선도의 이해는 희박조건일 때는 ΩL,CH4 축의 수직 선을 기준으로 기울어진 형상을, 과농조건일 때는 ΩU,CH4 축에 수직인 소화경계를 가지는 것이 옳다. ag = 30에서 300 s-1의 희박 소화경계(lean extinction boundary, LEB)에서 대칭 조건으로의 접근은 조금 더 큰 기울기를 형성한다. 상세히 관찰하자면, ag = 30 s-1에서 하나의 화염만 존재하는 경우 가연 한계는 ΩU,CH4 = 0, ΩL,CH4 = 4.23%로 나타나지만, 대칭 조건에 가까워지면 최소 가연 한계는 ΩL,U,CH4 = 3.73%로 확장된다. 나아가서, ag의 증가로 인해 후류 간격이 줄어들면서 단일화염 조건과 대칭화염 조건의 차이는 더욱더 벌어진다. 이것은 증가하는 ag에 따라 후류 상호작용이 강화되어 약한 화염이 강한 화염의 활성기 공유와 후류 영역의 열적 상호작용을 통해서 기생하고 있는 것으로 이해할 수 있고, 충분한 생존 조건을 형성함으로 인해서 신장률의 증가에 따라 N.F 조건의 화염 영역이 줄어들고 P.F 조건에 확장되는 것을 관찰할 수 있다.
비슷한 현상으로 과농 소화 경계(rich extinction boundary, REB)에서도 대칭 조건으로 접근할 때, 신장률로 인한 후류의 상호작용을 통해 기울기를 가지는 것으로 이해된다. 하지만 ag = 30 에서 300 s-1까지 기울기는 변동이 없으며, 소화 경계는 낮은 기울기를 나타내며 수축하게 된다. 이는 희박조건과 달리, 과농조건의 약한 화염은 생존을 위해 정체점을 넘어서 N.F 조건으로 존재하고, 약한 화학적 상호작용으로 인해 강한 화염으로부터 충분한 활성기를 공유받지 못하는 것을 의미한다. ag = 500 s-1 이상의 삼중 화염의 소화 경계는 매우 복잡한 상호작용을 보여주는 섬 모양의 형태 가진다. ag = 500에서 740 s-1까지 지속적으로 수축하며, 마침내 ΩL,U,CH4 = 7.12% 조건에서 최종 소화점을 가지게 된다.
앞서 논의한 것에 따르면, 자유 전파하는 화염의 층류 연소속도는 LeD < 1(> 1) 조건일 경우 ag의 증가에 따라 증가(감소)한다. 과농–과농 화염에서는 CH4, C3H8의 LeD와 Leeff가 1보다 크므로, ag의 증가에 따라 소화 경계의 수축은 충분히 이해가 된다. 그러나 희박–희박조건은 LeD와 Leeff 모두 1보다 작으므로, ag의 증가는 소화경계의 확장을 유도해야 하나, 오히려 급격한 수축을 발생시키고, 이러한 현상은 단순한 후류에서 화학적 상호작용으로는 이해되지 않고, 상류와 후류 모두에서 열 및 화학적 상호작용을 고려해야 함을 나타낸다. 따라서 화염의 소화 거동을 해석하기 위해서는 상류와 후류에서 발생하는 열 및 화학적 상호작용에 대한 상세한 조사가 필요하므로, 3.3절에서 다루도록 하겠다. 또한, 복잡한 상류 및 하류의 상호작용이 작용하는 삼중 화염의 영역(섬 모양)을 해석하기 위해서는 먼저 부족반응물 및 유효 Lewis 수 개념에서 LeD, Leeff < 1 조건, 즉 상호작용이 활발히 일어나는 희박 예혼합화염 영역에 대한 선 이해가 필수적이기 때문에, 본 연구에서는 희박 비대칭 화염의 구조 및 소화 특성을 주제로 상세히 살펴보겠다.
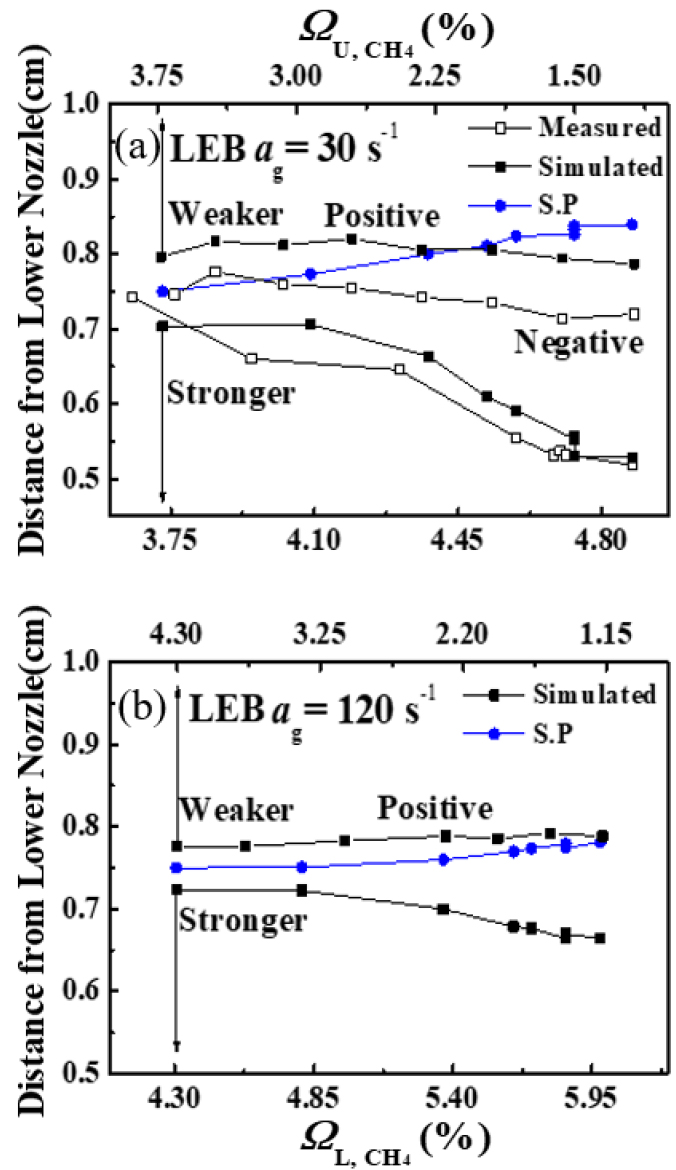
상호작용하는 화염의 구조를 살펴보기 이전에 ag = 30과 120 s-1의 LEB에서 발생하는 비대칭 화염의 위치를 Fig, 4에 나타내었다. 빈, 채워진 사각 심볼은 실험적, 수치적 화염의 위치를 의미한다. 파란색 원형 심볼은 해당 조건에서 수치적으로 취득한 정체점을 의미한다. ag = 120 s-1의 실험값은 강한 신장률로 인하여 발생한 병합 화염(merged flame)으로 화염 위치의 구분이 불가능하여 제외하였다. 실험적 화염 위치 결정에 관한 내용은 2.1절에 상세히 나와 있고, 수치적 화염 위치는 최대 열 방출(maximum heat release rate) 지점으로 정의되었다[22]. 최대 오차율은 위 화염에 대하여 약 6.5%이고, 아래 화염에 대해서 약 2.2%를 가지고 있다. Fig. 4(a, b)에서 위와 아래 화염은 각각 약한, 강한 화염을 나타낸다. ag = 30 s-1에서 실험적 결과는 화염이 N.F 조건으로 전환하는 과정이 실제로 존재한다는 것을 잘 보여준다. (a)에서 강한 화염은 소화 경계선을 따라 증가하는 전파속도로 인해 S.P를 넘지 않고, 노즐 방향으로 움직이는 것을 확인할 수 있다. 약한 화염은 강한 화염으로부터 후류를 통해 CO, H, OH, O와 같은 활성기와 열 공유를 공급받아 생존 조건을 형성한다. 화염의 강도 차가 심해짐으로 인해, 약한 화염은 생존을 위해 정체점을 넘는, N.F 조건으로 전환되고, 이러한 현상은 약한 화염이 강한 화염에 기생하는 관계로 이해할 수 있다. (b)에서는 신장률의 증가가 후류의 간격을 좁혀 더 많은 활성기 또는 열적 상호작용을 유도하므로, 약한 화염이 P.F 조건에서 생존할 수 있는 충분한 조건을 형성한다. 이처럼, 후류 상호작용하는 소화 메커니즘을 화염 구조를 통해 이해하기 위해서 3.2절에서 상세히 살펴보도록 하겠다.
3.2 희박 소화경계에서 비대칭 화염 구조
앞서 설명하였듯이, 존재할 수 없는 희박 예혼합화염의 조건에서 추가적인 생존을 가져다주는 상호작용은 소화 경계에서 기울어진 형태를 유도한다[8,9,10]. 이러한 현상들은 후류에서 CO, H, OH, O와 같은 활성기와 열의 교환으로부터 발생이 된다고 보고되었지만[21,22,23,24,25]. 추가적으로 상류와 하류 전체의 상호작용으로 발생하는 복잡한 소화 경계에 대한 이해는 분명하게 밝혀지지 않았다.
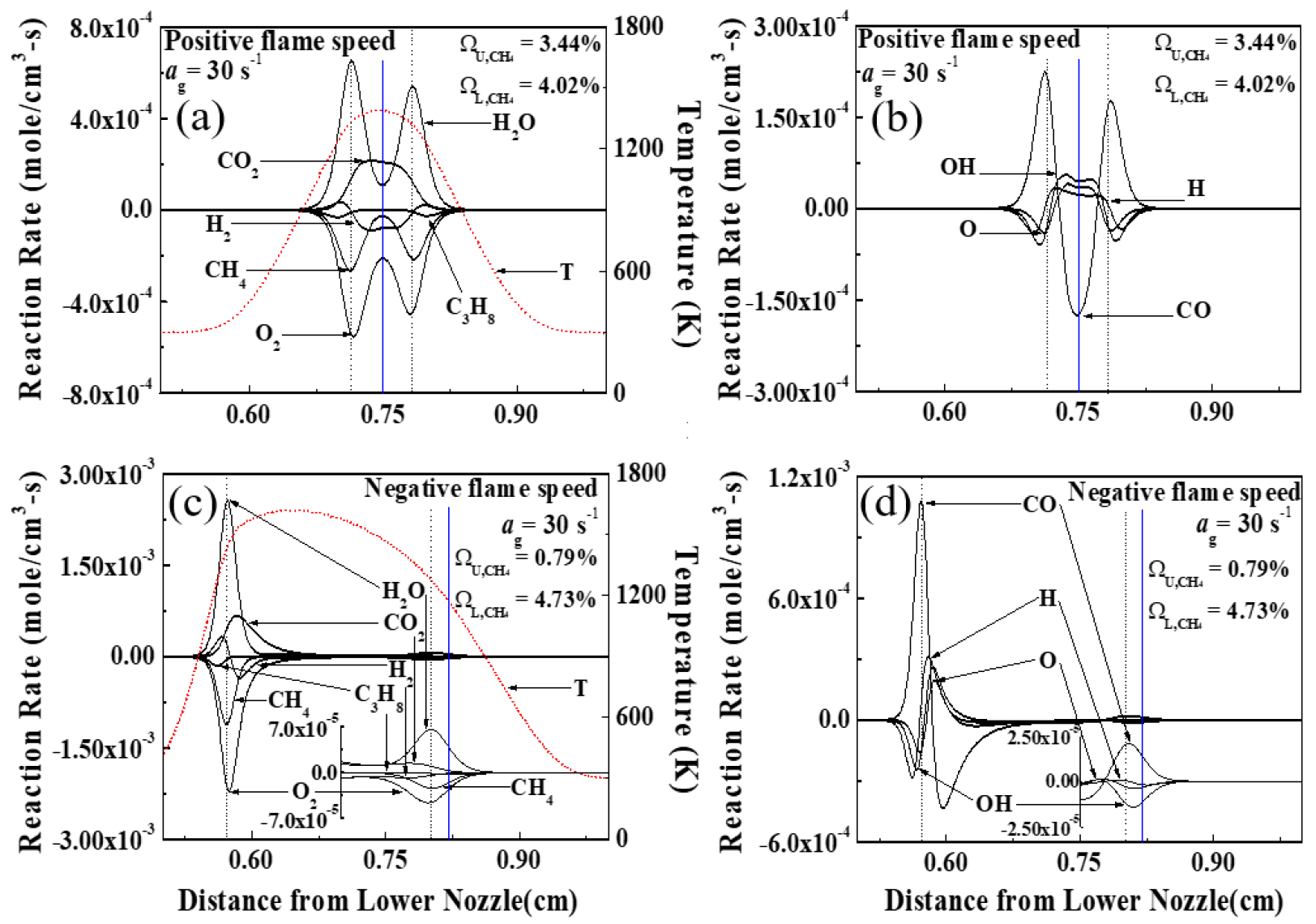
Fig. 5는 ag = 30 s-1의 LEB 조건에서 발생하는 대표적인 화염 구조를 온도와 주요 화학종 그리고 CO, H, OH, O의 생성 및 소모율에 대하여 나타냈다. (a, b)는 P.F 조건을, (c, d)는 N.F 조건에 해당한다. 세로 실선, 점선은 각각 정체점과 화염 위치를 의미한다. 내부 그래프는 후류에서 화염 간 이어진 반응을 관찰하기 위하여 삽입되었다. 화염의 강도가 다른 비대칭 화염에서 온도 프로파일은 후류에서 최대온도를 가지고, 약한 화염으로 기울어져, 후류에서도 열적 상호작용이 존재함을 암시한다. 상세한 열적 상호작용의 관찰은 3.3절에서 다루도록 하겠다.
모든 조건에서 주요 반응물인 CH4, C3H8은 상류와 화염대(flamelet)에서 대부분 소비가 된다. 하지만 O2와 H2는 화염대 이전에서 모두 소비되지 않고 후류에서 지속적인 소비율을 나타낸다. 더불어 (b)에서 발견할 수 있는 CO 또한 활발한 소비율을 보이며, 결과적으로 H2O와 CO2를 후류와 약한 화염에서 발생시킨다. 이것은 Leeff < 1 인 LEB 조건과 LeD < 1인 H2, 느린 반응을 가진 CO를 통한 강한 화학적 상호작용이 화염 간의 공유가 이루어진다는 것을 보여준다. 따라서, CH4, C3H8과 H2의 소비는 후류에 CO를 포함한 H, OH, O 활성기를 충분히 공급하여 급격한 화학적 상호작용을 형성한다. 특별히, 강한 상호작용을 하고 있는 (a)에서 H2는 후류에서 상당히 소비되어 H 활성기를 생성 후 후류에서 소비되는 것을 관찰할 수 있다. 여기서 화염의 전체 반응율의 척도는 H + O2 = O + OH, R1 반응을 통해 이해할 수 있다는 것을 알아야 한다. 이것을 토대로 H, OH 활성기는 강한 화염과 약한 화염의 기생 관계에 중요한 역할을 하는 것으로 판단된다. 약한 화염은 자생 가능한 조건이 아니지만, 충분한 활성기와 반응물을 공급받게 되고, S.P 이전에 가연 조건(flammable condition)을 형성하기 때문에 P.F 조건으로도 충분히 생존할 수 있게 된다. 반면, N.F 조건인 (c, d)는 후류에서 P.F보다 감소된 상호작용을 H2와 O2 그리고 CO와 활성기들을 통해서 확인할 수 있다. N.F 조건의 강한 화염은 더 높은 Leeff와 LeD를 가지고 있어 약한 화염으로의 활성기 공유가 줄어든 것과 강한 화염의 전파속도 상승으로 발생한 화염 간의 거리 증가가 상호작용의 역할을 감소시킨 것으로 판단된다. 여기서 약한 화염은 정체점을 넘어 생존을 위해 강한 화염에 기생하게 되고, 후류에서 열 및 화학적 상호작용 없이 약한 화염의 생존은 불가능하다는 것을 보여준다.
지금까지 후류에서 발생하는 화학적 상호작용의 중요성과 비대칭 희박 - 희박 화염의 관계에 대해서 화염 구조를 통해 알아보았다. 특징적으로 H 활성기와 CO가 화염 간의 기생 관계에 중요한 역할을 하는 것으로 나타났다. 하지만 활성기와 화학종의 소모 및 생성률은 복잡한 반응으로 기생하는 약한 화염의 소화 메커니즘을 완전히 이해하기에 어려움이 있다. 더욱이 화학적 상호작용만을 이용하여 3.1절에 언급했던 희박 - 희박 화염이 Leeff < 1 조건임에도 불구하고 신장률의 증가에 따라 소화 경계가 축소하는 현상을 설명하는 것은 불가능하다. 따라서, 3.3절에서는 기생하는 약한 화염의 화학적 상호작용을 보여주는 주요 반응과 상류 및 후류에서 발생하는 열적 상호작용을 관찰함으로써 전체 화염의 소화 거동 메커니즘을 이해하고자 한다.
3.3 희박 비대칭 화염의 소화 메커니즘
강하게 상호작용하는 희박 - 희박 화염에서, H2와 CO가 후류에서 상당히 소모되는 것을 화염 구조를 통해 확인할 수 있었다. 특히나 후류에서 이루어지는 H 활성기의 소비(생성)를 통한 상호작용으로 발현된 약한 화염의 가연 한계 확장은 이전 연구에서도 보고되었다[25]. 주요 분기 반응(main chain branching reaction)을 나타내는 H + O2 = O + OH, R1과 반대로 H + O2(+M) = HO2(+M), R10에서 발생하는 HO2 활성기는 소멸반응(chain terminating reaction)을 대표하는 활성기로 알려져 있으며, 점화 시간 지연 및 폭발한계 거동을 설명하기 위해 제안된다[26, 27]. 후류 상호작용은 CO의 느린 반응(slow reaction)에 큰 영향을 받는다[28]. Fig. 5(b, d)에서 보이는 것처럼 CO는 OH와 결합하여 CO + OH = CO2 + H, R26에 의해 완전 반응을 진행한다. 따라서, R10과 R26은 상호작용으로 생존하는 약한 화염의 소화 거동을 설명하기에 적절한 것으로 판단되어 Fig. 6을 통해 살펴보겠다.
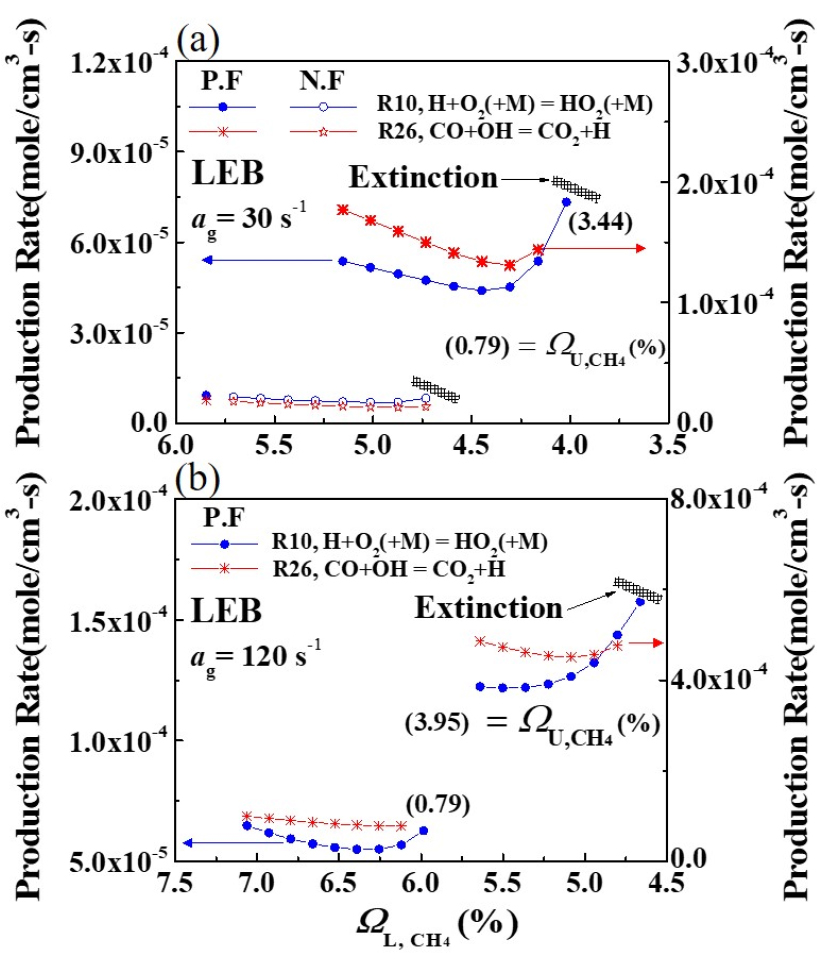
강한 화염으로부터 전달받는 화학적 상호작용의 정도를 조절하기 위해 고정된 ΩU,CH4에 대하여 ΩL,CH4를 소화 지점까지 감소시켰다. ag = 30, 120 s-1에서 발생하는 LEB 상에서 대칭(ΩU,CH4 = ΩL,CH4)과 단일 화염(ΩU,CH4 = 0.00%) 조건 직전에 해당하는 소화 지점(ΩU,CH4 = 0.79%)을 이용하였다. 이때 약한 화염에 해당하는 온도가 ag = 30 s-1의 P.F, NF 조건에서 각각 1,380K에서 1,320K로, 1,306K에서 1,290K로 단순 감소하며, 약한 화염의 강도가 점차 약화되고있는 현상을 보여준다. 이러한 현상은 ag = 120 s-1의 조건에서도 동일하게 발생하였다.
화염 구조를 통해 확인된 화학적 상호작용이 강하게 일어났던 P.F 조건에서 R10이 ΩL,CH4의 감소와 함께 줄어드는 반응률을 보이다, 소화 직전에 급격하게 상승하는 현상이 Fig. 6(a, b)에서 관찰되었다. 이를 통해 화염의 소화 과정 시 두드러지는 현상이 R10을 통해서 잘 나타나는 것으로 확인된다. R10에서 생성된 HO2는 H와 결합하여 새로운 O, OH 활성기로 대체된다[29]. 따라서 CO는 추가적으로 생성된 OH 활성기와 추가적인 반응을 하며 소화 경계 확장에 영향을 미치는 것으로 이해가 되므로 반응 R26 또한 소화 직전 역전된 기울기를 나타낸다. 반면 N.F 조건(ΩU,CH4 = 0.79%)의 경우는 P.F 조건과 같은 거동을 나타내지 않는데, 이것은 온전히 하나의 화염만으로 생존할 수 있는 조건이 아닌 약한 화염이 강한 화염으로부터의 열적 공유에 완전히 의존하여 생존하고 있다는 것을 의미한다. 위 현상은 화염 간의 열전도를 통해 자세히 설명된다.
또 하나의 특이한 점은, 미미한 상호작용을 나타내는 N.F 조건(ΩU,CH4 = 0.79%)에서 약한 화염은 증가하는 ΩL,CH4에 따라 P.F 조건으로 전환되는 현상이 발생한다. 약한 화염이 후류 상호작용을 통해 정체점 이전에 가연 조건(flammable condition)을 형성하기 때문으로 판단된다. 이것을 토대로 기생하는 약한 화염의 생존방식이 후류 열 및 화학적 상호작용이라는 것과 약한 화염이 기생적 생존을 위해 정체점을 넘어가는 것을 분명히 이해할 수 있다. 나아가 (b)에서 증가된 신장률(ag = 120 s-1)은 후류 영역을 좁게 만들어 상호작용을 증가시키는데, ΩU,CH4 = 3.44, 0.79% 두 조건에서 나타나는 R10 반응의 곡선 형태를 통해서 직관적으로 확인할 수 있다. 따라서, 후류에서 강한 화학적 상호작용을 유도하는 H 활성기의 R10 반응이 R26의 CO 완전 반응에 긍정적 영향을 미치며, LEB 소화경계의 기울기 형성 및 확장에 중요한 역할을 하는 것으로 판단할 수 있다.
지금까지, 후류에서 발생하는 화학적 상호작용의 거동을 통해 소화 경계에서 발생하는 P.F와 N.F의 기울기 차이와 P.F에서 가연 한계 확장을 설명할 수 있었다. 그러나, 앞서 설명한 것처럼 신장률의 증가에 따라 전파속도가 증가하는 Leeff < 1 조건임에도 불구하고, 증가하는 신장률에 따른 LEB의 축소 원인은 분명하게 밝혀지지 않았다.
Fig. 5(a, c)의 온도 분포를 주의 깊게 살펴보았을 때, 최대온도로부터 약한 화염은 기울어진 형태를 가지며, 약한 화염으로부터 미연 온도(298K)까지 역시 음의 기울기를 가졌다. 이것으로 미루어 보아, 각 화염의 입장에서 최대화염 온도와 미연가스 온도(상류)로의 열 전달(heat transfer)은 소화 거동을 살펴볼 수 있는 물리적 인자로 제기될 수 있다.
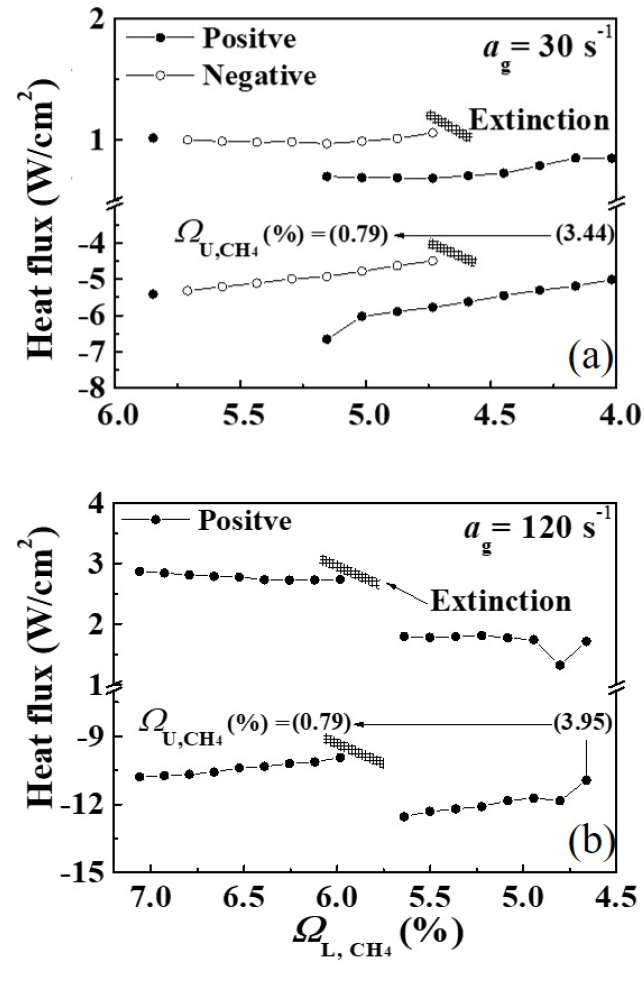
희박 – 희박 비대칭 예혼합 화염의 전체 소화 과정을 살펴보기에 앞서, 강한 화염에 기생하는 약한 화염의 열적 상호작용 거동을 살펴보기 위해, Fig. 6과 동일한 방법으로, ag = 30, 120 s-1과 ΩU,CH4 = 3.44%와 0.79% 조건에서 약한 화염의 강도를 고정하고, 강한 화염을 감소시켜 소화 거동을 관찰하였다. 여기서 Positive와 Negative는 각각 양(P.F) 및 음(N.F)의 화염속도를 나타낸다. Fig. 7(a)의 약한 화염은 N.F 조건(ΩU,CH4 = 0.79%)이 P.F 조건(ΩU,CH4 = 3.44%) 보다 많은(적은) 열 이득(손실)을 보이는 것으로 확인된다. 이것은 LEB 형성을 위해서 약한 화염은 더욱 강한 상대 화염을 요구하면서 열적 기생에 의존하는 것으로 이해된다. 최대온도의 증가로 열 이득은 증가하기 때문이다. 반면 P.F 조건의 약한 화염은 후류에서 화학적 상호작용으로 인해 비교적 낮은 상대 화염의 강도를 요구하기 때문에, 적은 열 이득임에도 생존할 수 있다. 하지만 강한 화학적 상호작용을 하고 있음에도 불구하고, 열 손실이 P.F 조건(ΩU,CH4 = 3.44%)에서 가장 크게 발생하기 때문에 마침내 소화하는 것을 알 수 있다. 신장률이 증가한 (b)에서는 후류에서의 상호작용을 통해 열 이득이 증가하지만, 상류로의 열 손실에 약 20%에 머무르게 되며, 결국 약한 화염은 소화 거동을 일으키는 것으로 판단된다.
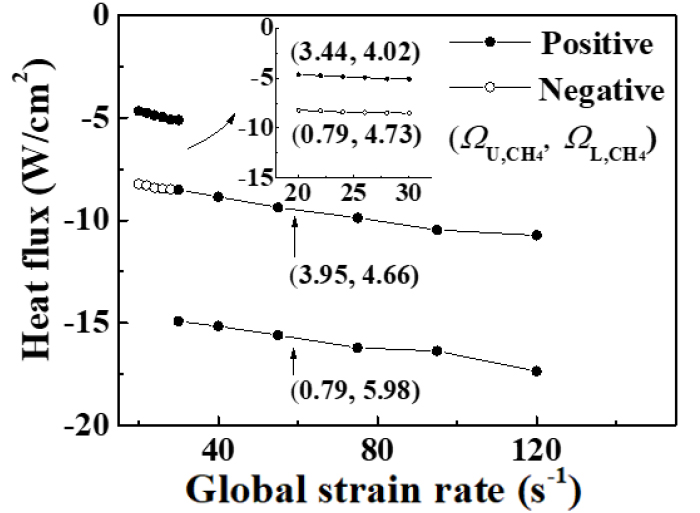
전체 상호작용하는 화염의 최종 소화는 강한 화염의 소화 후에 이루어지므로, 강한 화염의 입장에서 전도 열 손실(conductive heat loss)에 관해 조사하는 것이 필수적이다. 따라서 Fig. 8에서 소화 지점까지의 신장률 증가에 따른 열 손실을 도시하였다. ag = 30 s-1의 소화 조건을 나타내는 (ΩL,CH4, ΩU,CH4) = (3.44, 4.02), (0.79, 4.73)과 120 s-1의 소화 조건(3.95, 4.66), (0.79, 5.98) 모두 양과 음의 화염속도에 무관하게 신장률의 증가에 따라 급격한 열 손실 증가를 보여준다. 나아가 ag = 30 s-1과 비교해 120 s-1의 열 손실은 상당히 크게 작용하며, 이를 통해 신장률 증가가 상류로의 추가적인 열적 상호작용을 유발하여 가연 영역(flammable region)을 급격하게 줄이는 것으로 이해할 수 있다. 따라서, 상류와 후류에서 열 및 화학적 상호작용하고 있는 비대칭 희박 - 희박 화염의 모든 소화는 결국 상류로의 열 손실로 이루어지며, 전도 열 이득(손실)을 통해서 전체적인 소화 메커니즘의 원인을 분명하게 할 수 있었다.
이후 추가 연구에서 과농 – 과농 화염 및 희박 – 과농 화염의 섬 모양 소화 경계 내 복잡한 상호작용을 하는 삼중 화염의 구조 및 소화 특성을 살펴봄으로써, SNG – air 대향류 연소기에서 발생하는 전체 화염의 소화 메커니즘을 보고할 예정이다.
4. 결 론
대향류 연소기에서 상류 및 후류 상호작용하는 SNG (80% CH4 + 9% C3H8 + 11% H2) - air 희박 예혼합화염의 소화 거동을 관찰하기 위해 실험 및 수치해석이 수행되었고, 다음과 같은 결론을 도출하였다.
1) 상호작용하는 SNG 희박 예혼합화염의 소화 경계(extinction boundary)에서 실험을 통해 상호작용 현상을 설명하기 위해 적절한 상세 화학 반응기구를 선정하였으며, UCSD Mech. 이 2.14%의 가장 적은 오차율을 보이며 소화 경계를 만족스럽게 묘사하였다.
2) 화염의 안정화 선도는 각각 희박(과농) - 희박(과농) 조건에서는 이중 화염을, 희박 – 과농 조건에서는 확산화염을 포함한 삼중 화염을 나타냈다. 신장률(ag)의 증가에 따라 Leeff < 1( > 1) 조건에 따라 소화 경계를 기울어진(직각의) 형태로 유도했다. 나아가서 희박(과농) - 희박(과농) 조건의 소화 경계를 수축시켰으며, 삼중 화염의 생존 영역(섬 모양)의 감소를 통해 최종적으로 하나의 소화 점을 보여줬다.
3) 희박 – 희박 예혼합화염의 후류 상호작용에서 상류와 화염대에서 소비되는 CH4, C3H8와 달리 H2는 후류에서 약한 화염까지 강하게 소모되는 것을 확인할 수 있었다. Leeff < 1 조건의 희박 예혼합화염은 후류에서 발생한 CO와 H, OH, O 활성기를 통해서 화학적 상호작용을 하는 것으로 판단된다. 이때 정체점 이전에 충분한 가연 조건을 형성하지 못한 약한 화염은 좌표 축 기준으로 음의 화염속도(negative flame speed)로 전환되며, 강한 화염에 완전히 기생하는 형태를 보인다.
4) 소화 거동 시 발현되는 H + O2(+M) = HO2(+M), R10 와 화염 구조에서 넓게 분포된 CO2의 원천반응인 CO + OH = CO2 + H, R26 반응을 통해서 소화 거동을 관찰하였다. 상호작용이 강한 P.F 조건의 약한 화염에서 소화 거동 시 기울기가 역전되는 곡선의 형태를 나타내며 일반적인 화염의 소화 거동을 보여주었지만, N.F 조건의 약한 화염은 강한 화염에 온전히 의존하는 형태로 소화하는 것을 확인했다. 나아가, 강한 화염의 추가적인 강도는 정체점 이전에 가연 조건을 형성하여 약한 화염을 P.F 조건으로 전환하였다. 이것을 토대로 후류에서 발생하는 화학적 상호작용은 약한 화염이 P.F 조건 유지에 도움을 주는 것으로 확인되었다.
5) 화학적 상호작용으로 P.F 조건의 약한 화염은 상대적으로 낮은 상대 화염의 강도를 요구하므로, 적은 열전도를 나타내지만, N.F 조건에서 약한 화염은 강한 화염으로부터 상당한 열적 지탱이 필요하기에 상당한 열전도를 보여준다. 하지만 두 가지 조건 모두 최대온도로부터 얻어지는 열 이득과 비교하여, 강한 화염이 상류로 전달하는 열 손실이 훨씬 크게 작용하면서 소화한다. 이때 상류로의 열 손실은 신장률의 증가와 같이 증가하므로, 최종적으로 상호작용하는 비대칭 희박 - 희박 예혼합화염의 소화 거동은 상류로의 열적 상호작용으로 비롯되는 것으로 판단된다.