1. 서 론
2. 실험 장치 및 방법
2.1 샘플 준비
2.2 TGA 실험 조건 및 방법
2.3 TMA 실험 조건 및 방법
2.4 연소 특성 지수
2.5 Kinetic method
2.6 회성분 분석 및 평가
3. 실험 결과
3.1 물성 분석
3.2 TGA 열중량 분석
3.3 연소 kinetic 분석
3.4 회 점착 및 용융 분석 결과
4. 결 론
1. 서 론
석탄을 생산하는 과정에서 굴진 또는 선탄 작업 후 폐기물로써 석탄 폐석(Coal Gangue)이 발생된다. 석탄 폐석은 탄소 함량과 발열량이 낮으며 회분 함량이 높은 특징을 가지고 있다. 국내에서 발생하는 석탄 폐석은 매년 7백만 톤으로 연간 석탄 채탄량의 18~30% 정도를 차지하고 있다[1], [2]. 적치된 폐석은 자연발화로 인해 유해 물질을 배출하며 또한, 풍화작용에 의한 미세 먼지도 발생시킬 수 있다. 폐석을 매립할 경우에는 토양과 수질 오염을 유발할 수 있으므로 석탄 폐석은 산업계 고형 폐기물 중 하나로 볼 수 있다[3], [4], [5].
석탄 폐석에 의해 발생할 수 있는 탄광 및 주변 환경의 오염 문제를 해결하기 위해 여러 분야에 걸쳐 석탄 폐석을 활용할 수 있는 방법을 소개하였다. 석탄 폐석은 주로 농업 및 건축 분야에서 사용되며 특정 금속 물질을 추출하기 위해서도 사용된다[6]. 또한, 연료로 활용되기도 하는데 석탄 폐석은 석탄의 30% 정도의 발열량을 가진 낮은 등급의 연료이다. 최근 중국, 인도와 베트남 등 개발도상국의 경제 발전으로 인해 석탄 수요가 증가함에 따라 발전용 역청탄의 가격이 증가한 반면, 폐석은 발전용으로 사용되는 역청탄보다 훨씬 낮은 가격으로 인해 해외에서 발전 연료로 사용하는 사례가 점차 증가하고 있다. 특히, 중국에서는 저등급 석탄을 사용하는 순환유동층(Circulating Fluidized Bed, CFB) 발전소에서 석탄 폐석을 연료로 사용한다[7], [8], [9]. CFB 보일러는 높은 연소 효율과 낮은 오염물질 배출로 청정 연소 기술로 주목받고 있다. 또한 다양한 연료를 사용할 수 있으므로 저등급 석탄, 바이오매스, 산업폐기물뿐만 아니라 폐석까지 연료로 사용할 수 있다[10]. Yi 등이 발표한 연구에서 40 t/h CFB 보일러에서는 연간 33만 톤, 발열량 999.86~1,229.82 kcal/kg 범위에 있는 저 발열량 석탄 폐석을 사용하였다. 보일러 정상 운전 시, 열효율이 80.05%에 도달하고 NOX 배출량 저감도 달성하였다[11]. Zhang 등의 연구는 130 t/h CFB 보일러에서 석탄 폐석을 45%(13,145 kg/h)로 혼소했을 때 석탄 사용량은 연간 7,103 kg/h 정도 감소하며 연간(6,000 h 운전) 약 5.5억 원 정도의 원탄 구매비용이 감소함을 보도하였다[12]. 이런 장점을 가지는 석탄 폐석을 연료로 활용하는 CFB 보일러는 50 MW, 135 MW, 300 MW까지 확대되었으며 현재 건설 중인 660 MW 초초 임계 CFB 보일러도 석탄 폐석 혼소율이 35%로 사용하고 있다[7], [13]. 따라서 석탄 폐석을 연료로 사용할 경우 환경오염 문제를 감소시킬 수 있을 뿐만 아니라 연료 비용 절감을 통해 경제적 이익을 창출할 수 있다.
국내외에서 고체 연료에 대하여 열중량분석기(Thermo- gravimetric Analysis, TGA)를 이용한 연소 kinetics 특성에 관한 연구는 많이 이루어졌다. 그러나 석탄 폐석에 대해서는 연구가 부족한 실정이며 특히, 국내에서 생산된 미활용 석탄 폐석에 대한 연소 특성, kinetics 특성에 관련된 연구는 전무하기 때문에 국내 석탄 폐석을 연료로 활용하려면 우선적으로 연소 특성에 대해 연구할 필요가 있다. 일반적으로 고체 연료의 kinetics 분석방법은 Model-fitting법과 Model-free법으로 나눌 수 있다. Model-fitting법은 단일한 승온율에서 반응차수에 따라 평균 활성화 에너지와 빈도인자를 구할 수 있는 장점을 가지는데 전체 반응의 평균활성화 에너지만 구할 수 있어서 정확성이 다소 부족한 경향을 보인다[12]. 한편, Model-free법은 반응 메커니즘에 의존하지 않고, 여러 승온 속도에 통해 임의의 전환율에 따라 활성화 에너지를 구할 수 있고 반응과정에서 활성화 에너지의 변화 추세도 도출할 수 있는 장점이 있다[14]. 그러나 반응모델 함수를 고려하지 않아서 반응차수 및 빈도인자 등 동역학 변수를 도출하기 어려운 점이 있다[15]. 석탄 폐석의 kinetics 특성에 관한 Fanrui Meng 등의 연구에서는 석탄 폐석의 연소 반응은 복잡한 과정이며 반응의 활성화 에너지는 반응 진행에 따라 변화된다고 밝혔다[16]. 그래서 본 연구에서 Model-free법과 Model-fitting법을 동시 적용한 석탄 폐석에 정확한 활성화 에너지와 빈도인자를 도출하여 석탄 폐석의 연소 동특성을 연구하고자 한다.
또한, 고체 연료는 여러 광물질을 함유하고 있으며 광물질의 특성에 따라서 연료로 사용할 때 설비 운전에 영향을 미칠 수도 있다. 특히, 고급 탄보다 저등급 탄은 광물 구성 중 Na, Cl 및 S와 같은 무기 광물질의 함량이 상대적으로 높게 나타난다. 석탄 연소과정에서 최종적으로 생산되는 회분은 노내 유동에 따라 회 융점보다 높은 영역에서 용융되어 부착되며 슬래깅(Slagging)을 형성한다[17]. 슬래깅은 보일러의 전열면에 부착되었을 때 열전달 효율의 감소로 인해 튜브 온도를 증가시킬 수 있다. 이는 튜브를 부식시키거나 막히게 만들어 파손을 일으키는 원인 중 하나이다. 슬래깅으로 발생한 거대 회분 응집물이 보일러 하부로 낙하하게 되면 보일러 운전 안전 문제를 발생할 수도 있다[18]. 그리고 회분이 과열기 및 재열기 등 상대적으로 온도가 낮은 전열면에 응축 및 부착되어 파울링(Fouling)이라는 현상을 발생할 수 있다. 저등급 탄을 사용할 때 파울링 경향이 증가할 수 있으며 특히, Na 함량이 높을수록 이러한 문제가 더 유발될 수도 있다[17]. 석탄 폐석은 저등급 고체 연료이며 회분의 함량이 매우 높다. 결국 이러한 현상을 예방하고 대응하기 위해 보일러 내에서 사용되는 고체 연료의 회 용융 특성, 슬래깅, 파울링 등의 현상을 분석하기 위한 연구가 필수적으로 요구된다. 그러나 석탄 폐석의 회 용융 특성 연구 및 점착성 연구 또한 부족하기 때문에 고 회분 석탄 폐석의 회 용융 특성을 연구할 필요가 있다[19].
따라서, 본 연구에서는 TGA를 이용하여 Model-free 법인 Ozawa-Flynn Wall method(OFW)과 Model-fitting 법인 Coats-Redfern method(C-R)을 통해 국내 미활용 연료인 석탄 폐석의 열분해 과정과 연소 특성을 분석하였다. 그리고 Thermo-mechanical Analysis(TMA)를 이용하여 석탄 폐석의 회 용융 특성을 분석하고 물성 분석을 통해 회 점착성을 예측하였다. 그리고 발전소에서 사용하고 있는 기존 석탄과 비교하여 석탄 폐석의 연료로서의 활용 가능성을 확인하고자 하였다.
2. 실험 장치 및 방법
2.1 샘플 준비
본 연구는 한국 강원도에서 생산된 석탄 폐석 GJ(굴진)와 ST(선탄)를 사용하였으며 비교 대상으로 현재 순환유동층보일러 발전소에서 사용 중인 석탄 K(Kideco)를 선정하였다.
샘플의 열중량 분석은 TGA를 사용하였고 회 용융 특성 분석은 TMA를 사용하였다. 그리고 ASTM(American Society for Testing and Materials)의 석탄 분석법에 의해 Thermogravimetric analysis 장비(TGA701, LECO Co.)를 사용하여 공업분석을 진행하였다. 원소분석은 상용 원소분석 장치를 사용하여 진행하였다. 물성 분석 결과는 Table 1, Table 2에서 확인할 수 있다.
Table 1.
Properties of GJ, ST and K
Table 2.
Chemical compositions of GJ, ST and K
그리고 각 샘플은 분쇄한 후에 체(Sieve)를 이용하여 입경 75~90 µm로 준비하였다. TMA 실험 전 회를 제작하였다. 75~90 µm 입경인 샘플을 산소 조건에서 승온 속도 10 °C/min으로 800°C까지 가열하여 회분 무게가 더 이상 변화가 없을 때까지 800°C로 유지하여 회를 제조하였다.
2.2 TGA 실험 조건 및 방법
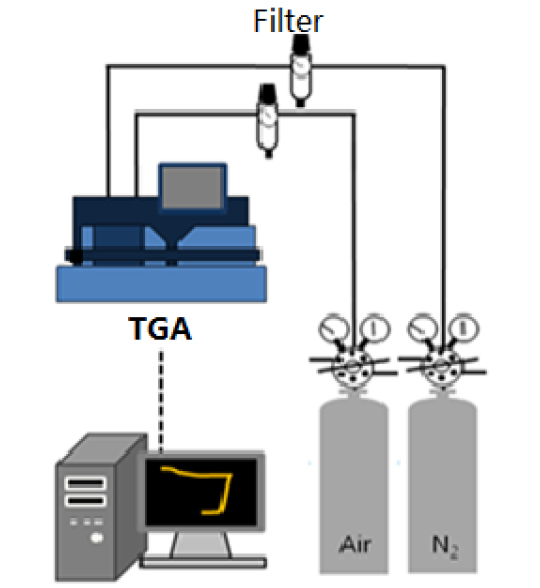
TGA 실험은 상용 실험 장비인 TGA-SDT Q600을 사용하여 진행하였다. Micro balance가 장착되어 있으며 열에 의한 물리적 및 화학적 반응이 발생한다. 시간과 온도의 변화에 따라 샘플 무게의 변화를 측정할 수 있다. 장비 개략도는 Fig. 1에서 보여주고 있다. TGA 실험 조건은 Air 분위기(N2 79% vol., O2 21% vol.)으로 100 ml/min의 유량을 공급하였고 샘플은 1회당 15(±0.1)mg을 사용하였다. 또한 승온 속도는 20, 30, 40°C/min으로 상온에서 1,000°C까지 가열하였다. 실험 결과의 정확성을 위해 각 실험을 최소 3회 이상 진행하였고 매우 유사한 결과를 얻었다.
2.3 TMA 실험 조건 및 방법
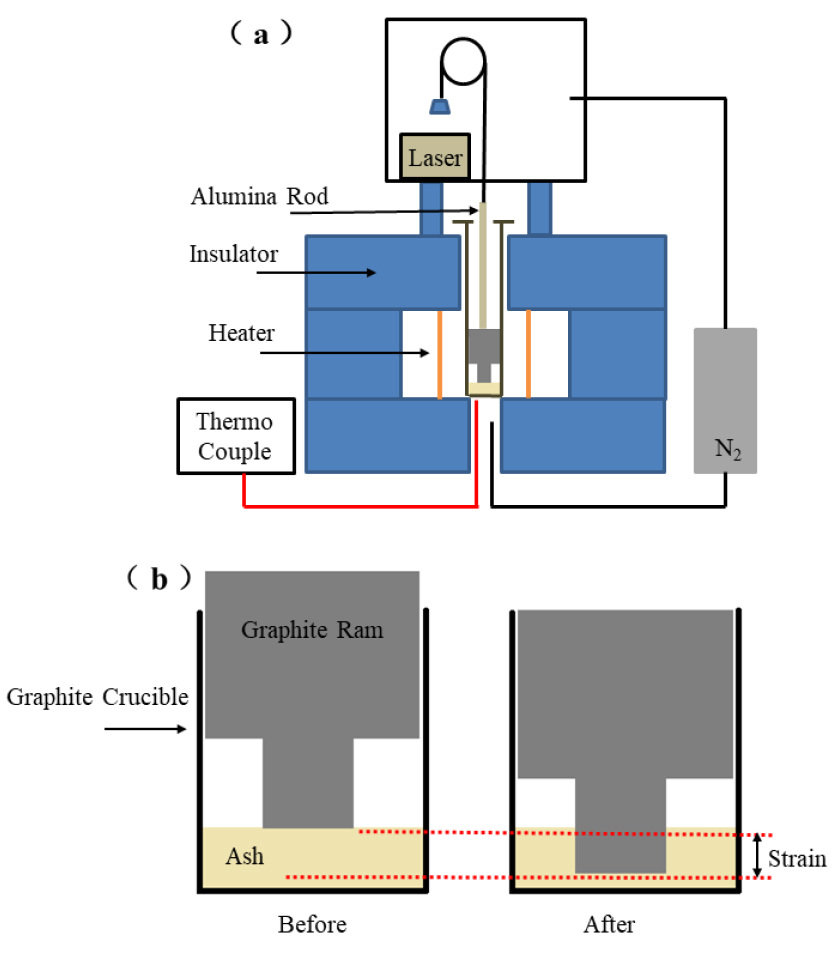
TMA 개략도는 Fig. 2(a)에서 나타내었고, Fig. 2(b)에서는 회의 용융 과정을 보여주고 있다. 회를 제조하여 200± 0.1 mg을 흑연 도가니에 넣어, Graphite ram과 회가 동일한 면적에 접촉하기 위하여 Tapping을 하였다. Ram을 일정 하중 하에서 샘플 위에 위치시킨 후, 노(Furnace) 내부에 넣는다. 준비된 회분 샘플은 질소 분위기에서 50°C/ min으로 600°C까지 12분간 급속으로 가열하였다. 600°C 까지 가열한 후 5°C/min으로 1,600°C 까지 가열하였다. Fig. 2(b)에서 확인할 수 있듯이 회가 용융되면서 Ram이 아래로 낙하하고, Ram과 도가니의 빈 공간에서 용융된 회분이 차지하게 된다. Ram이 가라앉은 변위는 레이저 변위계를 통하여 측정할 수 있다. 측정된 변위를 수축률(% Shrinkage)로 변환한 후 온도에 따른 수축률 그래프로 회 용융 특성을 분석할 수 있다. 측정된 결과 중에 용융 특성을 나타내는 온도 TX%(T25%, T50%, T75%, T90%) 있다. TX%는 회의 용융 정도가 X%에 도달하였을 때 온도를 나타낸다[18].
2.4 연소 특성 지수
연소 특성 지수(Combustion Characteristic Index, S)가 석탄 등 고체 연료의 연소성을 예측할 수 있으며 식 (1)으로 정의를 나타내었다[20]. S는 연료의 착화 성능, 연소 성능, 연소 완성도를 반영하여 클수록 연소성능을 더 좋은 것을 의미한다. TGA의 미분 값으로 DTG(Derivative- thermo Gravimetry)곡선을 통하여 DTGmax(최대 연소 반응율), DTGmean(평균 연소 반응율). Tign(착화 온도) 및 Tb(연소 종료온도)을 도출할 수 있으며 이를 통해 연소 특성지수를 구할 수 있다.
2.5 Kinetic method
일정한 온도에서 전환율을 식 (2)으로 표현할 수 있다[16].
K는 반응 속도상수이고 는 반응물의 농도함수로서 로 표현할 수 있다. t는 시간이고 α는 전환율이며 식 (3)으로 표현할 수 있다.
는 각각 초기 무게, 시간 t일 때 무게, 그리고 최종 무게를 의미한다.
Arrhenius 법칙에 의하여 식 (4)을 나타낼 수 있다. T는 온도(K)이며 A는 pre-exponential factor, R는 기체상수(8.314 J/(mol∙K))로 가정하여 계산하였다. 는 활성화 에너지(kJ/mol)이다. 승온 속도는 식 (5)같이 정의할 수 있다.
식 (2), (3), (4), (5)을 정리하여, 식 (6)을 도출하였다.
을 x로 가정하여 정리하면 식 (8)으로 표현할 수 있다.
를 Coats-Redfern method(C-R법)에 의해 정리하면 식 (9)과 같다[22]. 와 그래프를 나타내어 linear curve fitting을 통해 활성화 에너지를 구할 수 있다. 기울기는 , 절편은 이다.
OFW method는 여러 승온 속도 조건에서 전환율에 따른 온도를 측정하여 활성화 에너지를 도출하는 방법이다. OFW method는 식 (10)과 같이 표현할 수 있다. 는 상수이기 때문에 승온 속도에 따른 영향을 받지 않으므로 와 그래프를 통해 활성화 에너지를 구할 수 있다[21], [23], [24].
2.6 회성분 분석 및 평가
회 성분은 산성 성분(SiO2, Al2O3, TiO2)과 알칼리성 성분(Fe2O3, CaO, MgO, Na2O, K2O)으로 구분할 수 있다[18]. 알칼리성 성분은 주로 용융점이 낮은 성분이고 함량이 많을수록 회분의 용융점이 낮아지고 반대로 산성 성분은 용융점이 높은 성분을 포함하여 많을수록 용융점도 높아진다. 또한 공업분석 결과를 바탕으로 샘플의 회 점착 경향을 예측하고자 한다. 성능 지표(index)를 통해 석탄 폐석을 보일러 내부에서 연소했을 때 보일러 내부와 튜브 표면에 슬래깅과 파울링 상황을 예측할 수 있다[25]. 여기서 석탄 폐석을 연료로 쓰일 때 회 점착성을 분석하기 위해 세 가지 지수인 Base-acid ratio, Sulfur slagging factor, Fouling index를 도입하였다[19], [25], [26], [27].
Base-acid ratio(B/A ratio)는 알칼리성 성분과 산성 성분의 비로써 알칼리성 성분의 비중이 작으면 Base-acid ratio의 값이 작아 용융점이 높다. 이는 식 (11)으로 정의할 수 있다.
Sulfur slagging factor는 식 (12)으로 표현할 수 있다. 는 회분 중에 황 함량이며 이는 용융점을 낮추는 효과가 있는데 회분 중에 황분이 많을수록 슬래깅이 많이 발생한다.
는 파울링에 대한 영향을 미치며 가 많을수록 파울링이 많이 발생할 것이라 예측할 수 있다. 이에 따라 파울링 지수는 식 (13)과 같이 B/A ratio와 연료 중 의 함량으로 도출할 수 있다.
회 성분을 통해 슬래깅과 파울링 평가 기준은 Table 3에 나타내었다[19], [25], [26], [27].
3. 실험 결과
3.1 물성 분석
Table 1, Table 2에서 본 논문에서 사용된 샘플GJ, ST 및 K의 공업분석, 원소분석, 발열량 분석 결과를 확인할 수 있다. GJ의 가연성분(휘발분+고정탄소)은 ST보다 많으며 회분은 GJ(83.36%)이 ST(87.94%)보다 작은 것을 확인할 수 있다. 석탄 폐석이 회분을 높아 연소과정에서 산소와 가연성분의 산화 반응을 방해하는 효과가 있다[28]. 그리고 석탄 폐석이 석탄과 비교하였을 때는 가연성분은 매우 적고 회분은 매우 높은 점을 확인할 수 있다. 발열량도 저위발열량 기준으로 GJ와 ST는 다수 K보다 낮은 경향이 나타났다.
3.2 TGA 열중량 분석
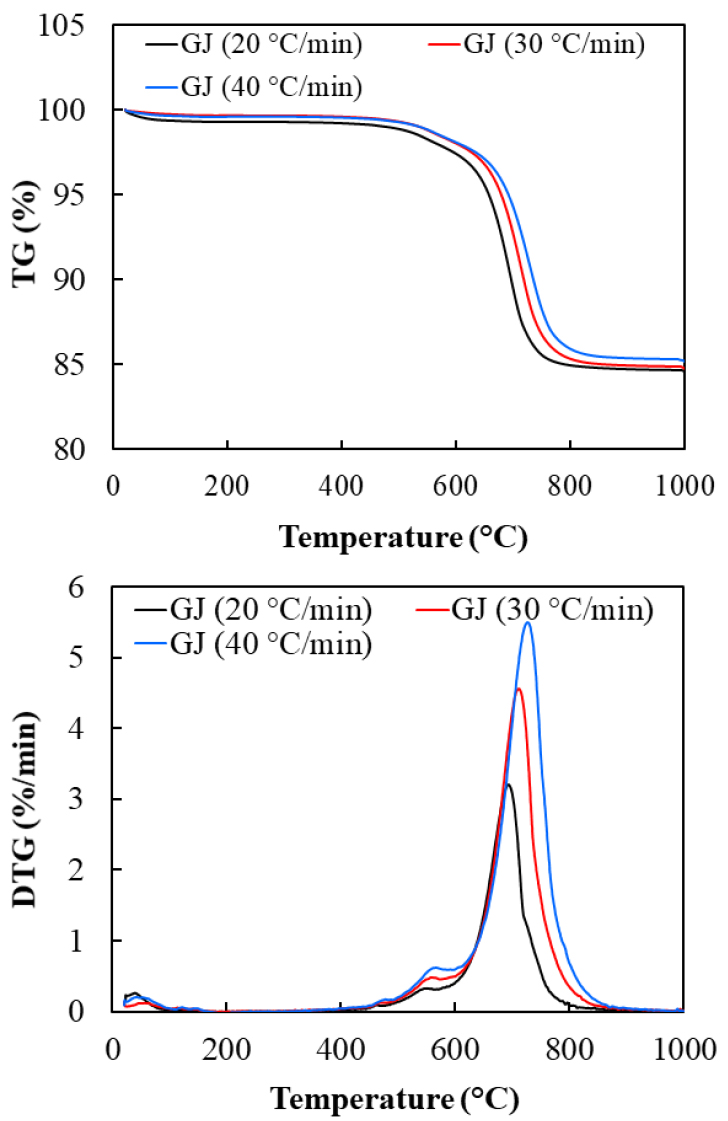
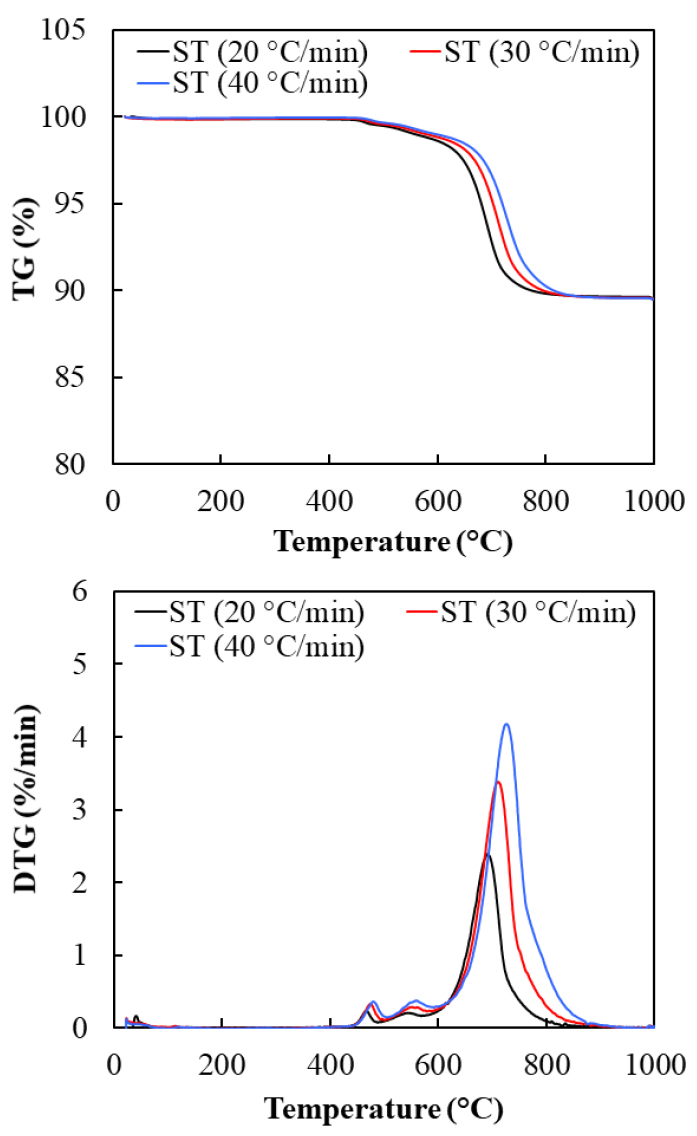
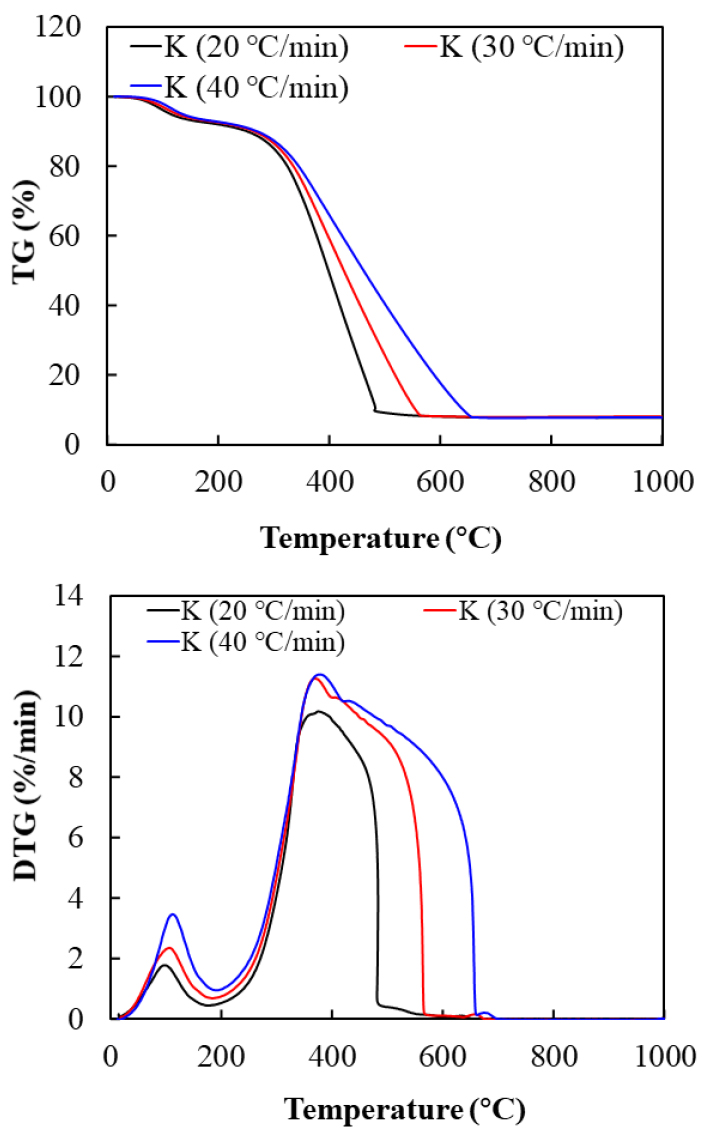
Fig. 3, 4, 5는 본 연구에서 사용한 샘플을 20, 30, 40 °C/min의 승온율로 상온에서 1,000°C/min까지 연소실험을 진행한 TG 및 DTG 그래프다. GJ와 ST의 연소과정은 크게 세 가지로 나눌 수 있다. 약 30°C부터 104°C 부근까지는 수분이 증발하는 영역이고 500~750°C 영역에서는 휘발분이 휘발된 후에 고정탄소의 연소 반응이 발생하여 급속 질량감소 반응을 보인다. 그리고 800°C 이후는 연소가 종료되어 무게 변화가 없다. 연소과정은 석탄과 같이 건조, 탈휘발, 휘발분과 고정탄소 연소로 나눌 수 있다. 그리고 승온 속도는 최종무게에 대한 영향이 작은 것을 확인할 수 있으며 수분 증발 과정에서도 영향이 크지 않은 것으로 확인할 수 있었다. 그러나 승온 속도 증가에 따라 표면부터 연료 중심까지 열전달 차이로 인해 연소 지연 현상이 발생하였다.
DTG 곡선은 TG 곡선의 미분한 값이며 DTGpeak 점은 최대 반응율을 의미한다. 승온 속도 증가에 따라 DTGpeak의 높이를 증가한다. 즉 승온 속도 증가에 따라 연소 반응율도 높아짐을 알 수 있었다. 이는 연소 특성을 향상시키는 것으로 선행연구와 같은 결과를 나타났다[16], [29]. 하지만 Tign과 Tb의 증가는 연소성이 저하된 지표다. 그래서 단순히 연소 반응 속도, Tign, Tb를 통해 승온속도가 연소과정의 영향을 평가하기 부족하며 본 연구에서 연소 특성 지수를 사용하여 연소성을 예측하였다.
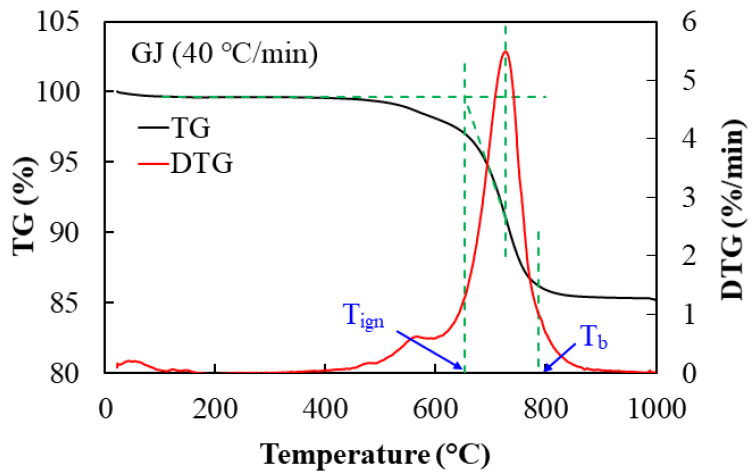
Table 4는 본 연구에서 사용한 각 샘플의 승온 속도별 연소 파라미터 결과를 정리하였다. Fig. 6과 같이 승온 속도가 40°C/min일 때 GJ의 TG, DTG 곡선을 예를 들어 나타내었다. 우선 DTG 곡선 피크 점을 통과하여 수직선을 그려 TG 곡선과 교차점부터 TG 곡선의 접선을 그렸다. 또한 수분이 증발한 초기 점의 수평선과 교차 위치에서 수직선을 내려 X축과 교점은 Tign를 나타낸다[15]. 연소종료 온도 Tb는 질량감소율 1%wt./min이 되는 지점의 온도로 정의하였다[30]. Table 4에서 정리된 연소 특성 지수를 확인하며 승온 속도의 증가에 따라 연소성이 향상된 것을 확인할 수 있었다.
Table 4.
Combustion characteristic parameters and combustion characteristic indexes of GJ, ST and K under different conversion
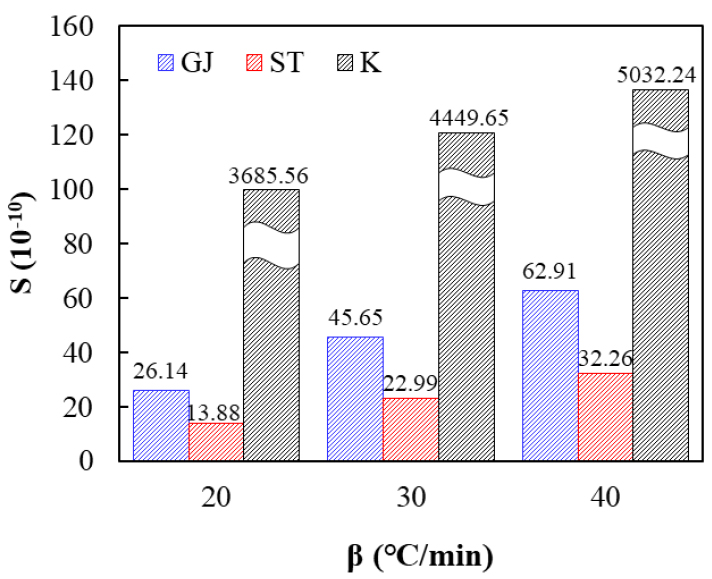
종합 연소 지수 S는 착화, 연소, 연소완성도(Burnout Properties)를 반영하여 클수록 연소 성능이 더 좋은 것을 나타낸다. Fig. 7에서 나오는 결과를 보면 GJ의 S값이 ST보다 높아 연소성을 더 좋은 것을 예측할 수 있으며 승온 속도 증가에 따라 GJ과 ST의 연소성 모두 개선되었다. 그리고 GJ이 승온 속도의 영향을 더 많이 받고 더 많이 개선된 경향을 보인다. 하지만 석탄 K와 비교했을 때는 석탄 폐석의 착화 온도와 연소 종료 온도가 높으면서 연소 특성지수 또한 석탄보다 매우 낮은 것을 확인하였다. 이는 석탄 폐석의 연소성이 석탄보다 우수하지 못한 것을 보인다.
3.3 연소 kinetic 분석
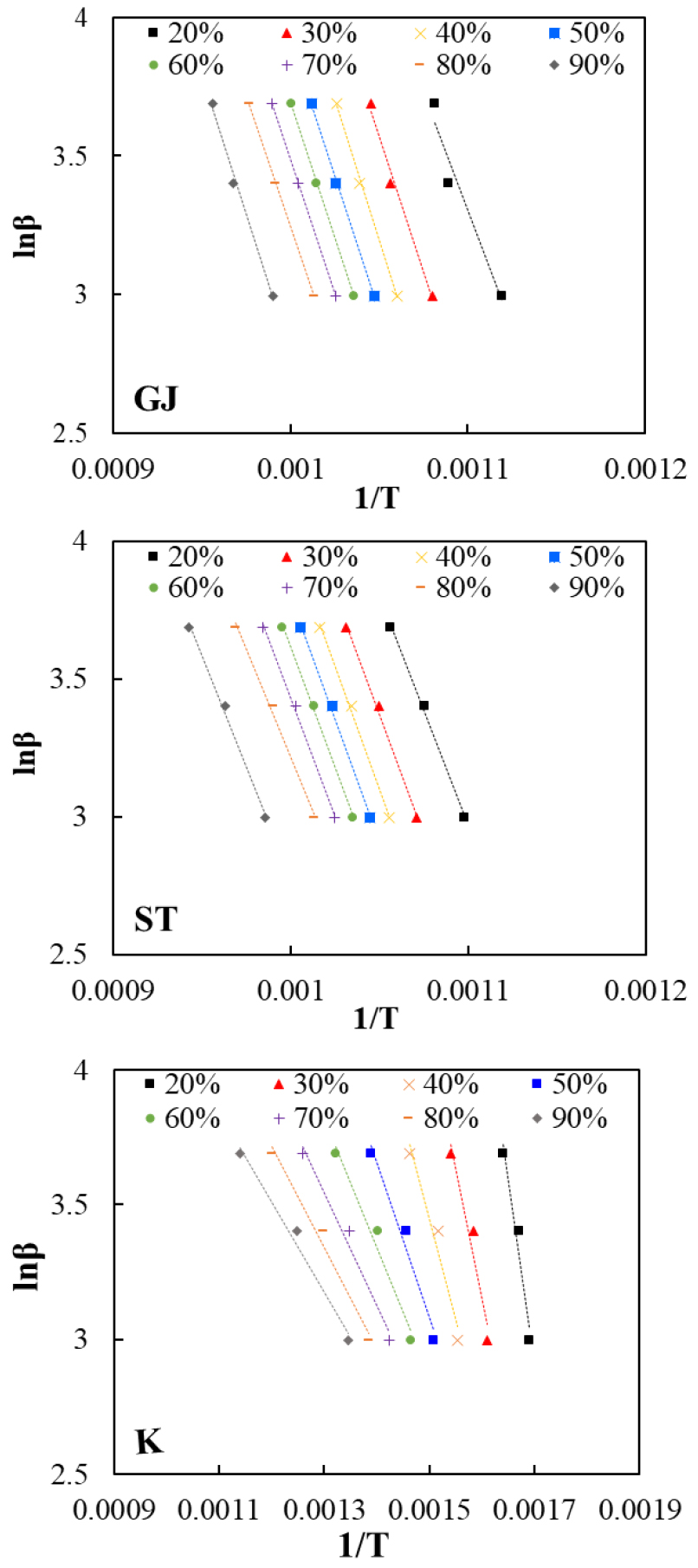
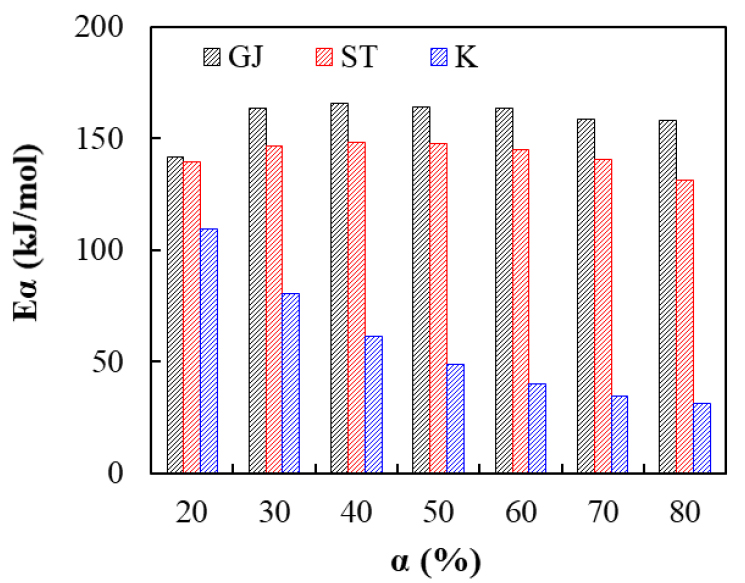
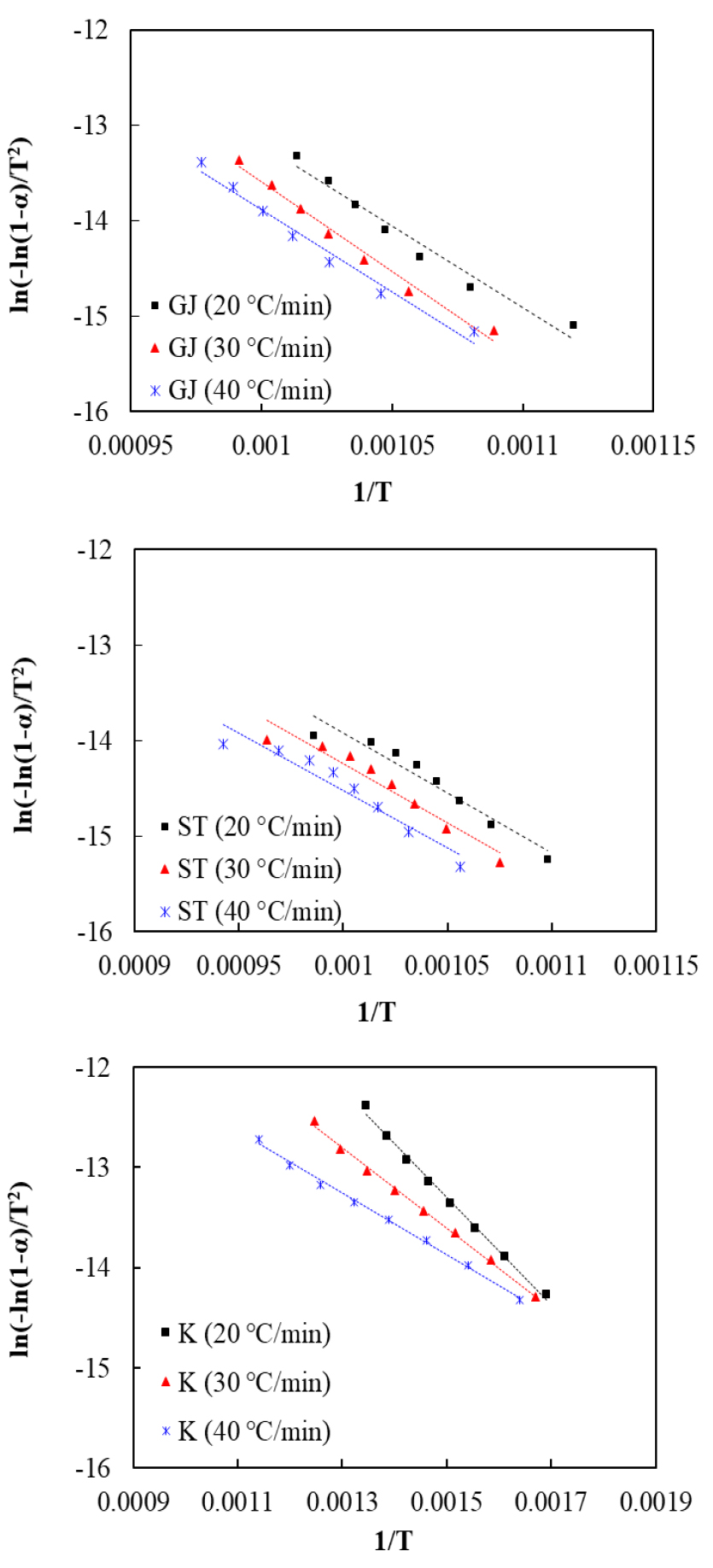
본 연구는 활성화 에너지 등 Kinetic 변수를 도출하기 위하여 OFW법과 C-R법을 사용하며, 도출된 결과를 각각 Fig. 8과 Fig. 10과 같이 그래프에 나타내었다. OFW법은 전환율에 따라 활성화 에너지의 변화 추세를 반영할 수 있다. Table 5는 OFW 법을 사용하여 승온 속도 20, 30, 40°C/min일 때 전환율별 활성화 에너지를 정리하였다. Fig. 9은 활성화 에너지 곡선을 나타내었다. 활성화 에너지를 도출하기 위하여 전환율 0.2 < α < 0.8을 사용하였다. R2는 거의 0.97 이상 도달하였으며 R2이 1과 가까울수록 정확도가 높다는 것을 선행 논문에서 알 수 있다[31]. OFW법을 통해 구해진 활성화 에너지는 GJ의 경우 141.47~165.71 kJ/mol, ST는 131.01~148.07 kJ/mol이며 K는 30.96 kJ/mol~109.25 kJ/mol이다. GJ의 활성화 에너지는 ST보다 높지만, 차이가 크지 않은 것을 확인하였다. 그러나 K의 활성화 에너지는 GJ와 ST와 비교해 상대적으로 낮은 것을 확인하였다. GJ와 ST는 전환율의 증가함에 따라 활성화 에너지가 증가하다가 감소한 후 다시 증가하는 경향을 나타냈다. GJ와 ST 모두 α=0.3일 때 활성화 에너지는 최댓값을 가진다. 휘발분은 연소 반응 중 초기일 때 활발히 탈휘발 반응이 일어나 연소반응을 촉진한다[16]. 0.2 < α < 0.3일 때 휘발분이 감소하며 고정탄소의 연소가 시작되어 활성화 에너지가 증가하였다. 고정탄소의 연소와 광물성 물질의 촉매 효과를 통해 활성화 에너지가 감소하였다[23]. 하지만 K의 경우, 연소반응의 진행에 따라 활성화 에너지를 감소하는 경향을 나타내었다.
Table 5.
Activation energy of GJ, ST and K under different conversion by OFW
| GJ | ST | K | |
| α (%) | E (kJ/mol) | ||
| 20 | 141.47 | 139.26 | 109.25 |
| 30 | 163.52 | 146.31 | 80.52 |
| 40 | 165.71 | 148.07 | 61.05 |
| 50 | 163.79 | 147.84 | 48.49 |
| 60 | 163.35 | 144.98 | 40.12 |
| 70 | 158.46 | 140.73 | 34.72 |
| 80 | 157.77 | 131.01 | 30.96 |
Table 6에서는 C-R법을 사용하여 승온 속도별 전체 반응의 평균 활성화 에너지와 빈도인자를 나타내었다. 우선 GJ의 활성화 에너지는 승온 속도에 따라 각각 143.97, 145.77. 15.325 kJ/mol이고 ST는 139.23, 143.33, 144.5 kJ/mol이며 K는 25.68, 33.31, 44.54 kJ/mol이다. 승온 속도 증가에 따라 연소 반응을 발생하기 위한 활성화 에너지는 낮아지며 빈도인자가 증가할수록 연소반응이 더 쉽게 일어나며 내부에 더 빈번한 반응을 일어나는 것으로 예측하였다.
Table 6.
Kinetic parameters of GJ, ST and K under different conversion by C-R
3.4 회 점착 및 용융 분석 결과
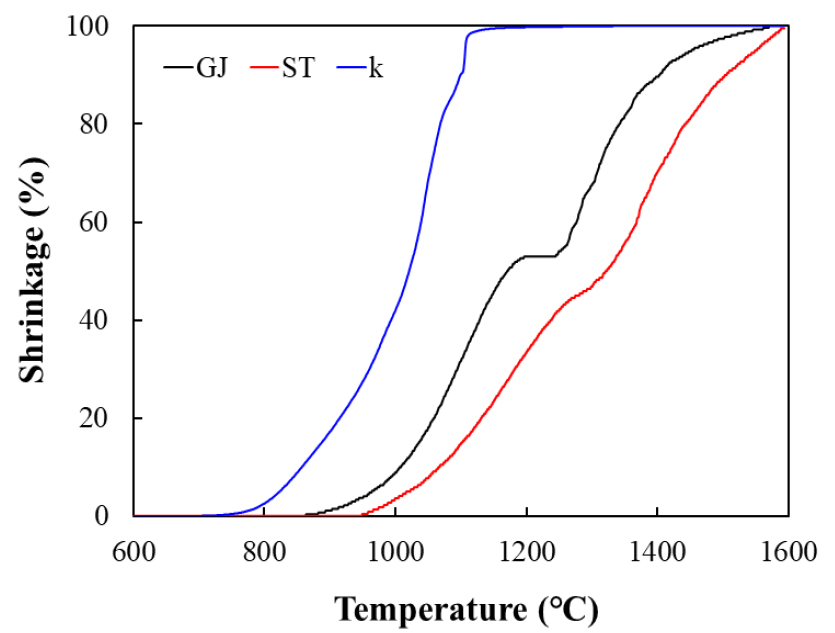
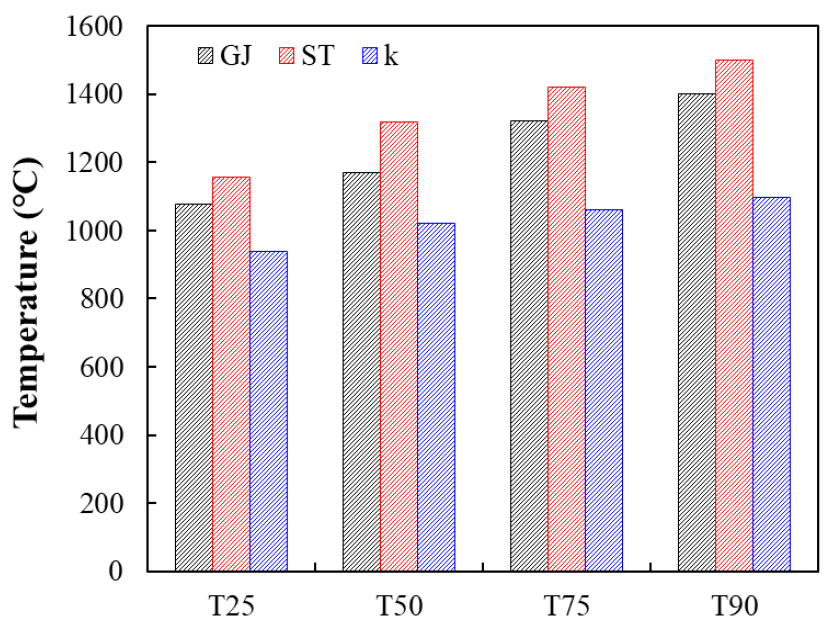
Fig. 11에서 TMA 실험 결과를 나타내었다. TMA 실험 결과를 TX%에 따라 Fig. 12와 Table 7같이 정리하였다. TMA 실험 결과를 통해 GJ과 ST가 높은 용융온도를 가지며 상대적으로 K는 낮은 용융온도를 가진 것을 확인하였다. 이는 샘플의 물성 분석을 통해 이해할 수 있다. Table 8은 용융점에 영향을 주는 성분을 정리하였다. SiO2 + Al2O3, K2O, CaO 및 Fe2O3에 의해 회 용융 특성에 대한 영향을 예측할 수 있다. 우선 Refractory contents인 SiO2 + Al2O3는 ST(89.4%), GJ(86.10%)와 K(57.50%)로 나왔다. 이에 따라 용융점은 ST > GJ > K로 예측할 수 있다. SiO2와 Al2O3는 높은 용융 온도를 가지고 있어 함량이 높을수록 회의 용융 온도를 높여주며 Fig. 12의 결과인 T90%을 확인하면 ST(1502°C)가 GJ(1402°C)보다 높은 용융 온도를 가진 것을 알 수 있었다. 그리고 Fluxing contents인 K2O, CaO, Fe2O3는 함량이 높을수록 회의 용융 온도는 낮아진다. 따라서 CaO와 Fe2O3 및 K2O의 함량은 GJ이 ST보다 높기 때문에 초기 용융 온도인 T25%이 GJ이 ST보다 약 80°C 정도 더 낮은 것을 확인할 수 있다. 그러나 K2O의 함량이 높으면 응결, 소결 및 슬래깅이 발생될 수 있는 점을 주의해야 한다[32].
Table 7.
TMA results of GJ, ST and K
| GJ | ST | K | |
| T25 | 1077 | 1157 | 940 |
| T50 | 1170 | 1320 | 1021 |
| T75 | 1321 | 1420 | 1060 |
| T90 | 1402 | 1502 | 1099 |
Table 8.
Chemical composition of the ash
| GJ | ST | K | |
| SiO2+Al2O3 | 86.10 | 89.40 | 57.50 |
| CaO | 0.95 | 0.50 | 11.07 |
| Fe2O3 | 5.67 | 4.24 | 18.15 |
| K2O | 4.17 | 3.83 | 1.69 |
Table 9는 식 (11), (12), (13)을 통해 회 용융 특성 지수를 나타냈다. GJ와 ST의 B/A ratio는 각각 0.14와 0.10이며 K는 0.64로 계산되었다. 이는 Table 3의 기준과 비교하면 GJ와 ST는 0.4보다 작으므로 회 용융점을 높은 것을 예측할 수 있고 K는 0.4 < 0.64 < 0.7이므로 낮은 용융점을 가질 것으로 예측하였다. 이 결과는 TMA 실험 결과와 일치한다. Sulfur slagging factor는 각각 0.15, 0.12와 0.08로 나왔는데, 이는 Table 3의 기준인 0.6보다 작아서 슬래깅 현상이 많이 발생하지 않을 것으로 예측할 수 있었다. 그리고 파울링 지수의 결과를 통해 GJ과 ST가 K보다 파울링 현상을 적게 발생한 것으로 예측된다.
4. 결 론
본 연구에서는 국내 강원도에서 생산된 석탄 폐석인 GJ와 ST에 대한 연소 특성 및 회 용융 특성을 분석하였으며 현재 순환유동층 발전소에 쓰이는 석탄 K와 비교하였다. Model-free법인 Flynn-Wall-Ozawa method를 통해 활성화 에너지를 도출하였고 Model-fitting법인 Coats-Redfern method를 통해 활성화 에너지와 빈도인자를 도출하였다. 그리고 고회분 연료인 석탄 폐석에 대한 회 용융 특성을 분석하였다.
1) 공업분석을 통해 GJ가 ST보다 더 많은 휘발분과 고정탄소를 가지고 회분 함량이 상대적으로 적어 연소성이 더 좋은 것으로 분석되었으며 이는 TGA 실험 결과와 일치하였다. 그리고 DTG 결과를 통해 승온 속도 증가에 따라 연소 반응이 촉진되었고 종합연소성지수(S)도 승온 속도 증가에 따라 함께 증가하여 연소성이 개선된 것을 확인하였다. 하지만 반전 현장에서 사용 중인 K 석탄과 비교했을 때 석탄 폐석은 연소성이 우수하지 못하고 발열량이 낮은 것을 확인할 수 있었다.
2) OFW법을 통해 도출한 GJ의 활성화 에너지는 141.47~165.71 kJ/mol이고 ST의 활성화 에너지는 131.01~148.07 kJ/mol 이다. C-R법을 통해 구한 활성화 에너지는 OFW법과 비슷한 경향성을 나타내었다. 승온 속도 증가에 따라 활성화 에너지는 감소하였으며 이는 화학반응이 발생할 때 필요한 최소 반응 활성화 에너지가 감소함을 나타낸다. 이는 승온 속도 증가에 따라 빈도인자도 증가하여 반응이 더 활발히 일어나 연소성이 좋아진 것으로 판단되었다.
3) TMA 결과와 회 점착 경향 지수를 통해 도출된 회 용융 특성은 GJ와 ST가 높은 회 용융 온도를 가진 것을 확인할 수 있었다. 회 점착 경향 지수인 B/A ratio, Sulfur slagging factor, Fouling index를 통하여 석탄 폐석의 용융점이 높을 뿐만 아니라 회분이 많지만 슬래깅과 파울링 현상은 적을 것으로 예측된다.
4) 석탄 폐석의 연소성은 좋은 경향성을 나타내지는 않았으나, 순환유동층 보일러에서 연료로 층물질과 순환하며 체류 시간을 연장할 수 있기 때문에 석탄 폐석 같은 저등급 연료도 적응이 잘 되는 것이다. 그리고 순환유동층보일러 내부 층물질로도 사용할 수 있으나 포타슘의 함량이 높아 응결, 슬래깅이 발생할 수 있다는 문제점을 유의해야 한다.
5) 단일 석탄 폐석의 연소성은 우수하지 못하지만, 석탄과 혼소하면 더욱 석탄 폐석의 연소성을 향상할 수 있을 것으로 예측된다.