1. 서 론
2. 방법론 및 실험장비
2.1 방법론
2.2 실험장비
3. 실험 결과 및 논의
3.1 질소 첨가가 NOx 배출에 미치는 영향
3.2 공기 추가가 NOx 배출에 미치는 영향
3.3 일정 산화제 유량 조건에서 질소 분율의 영향
4. 결 론
1. 서 론
대기질 규제가 강화되고 있음에도 불구하고, 가스터빈 및 산업용 버너와 같은 고온 연소 시스템에서는 여전히 질소산화물(NOx)이 지속적으로 배출되고 있다. NOx는 주로 NO와 NO2로 구성되며, 호흡기 및 심혈관 질환을 유발하고 오존 및 2차 미세먼지 생성의 전구물질로 작용하는 대표적인 대기오염 물질이다[1,2]. 세계보건기구(WHO)는 2021년 개정 대기질 지침에서 연평균 NO2 권고 기준을 10 µg/m³로 강화하였으며, 낮은 농도에서도 인체에 유해한 영향이 나타날 수 있음을 보고하였다[1]. 이에 따라 고온 연소 장치에서의 효과적인 NOx 저감 기술 개발은 중요한 공학적 과제로 인식되고 있다.
NOx는 연료 및 산화제에 포함된 질소와 산소의 반응을 통해 생성되며, thermal NOx, prompt NOx, N2O 중간체 경로, NNH 경로 등 다양한 생성 메커니즘이 존재한다[3,4,5,6]. 이 중 thermal NOx는 고온 조건에서 반응 속도가 지수적으로 증가하므로, 가스터빈과 같은 고온 연소 환경에서 지배적인 경로로 작용한다[7]. 따라서 화염 온도 저감과 반응물 조성 제어는 thermal NOx 억제를 위한 핵심 전략으로 간주된다.
이를 위해 연소 기반 저감 기술들이 개발되어 왔다. 예혼합 연소 적용, 연소 단계화(staged combustion), 배기가스 재순환(flue gas recirculation, FGR) 등이 대표적이다[8,9,10]. 그러나 이러한 방법들은 버너 구조 변경이나 추가 설비를 요구하는 경우가 많아 기존 시스템에의 적용에는 제약이 따른다. 따라서 구조적 개조 없이 적용 가능한 간단한 저감 전략에 대한 요구가 존재한다.
본 연구는 항공기 연료 탱크의 막 기반 공기 분리 시스템에서 착안하였다. 해당 시스템은 중공사막 모듈을 이용하여 공기를 질소 농축 공기로 분리함으로써 연료 탱크 내부의 산소 농도를 낮추고 안전성을 확보한다[11]. 본 연구에서는 이와 유사한 원리를 연소 시스템에 적용하여, 질소 농도가 증가된 산화제를 공급함으로써 thermal NOx를 저감할 수 있는지 실험적으로 검증하였다. 이를 위해 고분자 중공사막 모듈의 선택적 투과 특성을 모사한 질소 희석 기반 산화제 조성 제어 전략을 제안하고, 이를 대기압 조건의 예혼합 메탄–공기 스월 화염에 적용하였다. 제안된 방법은 산화제 내 질소 비율을 증가시키고 산소 농도를 감소시켜 화염 온도를 낮춤으로써 thermal NOx 생성을 억제하는 방식이다. 특히, 버너 구조 변경이나 능동 제어 장치 없이 기존 공기 공급 라인의 조성 조절만으로 적용 가능함을 확인하였다. 본 연구는 이러한 산화제 조성 제어 전략의 NOx 저감 가능성을 체계적으로 평가하고, 고온 연소 시스템에 적용 가능한 개조(retrofit) 기술로서의 타당성을 제시하고자 한다.
2. 방법론 및 실험장비
2.1 방법론
2.1.1 화학반응속도론
NOx 생성에는 여러 반응 경로가 존재하는 것으로 알려져 있다. 일반적으로 thermal NOx는 고온 연소 조건에서 비교적 넓은 당량비 범위에 걸쳐 지배적인 반응 경로로 작용하는 반면, prompt NOx는 연료 농후 조건(ϕ > 1)에서 그 중요성이 증가한다. 또한 N2O 중간체 경로는 매우 희박하고 저온의 연소 조건에서 주로 기여하는 것으로 보고되고 있다[4,5].
당량비(ϕ)는 실제 연료–공기비와 이론 당량비의 비로 정의되는 무차원 지표로, ϕ = 1은 화학양론 조건, ϕ < 1은 희박(lean), ϕ > 1은 농후(rich) 조건을 의미한다. 본 연구에서 고려한 당량비 ϕ = 1 및 연료 희박 조건(ϕ < 1)에서 Fig. 4, 5, 6에 나타난 바와 같이 단열화염온도가 약 1800 K 이상으로 유지되며, 이는 thermal NOx 생성을 촉진하는 고온 연소 조건에 해당한다[7]. 반면, 본 연구는 메탄 예혼합 연소를 대상으로 하여 연료 결합 질소에 의한 fuel NOx 생성은 배제할 수 있으며, 연료 농후 영역이 형성되지 않으므로 prompt NOx의 기여 역시 제한적일 것으로 판단된다. 또한 본 실험 조건의 고온 예혼합 연소 환경에서는 N2O 중간체 메커니즘의 영향도 상대적으로 미미할 것으로 예상된다.
따라서 본 연구에서는 thermal NOx가 NO 생성의 지배적인 반응 경로로 작용한다고 판단하였으며, thermal NOx 생성을 설명하는 대표적인 반응 기구인 Zeldovich 메커니즘을 기반으로 화학 반응 속도 해석을 수행하였다. Thermal NOx 생성은 다음과 같은 반응에 의해 지배된다.
상기 반응식을 기반으로 원자 질소(N)에 대해 준정상상태 가정(quasi-steady-state assumption, QSSA)을 적용하였다. 이는 원자 질소의 농도가 매우 낮으며, 생성 및 소멸 반응 속도가 전체 NO 생성 과정에 비해 상대적으로 매우 빠르게 이루어진다는 점에서 타당하다. 이에 따라 원자 질소의 정상상태 농도는 다음과 같이 유도될 수 있다[12].
또한, 고온 화염에서는 해리 반응이 빠르게 진행되므로 O2와 O 종이 국소 화학평형(local chemical equilibrium)에 도달한다고 가정할 수 있다. 따라서 원자 산소 농도는 평형상수 Kp를 이용해 다음과 같이 표현된다.
식 (3)과 (5)를 Zeldovich 반응의 순반응 속도식에 대입하면, NO 생성 속도식은 단일 전역 반응식 형태로 정리될 수 있다.
계산된 반응 속도 상수와 평형상수를 이용하여 혼합기 조성 및 반응 온도의 영향을 반영하였으며, NO 생성 속도는 단열 화염 온도(Tad)의 함수로 수치적으로 평가되었다. 산소 및 질소 농도와 단열 화염 온도는 엔탈피 평형에 기반한 1차원 Cantera 시뮬레이션을 통해 계산하였고, 화학 반응 해석에는 GRI-Mech 3.0 상세 반응 메커니즘을 적용하였다[13].
이렇게 도출된 전역 반응 파라미터는 스월 버너 실험에서 관측된 NOx 배출 경향을 해석하는 데 활용되었다. 단순화된 전역식은 모든 개별 반응 경로를 포함하지는 않지만, 실험에서 지배적으로 나타난 thermal NOx 경향을 물리적으로 일관되게 해석할 수 있는 틀을 제공한다.
2.1.2 CH* 화학발광
화염 구조 진단은 화학발광(chemiluminescence) 이미징을 기반으로 수행하였다. OH* 화학발광은 주로 280–350 nm의 자외선(UV) 영역에서 방출되며, 약 308 nm 부근에서 최대 강도를 나타낸다. 이에 따라 자외선 투과가 가능한 석영 광학계와 310 nm 중심 파장의 협대역 통과 필터의 사용이 요구된다[14]. 반면, CH* 화학발광은 약 430 nm 파장에서 강한 방출을 보이므로 가시광 영역에서 신호 획득이 가능하며, 상대적으로 광학적 제약이 적다.
본 연구에서는 실험 구성의 용이성과 신호 접근성을 고려하여 430 nm 대역통과 필터를 사용한 CH* 화학발광 이미징을 적용하였다. CH* 신호는 일반 가시광 렌즈 및 필터를 통해 안정적으로 획득할 수 있으며, 열방출률과 높은 상관관계를 가지는 것으로 알려져 있어 화염 전면 및 주요 반응 영역을 나타내는 대표적 지표로 활용된다[15].
본 연구의 목적은 화염의 기하학적 특성이 체류시간 및 NOx 생성에 미치는 영향을 규명하는 데 있으므로, CH* 화학발광을 이용하여 주요 반응 영역을 시각화하고, 다양한 운전 조건에서의 화염 구조 변화를 정량적으로 비교·분석하였다.
2.1.3 아벨 역변환 및 체류시간
CH* 화학발광 이미지는 신호 신뢰도를 확보하기 위해 노이즈 제거, 배경 보정, 대비 향상 등의 전처리 과정을 거쳤다. 각 실험 조건에서 50장의 순간 이미지를 획득한 후 앙상블 평균을 수행하여 신호 대 잡음비(signal-to-noise ratio, SNR)를 향상시켰다. 또한 이미지 처리 과정에서는 강도 표현 범위를 확장하기 위해 16-bit 그레이스케일 형식을 적용하였다. 이를 통해 저강도 화학발광 신호를 효과적으로 유지하고, 화염 구조와 배경 노이즈를 보다 명확히 구분할 수 있었다.
전처리된 화염 영상은 축대칭(axisymmetric) 조건을 만족하도록 정렬한 뒤, 선적분(line of sight)된 2차원 영상에 아벨 역변환(inverse Abel transform)을 적용하여 3차원 강도 분포 f(r,z)를 재구성하였다[16]. 아벨 변환은 축대칭 강도장이 시선 방향으로 투영되어 관측 영상 F(y,z)로 표현되는 수학적 관계를 나타낸다[17]. 정방향 아벨 변환은 축대칭 강도장의 투영 과정을 의미하며[18], 아벨 역변환은 이 투영 영상으로부터 반경 방향 강도 분포를 복원하여 원래의 3차원 화염 구조를 재구성하는 과정이다[19].
화염 경계는 background 신호를 제거한 후, 기준 공기 기준 최대 CH* 강도의 약 50% 이상을 갖는 영역으로 정의하였다. 이러한 기준은 조건 간 일관성을 유지하기 위해 모든 실험 조건에 동일하게 적용하였으며, 해당 임계값을 기준으로 아벨 변환을 수행하였을 때 실제 화염 형태와 가장 유사한 결과를 보임을 확인하였다. 또한 임계값을 변화시킨 경우에도 체류시간 변화의 전반적인 트렌드는 유사하게 유지되어, 본 연구에서 적용한 화염 경계 정의가 체류시간 산정 결과에 미치는 영향은 제한적인 것으로 판단된다. CH* 화학발광 이미징을 위한 카메라 및 광학 필터 설정 조건은 Table 1에 정리하였다.
Table 1.
Camera and optical settings for CH* chemiluminescence imaging under experimental conditions with constant oxidizer flow rate
|
Camera settings | Camera model | Nikon D7500 |
| ISO | 51200 | |
| Exposure time | 1/15 s | |
| Aperture (f-number) | f/4 | |
| Optical filter | Type | Band-pass filter |
| Center wavelength | 430 nm | |
| Bandwidth (FWHM) | 10 nm |
Fig. 1은 선적분으로 획득된 화염 영상으로부터 체적 방출 강도 분포를 재구성하기 위한 아벨 변환의 개념을 나타낸다. 본 연구에서는 Fig. 2에 제시된 절차에 따라 아벨 변환을 수행하였다. 재구성된 강도 분포는 CH* 방출의 공간적 분포를 반영하며, 이를 기반으로 화염 체적을 정량화하였다. 먼저, 아벨 역변환으로 얻은 강도 분포를 광학 배율과 버너 형상을 고려하여 산정된 공간 보정 계수를 이용해 픽셀 좌표에서 실제 물리적 길이로 변환하였다. 각 축 방향 위치에서 반경 방향 CH* 강도 분포로부터 국소 화염 반경을 산정하였다. 이후 원통형 체적 요소를 적용하여 미소 화염 체적을 계산하고, 이를 축 방향으로 적분하여 전체 화염 체적 Vf를 구하였다. 산정된 화염 체적은 체적 기반 정의에 따라 체류시간 계산에 활용되었으며, 체류시간은 다음과 같이 정의된다.
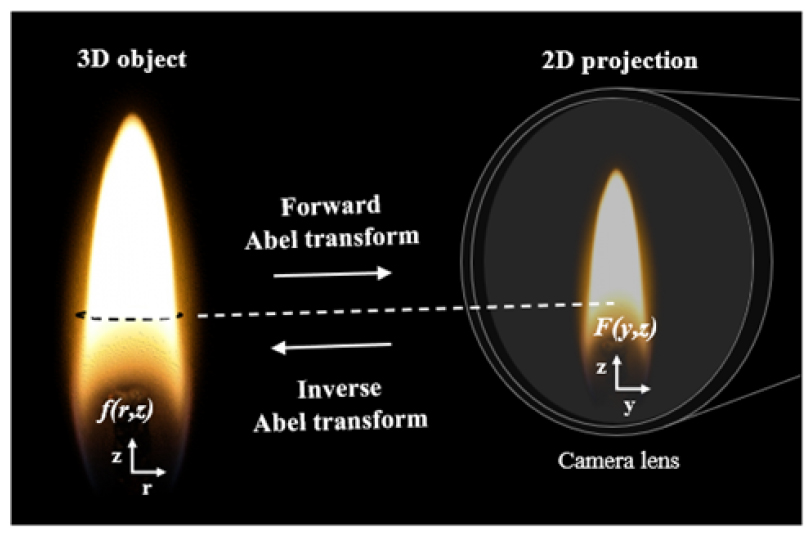
Fig. 1.
Concept of Abel transform relating the volumetric emission field to the line-of-sight integrated image[16].
여기서 Vf는 적분된 화염 체적, ua는 노즐 출구에서의 평균 축방향 유속, A는 노즐 단면적을 의미한다. 본 연구에서는 이렇게 계산된 체류시간을 thermal NOx 생성과의 상관관계를 분석하는 데 활용하였다. 기존 연구에 따르면 체류시간이 증가할수록 고온 영역에서의 반응 지속 시간이 길어져 thermal NOx 생성률이 증가하는 경향이 보고되어 있다[20]. 본 연구에서도 유사한 경향이 관찰되었으며, 다양한 운전 조건에서의 NOx 배출 특성을 정량적으로 해석할 수 있는 근거를 제공하였다.
2.2 실험장비
2.2.1 스월 버너
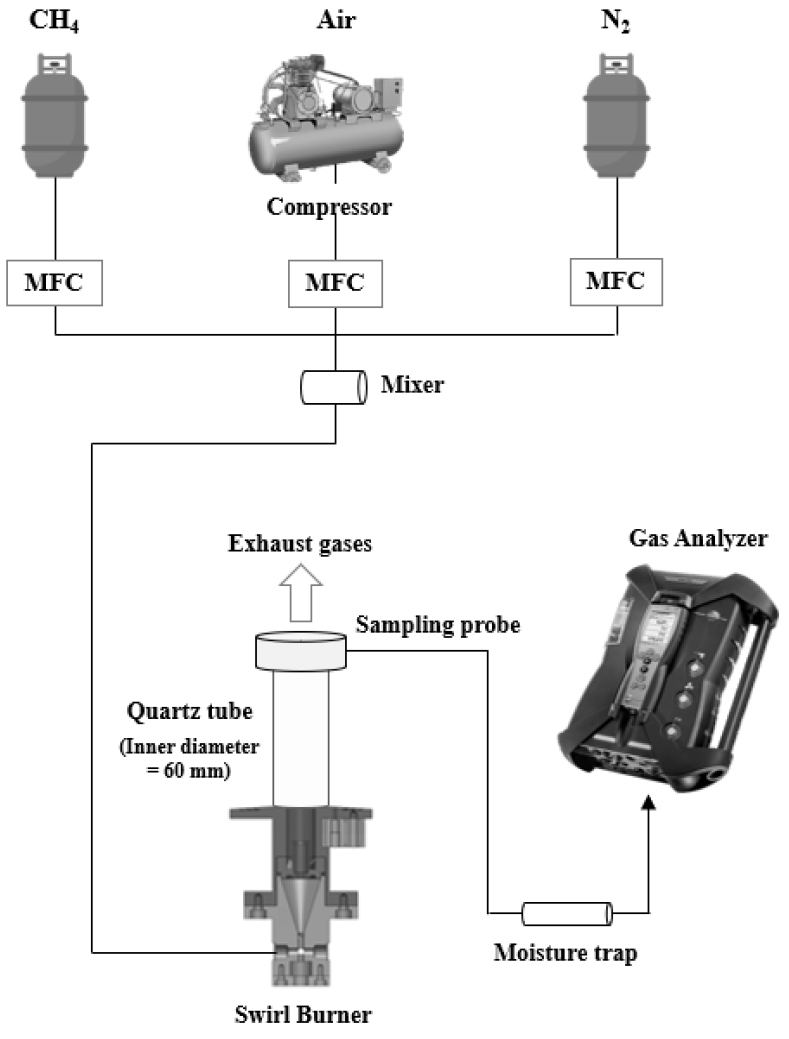
Fig. 3은 본 연구에 사용된 연소 실험 장치의 개략도를 나타낸다. 모든 실험은 대기압 조건에서 수행되었으며, 스월 수 0.6으로 운전되는 스월 안정화 버너를 사용하였다. 스월 수는 유동 내 회전 강도를 나타내는 무차원 지표로, 각운동량 유속과 축방향 운동량 유속의 비로 정의된다[21]. 스월 수가 증가할수록 회전 성분이 강화되며, 축류형 베인 스월러(axial-type vane swirler)의 경우 스월 수는 스월러의 기하학적 형상에 기반하여 식 (10)과 같이 근사적으로 산정할 수 있다[22].
여기서 외경 d, 허브 직경 dh, 베인 각도 θ는 축방향에 대해 정의된다. 예혼합 메탄 연소에서 스월 수 약 0.6은 내부 재순환 영역(internal recirculation zone, IRZ)의 형성을 유도하여 화염 안정화에 기여하며, 축대칭 화염 구조를 형성하는 데 중요한 역할을 한다[23]. 이러한 유동 구조는 산화제 조성 변화로 반응성이 저하되는 조건에서도 안정적인 화염 유지를 가능하게 하며, 온도, 혼합 및 체류시간이 NOx 생성에 미치는 영향을 정량적으로 분석할 수 있는 기반을 제공한다.
연료와 산화제 유량은 질량 유량 제어기(mass flow controller, MFC)를 이용하여 정밀하게 제어하였다. 조성이 조절된 산화제는 연소기 유입 전 상류 믹서에서 연료와 충분히 예혼합되었다. 반응 영역은 석영(quartz) 챔버로 구성하여 광학적 접근성을 확보하는 동시에 유동 안정성을 유지하였다.
NOx 농도는 전기화학식 가스 분석기(TESTO 350 K)를 사용하여 측정하였으며, 하류 출구에서 일정 유량으로 가스를 채취하여 분석기로 이송함으로써 신뢰성 있는 측정을 확보하였다. 가스 분석기의 측정 범위 및 분해능 등 주요 사양은 Table 2에 정리하였다. NOx 농도는 1 Hz의 샘플링 주기로 측정하였으며, 각 실험 조건에서 총 30개의 데이터를 취득한 후 평균값을 사용하였다.
Table 2.
Specifications of TESTO 350 K
| Sensor |
Range (Accuracy) | Resolution | Sampling rate |
| NO |
0-4,000 ppm (±5 ppm) | 1 ppm | 1 Hz |
| NO2 |
0-500 ppm (±5 ppm) | 0.1 ppm | |
| O2 |
0-25 vol.% (±0.8%) | 0.01% |
또한, 수분은 전기화학식 센서의 응답 특성에 영향을 미쳐 신호 변동이나 측정 오차를 유발할 수 있다. 이에 따라 분석기 상류에 전처리 장치를 설치하여 배기가스 내 수분을 제거함으로써 간섭을 최소화하고 측정 신뢰성을 확보하였다. 또한, NOx 배출 특성은 질소산화물 배출지수(EINOx)를 이용하여 평가하였다. 단순 농도 값은 연소 조건이나 희석 정도에 따라 영향을 받을 수 있으므로, 다양한 운전 조건에서 NOx 배출을 정량적이고 일관되게 비교하기 위해 EINOx를 적용하였다[24].
2.2.2 실험 조건
실험은 세 가지 조건(실험 A, B, C)으로 구분하여 수행하였다. 각 조건은 사전 실험을 통해 lean blowout, flashback, 화염 전이 한계를 확인한 후 설정되었다. 이를 바탕으로 화염이 안정적으로 유지되면서도 산화제 조성 변화에 따른 NOx 배출 특성이 충분히 나타나는 운전 범위를 선정하였다.
기존 연구에서는 산화제 내 질소 비율 증가 효과를 분석할 때 당량비와 체적 유량을 일정하게 유지하는 조건을 주로 적용하였다. 그러나 이러한 접근은 질소 비율 증가에 따라 연료 유량을 감소시켜야 하므로, 총 열방출률이 동시에 감소하는 한계를 가진다[25,26]. 본 연구에서는 열방출력 변화의 영향을 배제하고 산화제 조성 변화의 효과를 독립적으로 평가하기 위해, 모든 조건에서 연료 유량을 일정하게 유지하고 산화제 조성만을 변화시켰다.
실험 A에서는 산화제 내 질소 유량을 점진적으로 증가시켜 질소 희석 효과를 분석하였다.
실험 B에서는 질소 대신 공기 유량을 증가시켜, 불활성 희석 효과와 산화제 공급 증가 효과를 구분하고자 하였다. 실험 C에서는 총 산화제 유량을 일정하게 유지한 상태에서 질소 비율만을 변화시켰으며, 질소 유량 증가에 상응하는 만큼 공기 유량을 감소시켜 총 유량 변화의 영향을 배제하였다. 이를 통해 산화제 조성 변화 자체의 영향을 분리하여 분석할 수 있도록 하였다.
이들 조건을 체계적으로 설명하기 위해 메탄–공기 연소의 기준 전역 반응식(식 (12))을 정의하였다.
식 (13)는 실험 A에 해당하며, 동일한 산소량을 유지하면서 추가 질소를 공급한 경우를 나타낸다. 여기서 α는 연료 유량으로 정규화된 추가 질소 유량을 의미한다.
식 (14)는 실험 B에 해당하며, 공기를 추가 공급한 조건으로서 산소와 질소가 동시에 증가하는 경우이다. 이때 α + β는 추가된 공기 유량을 연료 유량으로 나눈 값이다.
식 (15)은 실험 C에 해당하며, 총 산화제 유량을 일정하게 유지한 상태에서 질소 비율만을 조정한 경우를 나타낸다. 이 조건에서는 질소 증가에 따라 공기 유량이 감소하므로 당량비가 변화하며, γ는 이러한 조성 변화를 반영하는 매개변수로 정의된다.
모든 실험은 기준 공기 유량 100 LPM 조건에서 수행되었으며, 각 실험 목적에 따라 해당 기준 조건으로부터의 변화를 적용하였다. 실험 조건의 세부 사항은 Table 3에 요약하였다.
Table 3.
Experimental conditions
3. 실험 결과 및 논의
3.1 질소 첨가가 NOx 배출에 미치는 영향
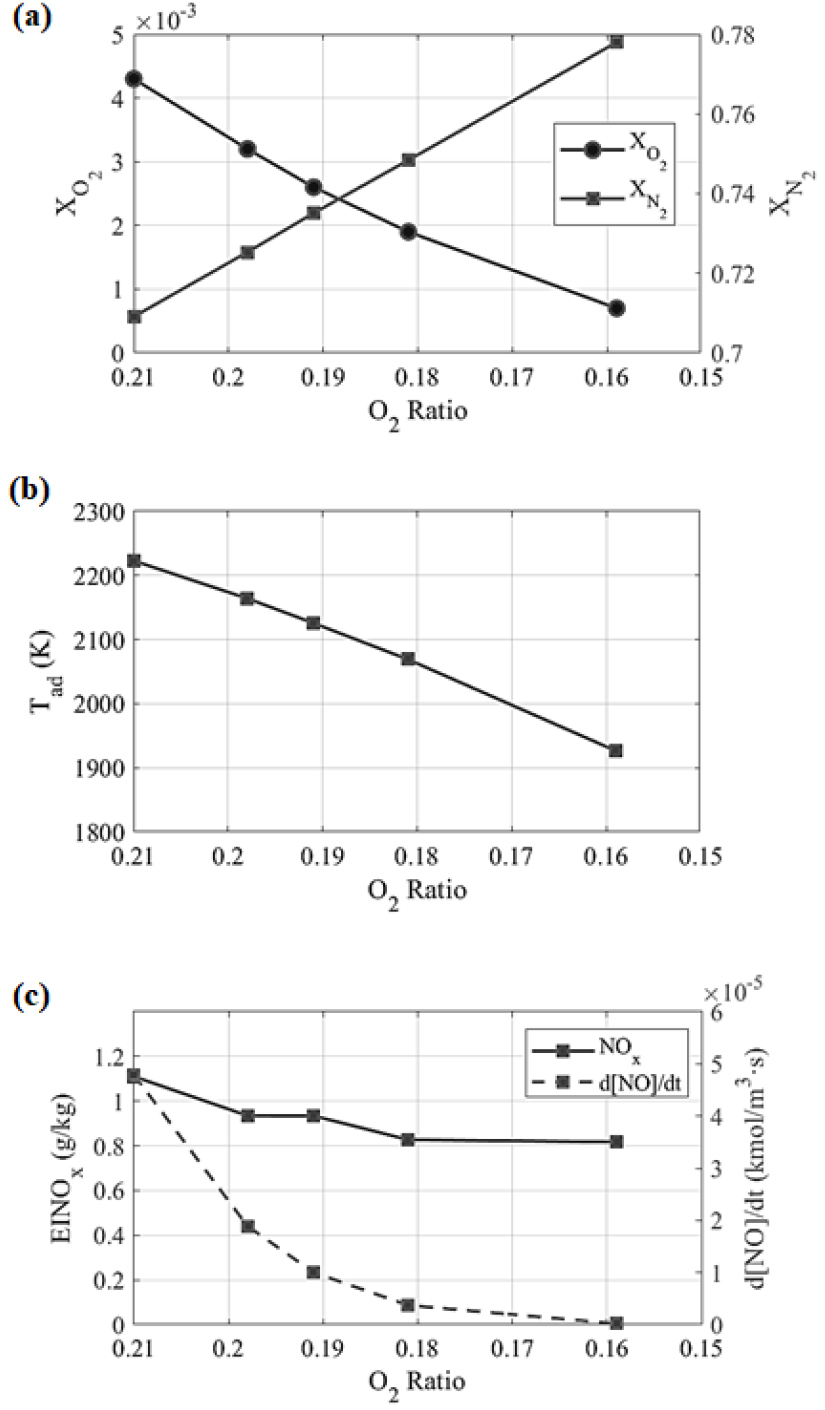
Fig. 4와 같이 산화제 내 질소 농도가 증가함에 따라 NOx 배출이 현저히 감소하는 경향이 확인되었다(실험 A). 기준 공기 조건에서 EINOx는 1.110으로 측정되었으며, 표준편차는 0.006으로 나타났다. 질소 비율이 증가함에 따라 EINOx는 점진적으로 감소하여, 질소 비율이 최대인 조건(O2 ratio 0.159)에서는 0.817로 감소하였고, 해당 조건의 표준편차는 0.002로 나타나 반복 측정에 따른 변동이 매우 제한적임을 확인하였다. 이는 기준 공기 조건 대비 약 26%의 EINOx 저감에 해당하며, 동일한 결과를 산소 농도 15% 기준으로 환산할 경우 약 45%의 감소 효과를 나타낸다.
이러한 NOx 저감은 두 가지 주요 메커니즘에 기인한다. 첫째, 질소 증가와 산소 감소로 인해 반응물 조성이 변화하면서 전체 산화 반응 속도와 활성 라디칼 풀이 감소하여 thermal NOx 생성이 억제된다. 본 연구에서는 연료 유량과 당량비를 일정하게 유지한 상태에서 질소 유량만을 증가시켰으며, 전역 반응식을 통해 도출한 생성물 조성을 기반으로 산소 및 질소 농도를 정의하여 이러한 조성 효과를 정량적으로 평가하였다. 이 과정에서 각 조건별 EINOx의 표준편차는 0.001–0.002 범위로 유지되어, 관측된 NOx 감소 경향이 실험적 오차가 아닌 조성 변화에 따른 물리적 효과임을 뒷받침한다.
둘째, 질소 첨가는 총 산화제 유량 증가를 수반하여 화염 온도를 저하시킨다. 화염 온도 감소는 thermal NOx 생성 속도를 직접적으로 낮추므로, 산소 농도 감소에 따른 조성 효과와 온도 저하의 복합적인 영향으로 NOx 배출이 크게 억제된 것으로 해석된다.
3.2 공기 추가가 NOx 배출에 미치는 영향
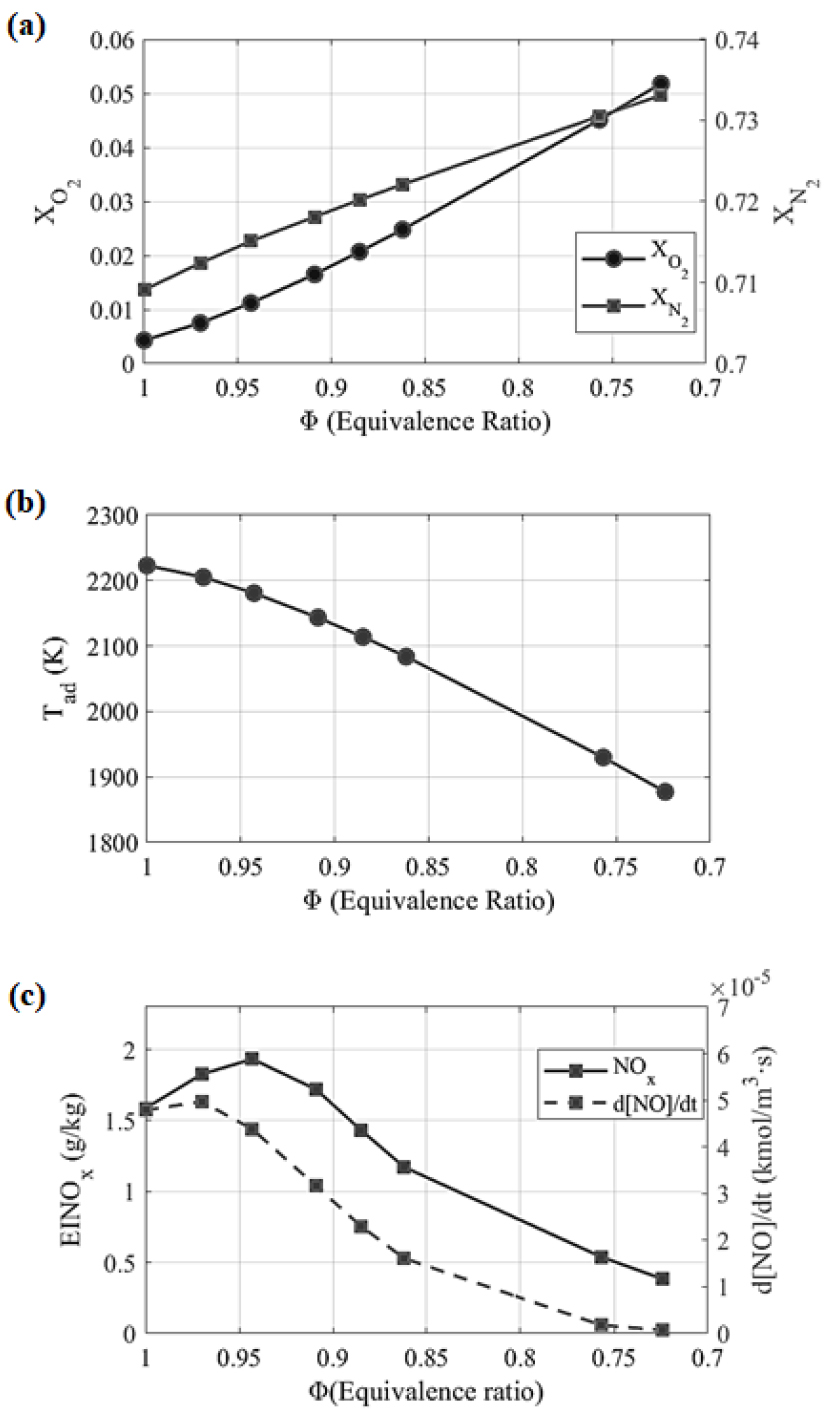
실험 B는 질소 추가(실험 A)의 대안으로 공기를 추가 공급하여, 산화제 유량 증가 효과를 직접 비교하기 위해 수행되었다. 실험 A에서는 열출력을 일정하게 유지한 상태에서 질소를 첨가함에 따라 총 산화제 유량이 증가하고 단열 화염 온도가 감소하였다. 이에 본 실험에서는 질소 대신 공기를 추가하여 산화제 유량 증가 효과를 구현하였으며, 그 결과 당량비가 점진적으로 감소하는 조건이 형성되었다. 본 연구에서는 연료 유량을 일정하게 유지하였으므로, 공기 유량 증가는 당량비를 1에서 더 희박한 영역으로 이동시키는 역할을 한다.
Fig. 5와 같이 산화제 유량 증가에 따라 단열 화염 온도는 감소하였으며, 이는 실험 A와 유사한 경향이다. 그러나 본 조건에서는 공기가 추가되므로 산소와 질소 농도가 동시에 증가하며, 질소 희석에 의해 산소 농도가 감소했던 실험 A와는 근본적인 차이가 있다.
NOx 배출은 초기 구간에서 증가하는 경향을 보였는데, 이는 반응물(특히 O2) 농도 증가로 인해 NOx 생성 반응이 촉진되었기 때문이다. 이후 산화제 유량이 더욱 증가함에 따라 화염 온도 저하 효과가 지배적으로 작용하여 NOx는 다시 감소하는 경향을 나타냈다. 이러한 NOx 변화는 각 조건에서 측정된 EINOx의 표준편차가 0.002–0.017 범위로 비교적 작게 유지된 가운데 관찰되어, 본 연구에서 논의한 반응물 농도 효과와 온도 감소 효과 간의 경쟁에 의해 결정된 NOx 생성 거동임을 뒷받침한다.
3.3 일정 산화제 유량 조건에서 질소 분율의 영향
3.3.1 질소산화물 배출량 비교
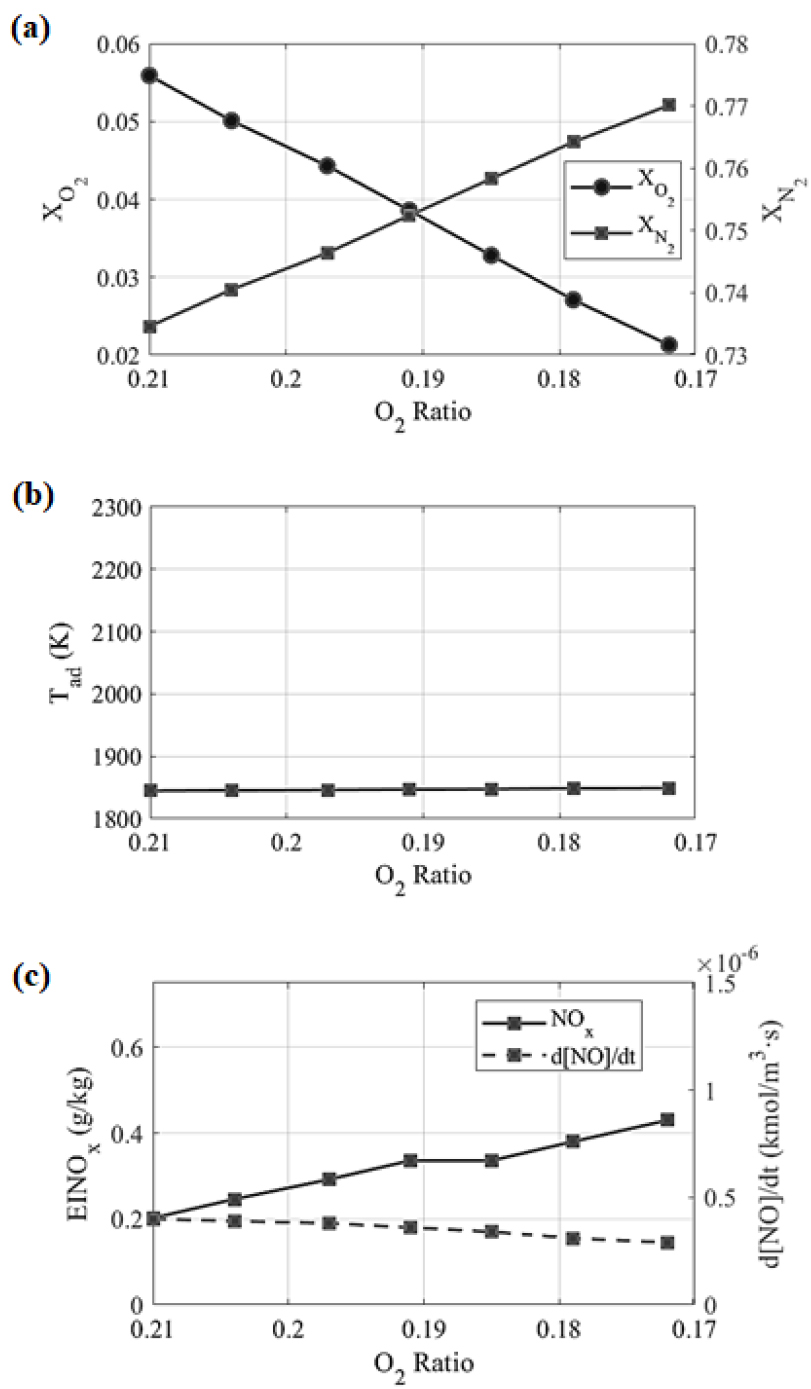
실험 C(총 산화제 유량 일정, 질소 분율 변화)에서는 NOx 저감 효과가 뚜렷하게 나타나지 않았다(Fig. 6). 본 조건은 총 산화제 유량을 유지한 상태에서 질소 분율만을 증가시키기 위해 설계되었으며, 이에 따라 질소 증가량만큼 공기 유량을 감소시켰다. 그 결과 당량비는 초기 조건 대비 증가하였고, 운전 범위는 ϕ = 0.704에서 0.859까지 확장되었다.
총 산화제 유량이 일정하므로 단열 화염 온도는 거의 변화하지 않았다. 그러나 측정된 NOx 배출은 단열 화염 온도만을 기준으로 예측한 NO 생성 속도의 경향과는 일치하지 않았다. 이는 NO 생성 속도가 국소적인 화학 반응 속도를 나타내는 지표로서, 고온 영역에서의 반응 지속 시간, 즉 체류시간의 영향을 직접적으로 반영하지 못하기 때문으로 판단된다. 본 조건에서 관측된 EINOx는 산소 분율 감소에 따라 증가하는 경향을 보였으며, 각 조건에서의 표준편차는 약 0.001–0.002 범위로 작게 유지되어 이러한 증가 경향이 반복 측정에 대해 일관되게 나타남을 확인하였다.
이러한 점을 고려하여, 본 연구에서는 CH* 자발광 이미지를 아벨 역변환하여 화염 체적을 산정하고, 이를 바탕으로 체류시간을 도출하였다. 체류시간 평가는 2장에서 제시한 방법을 적용하였으며, 체류시간을 함께 고려함으로써 실험 C 조건에서 관측된 NOx 배출 경향을 보다 합리적으로 해석하고자 하였다.
3.3.2 아벨 역변환 및 체류시간
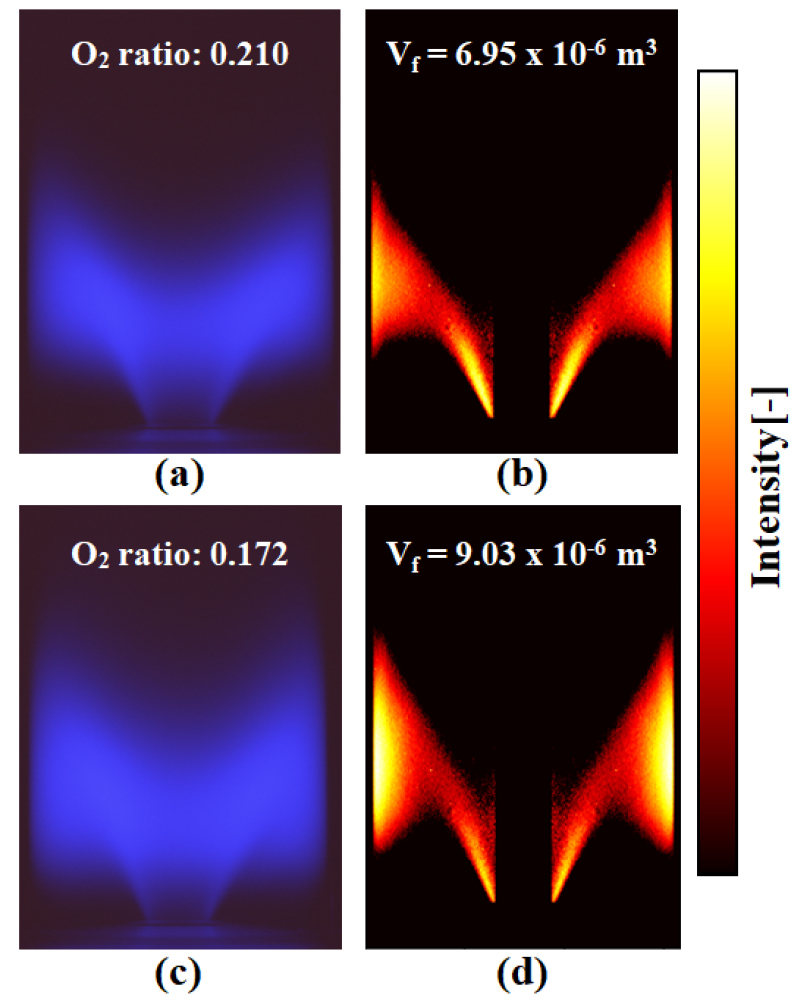
산화제 내 질소 분율이 증가함에 따라 연소 반응성이 저하되고 화염은 하류 방향으로 연장되었다. 강한 열방출 영역 역시 하류로 이동하여 석영 벽면에 보다 인접한 위치에서 형성되었다. 동시에 화염 체적이 확대되면서 체류시간이 증가하는 경향이 나타났다.
정량 분석 결과, 질소 분율 증가에 따라 화염 체적과 체류시간이 모두 증가하였으며, 이에 상응하여 NOx 농도도 증가하는 경향을 보였다(Fig. 7, 8). 이는 온도 변화가 크지 않은 조건에서 체류시간 증가가 NOx 생성에 누적적으로 기여했음을 의미한다. Fig. 7은 일정 유량 조건에서 기준 공기와 질소 분율 82.8% 조건의 CH* 자발광 영상과 역 아벨 변환 결과를 비교한 것이다. 분석 결과, 질소 분율 82.8% 조건에서 화염체적과 체류시간이 기준 대비 약 30% 증가한 것으로 나타났으며, 이는 NOx 증가 경향과 일치한다.
따라서 총 유량이 일정한 조건에서는 질소 분율 증가로 인한 반응 영역의 하류 이동과 화염 체적 확장이 체류시간을 연장시키며, 그 결과 NOx가 소폭 증가하는 것으로 해석된다.
4. 결 론
본 연구는 예혼합 메탄–공기 스월 화염에서 산화제 조성 제어를 통해 thermal NOx를 효과적으로 저감할 수 있음을 실험적으로 확인하였다. 실험 A(질소 유량 증가)에서는 열방출률을 일정하게 유지한 상태에서 산화제 유량 증가로 화염 온도가 감소하였고, 이에 따라 NOx 생성이 뚜렷하게 저감되었다. 실험 B(공기 유량 증가)에서는 유량 증가로 인해 화염 온도가 감소하였으나, 산소와 질소가 동시에 증가함에 따라 초기에는 반응물 농도 증가 효과가 우세하여 NOx가 증가하였고, 이후 온도 저하 효과가 지배적으로 작용하면서 감소하는 비단조적 거동을 보였다. 반면, 총 산화제 유량을 일정하게 유지하고 질소 분율만 증가시킨 실험 C에서는 화염 온도 변화가 미미하였으나, 반응 영역이 하류로 이동하고 화염 체적과 체류시간이 증가함에 따라 NOx가 소폭 증가하였다. 이러한 결과는 질소 희석 효과가 단순한 온도 저감뿐 아니라, 반응 영역 위치와 화염 구조 변화를 통해 NOx 생성 특성에 복합적으로 영향을 미침을 보여준다.