1. 서 론
비료는 현대 농업에서 생산물 품질 향상과 작물 생산성 증대에 필수적이다[1]. 산업적으로 비료의 주요 원료인 질산(HNO3)은 주로 암모니아(NH3)를 촉매적으로 산화하여 NO를 생성한 뒤, NO를 NO2로 전환하고 물에 흡수시키는 Ostwald 공정을 통해 생산된다[2]. 이때 질산 생산에 필요한 암모니아는 대부분 Haber–Bosch 공정을 기반으로 제조되는데, 암모니아 생산은 에너지 시스템 CO2 배출의 약 1–2%를 차지하는 것으로 보고되고 있어 지속 가능한 대안 공정이 요구된다[3]. 이러한 배경에서, 최근 플라즈마 기반 질소산화물 생산이 주목받고 있다. 플라즈마 공정은 재생전력과 직접 연계 가능한 전기화 공정으로서, 화석연료 연소에 따른 CO2 배출을 크게 줄일 수 있다. 또한 공정이 모듈형으로 구현될 수 있어 농작물 생산지 인근에 분산 설치가 가능하며, 이에 따라 비료의 장거리 운송과 중앙집중형 생산시설에 대한 의존도를 낮출 수 있다[4]. 나아가 기존의 Haber–Bosch 및 Ostwald 공정으로 이어지는 2단계 경로와 달리, 공기에서 NOx를 직접 생성한 뒤 수상 흡수 공정을 통해 질산으로 전환할 수 있어 공정 단계를 단순화할 수 있다.
최근 유전체장벽방전(DBD), 글로우 방전, 코로나 방전과 같은 비열 플라즈마와, 마이크로웨이브 플라즈마, 아크 및 스파크 방전과 같은 열플라즈마 등 다양한 플라즈마를 활용한 질소산화물 합성 연구가 진행되고 있다. 이 중에서도 열플라즈마는 비열 플라즈마 대비 에너지 코스트가 대체로 낮다고 보고되었는데[5], 이는 고온 환경을 조성함으로써 열적 NO 생성 경로(즉, Zeldovich 반응)가 활성화될 수 있기 때문으로 추측된다. 이에 따라 최근 열플라즈마를 활용한 질소산화물 합성 연구에 대한 관심이 증가하고 있다.
열플라즈마 기반 질소산화물 공정의 수율, 에너지 효율, 그리고 생성물 선택성은 반응기 내 고온 유동의 온도와 냉각 과정에 의해 크게 좌우된다. 따라서 공정 최적화를 위해서는 실험과 더불어 시뮬레이션 기반의 화학반응 분석이 필수적이며, 이를 위해 상세 반응 메커니즘과 플라즈마 고온 유동의 냉각 과정을 반영한 모델의 개발이 함께 요구된다. 그러나 현재 열플라즈마 질소산화물 합성 연구에서 사용되는 반응 메커니즘은 연구자의 경험을 바탕으로 kinetic database 내의 화학반응들을 수작업으로 조합하여 생성하는 경우가 많았다. 열플라즈마는 초고온 영역에서 저온 영역까지 넓은 온도 범위를 포함하므로, 온도에 따라 주요 화학종과 반응 경로가 달라진다. 이를 일관된 기준 없이 수동으로 구성하게 되면, 중요한 반응 경로의 누락으로 이어질 수 있으며, 이는 결과의 재현성과 신뢰성을 저하시킬 수 있다. 이를 극복하기 위해, 명확한 생성 기준에 따라 주요 화학종과 반응을 체계적으로 선별하는 자동 메커니즘 생성 도구의 활용이 필요하다. Reaction Mechanism Generator(RMG)는 MIT의 Green Group에서 개발된 오픈소스 기반의 자동 메커니즘 생성 도구로[6], 주어진 온도·압력·조성 조건에서 반응 계열(reaction family)과 kinetic/thermodynamic 데이터베이스를 바탕으로 주요 화학종과 반응을 체계적으로 탐색하여 상세 화학반응 메커니즘을 생성한다. 생성 과정에서 RMG는 주어진 화학종 구성에 대해 생성 가능한 화학종과 반응들을 반응속도(중요도)에 기초해 반복적으로 탐색하여 메커니즘에 포함시키므로, 연구자 경험에 기초하지 않는 자동화된 메커니즘 생성이 가능하다.
본 연구에서는 기존의 수작업 중심 메커니즘 구축의 한계를 극복하기 위해, RMG를 이용하여 고온 조건의 NOx 합성 해석에 적합한 상세 메커니즘을 생성하였다. 생성된 상세 반응 메커니즘의 검증은 선행 연구[5]에서 수행된 대기압 마이크로웨이브 열플라즈마 NOx 합성 실험에 대한 반응기 네트워크 시뮬레이션을 재수행하여 실험 결과와의 비교를 통해 달성하였다. 추가적으로, 선행 연구[5]의 해석 결과와 비교하고, 반응 경로 분석을 통해 NOx 생성 메커니즘의 주요 반응 경로를 규명하였다.
2. 방법론
2.1 RMG의 메커니즘 생성 방식
RMG에 대한 자세한 설명은 Gao 등[6]의 연구에 제시되어 있으므로, 여기서는 관련 내용을 간략히 소개한다. RMG는 Susnow의 rate-based algorithm[7]을 통해 모델을 점진적으로 확장한다. 여기서 core는 최종 메커니즘에 포함되는 화학종과 반응으로 구성된 영역이며, edge는 RMG가 고려할 후보 화학종과 반응들이 존재하는 영역을 의미한다. 온도·압력 조건에 대해 초기 화학종과 반응 계열(reaction family)들을 통해 발생 가능한 기초 반응들(elementary reactions)이 반응에 참여할 화학종과 함께 edge에 포함된다. 반응 계열은 반응 부위(reaction site)에 대한 템플릿과, 반응물이 생성물로 전환될 때 결합이 어떻게 변화하는지를 규정하는 반응 레시피(reaction recipe)로 구성된다. 이때 각 반응 계열에는 반응 속도 추정을 위한 계층 트리가 포함되어 있으며, RMG는 rate rules에 기초하여 반응 속도를 추정한다. 계층 트리 내 반응 정보는 상위 노드로 갈수록 일반화되고 하위 노드로 갈수록 세분화되는데, RMG의 rate rules는 반응 정보가 가장 일치하는 노드를 찾을 때까지 하위 트리를 탐색한다. 직접 일치하는 반응이 존재하면 해당 반응 속도 상수를 사용하고, 직접 일치하는 반응이 없으면 가장 가까운 상위 노드에 속한 반응들의 반응 속도를 평균하여 반응 속도를 추정한다. 이러한 속도 추정 방식을 바탕으로, edge의 화학종 𝑖의 플럭스 Ri=dCi/dt가 ϵRchar을 초과하면 해당 화학종이 core로 포함되며, 이에 따라 관련 반응들도 core에 포함된다. 여기서 Ci는 화학종 i의 농도, ϵ은 사용자가 정의한 허용오차이며, Rchar는 core에 있는 화학종 flux의 제곱평균제곱근(Root mean square)을 나타낸다. 이후 RMG는 해당 과정을 반복하며 모델을 확장하며, 사용자가 정의한 조건에서 더 이상 edge의 화학종이 core로 이동하지 않는다면, 모델 생성은 종료된다. 한편, 반응 계열을 통해 다수의 반응이 생성되는 과정에서 열역학적 물성이 알려지지 않은 화학종이 포함될 수 있다. 이 경우 RMG는 기본적으로 Benson의 그룹 가산성(group additivity) 방법을 이용하여 해당 화학종의 열역학적 파라미터를 추정한다[8]. 이 방법은 양자 화학 계산에 비해 정확도는 낮을 수 있으나 계산 비용이 매우 작아, RMG 내에서 기본 추정 방법으로 사용된다. 참고로, RMG가 추정한 열역학적 파라미터 또는 속도 상수의 신뢰성이 낮은 경우에는 문헌값 또는 양자 화학 계산 결과를 기반으로 해당 값을 보완하고, 이를 반영시켜 메커니즘 생성을 재수행할 수 있다.
2.2 모델 생성 입력 조건
본 연구의 메커니즘 생성 모델은 RMG-Py(version 3.3.0)와 RMG-database(version 3.3.0)[9]를 사용하였다. Kang et al 연구[5]는 대기압 마이크로웨이브 플라즈마 반응 과정을 고려한 화학 반응기 네트워크 시뮬레이션을 사용해 NOx 합성이 플라즈마 유동의 온도가 6000 K부터 1880 K 사이인 구간에서 대부분 발생함을 확인하였다. 따라서, 이를 고려해 반응 메커니즘은 압력은 1 bar, 온도는 각각 5000, 4000, 3000, 2000 K를 갖는 4개의 등온, 등압 반응 해석에 함께 적용 가능한 메커니즘으로 생성될 수 있도록 하였다. 한편, RMG는 추정한 열역학적 물성치를 NASA polynomial로 표현하여 계산하며, 열역학 데이터의 최대 온도는 현재 5000 K까지 고려한다. 역반응 속도 계산에 필요한 평형상수는 화학종의 열역학적 물성치를 기반으로 산정되므로, 5000 K를 초과하는 온도에서는 메커니즘 생성 계산을 수행할 수 없다. 이에 따라 본 연구에서는 메커니즘 생성의 상한 온도를 5000 K로 설정하였다. 초기 화학종은 각각 질소, 산소, 아르곤(압력 의존 반응을 위한 불활성 기체)으로 설정하고, 질소, 산소, 그리고 아르곤 몰분율은 각각 0.05, 0.05, 그리고 0.90(즉, 질소-산소 혼합물 10%와 불활성 기체 90%)로 설정하였다.
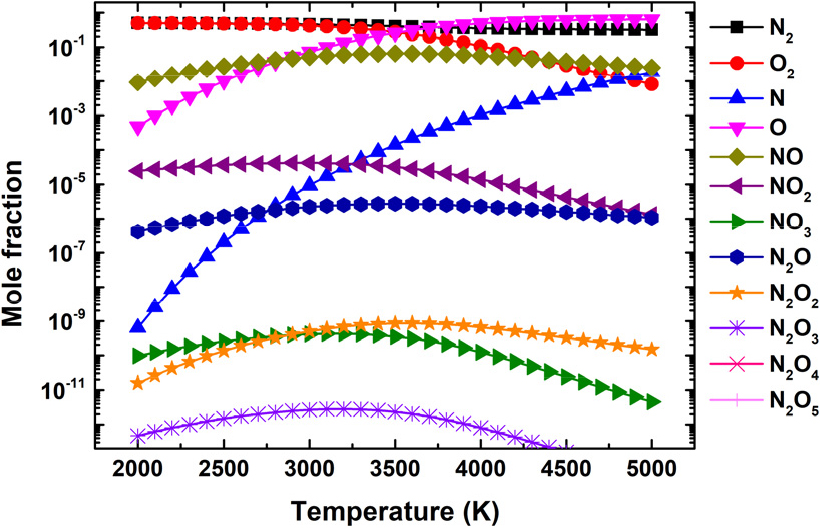
추가적으로, RMG에서는 메커니즘이 불필요하게 확장되는 것을 막기 위해 제약 조건을 설정할 수 있다. 제약 조건을 확인하기 위해, N2:O2 비율은 5:5 조건으로 NxOy (0≤x≤2, 0≤y≤5) 화학종들을 2000 K부터 5000 K까지 Cantera(ver 3.2.0)[10]를 이용하여 대기압 하에서 열역학적 평형 계산을 수행하였으며, 결과를 Fig. 1에 나타내었다. 해당 온도 범위에서 N2O2, N2O3, N2O4, N2O5의 몰분율은 약 10-10 이하로 고온에서 안정하게 존재하기 어려움을 보여준다. 이에 따라, 본 연구에서는 최대 질소 원자수와 최대 산소 원자수를 각각 2로 설정하여 NxOy (0≤x≤2, 0≤y≤2)인 화학종만 메커니즘에 포함될 수 있도록 고려하였고, NOx 형성 반응에 중요한 질소 원자 라디칼(N)은 홑전자(unpaired electrons)가 3개이므로 maximum radical electrons를 3으로 설정하였다. 위 설정은 화학반응을 통해 생성 파괴될 수 있는 N 원자 2개 이하, O 원자 2개 이하로 구성되면서 최대 다중도(multiplicity) 4 이하인 모든 화학종을 메커니즘에 포함하도록 하며, 생성된 화학종은 중성종 뿐 아니라 전자여기종을 모두 포함한다. 모델의 tolerance는 0.05로 설정하였고, 이는 RMG에서 권장하는 수치 범위인 0.01~0.05 내에 해당한다[11].
Thermodynamic library로는 RMG 내장 library인 primaryThermoLibrary와 함께 본 연구를 위해 구축한 NOx-thermo를 사용하였다. NOx-thermo는 NxOy (0≤x≤2, 0≤y≤5) 화학종들로 구성되어 있으며, 화학종들의 NASA 7-coefficient polynomials는 Burcat’s thermodynamic data[12]와 RMG-database를 참고하여 최대 온도 범위 6000 K까지 적용 가능한 데이터들로 구성하였다. Seed mechanism은 사용하지 않았으며, Reaction library는 RMG-database의 GRI-Mech3.0-N과 NOx-2018을 사용하였다. 이에 더해, 5000 K 이상의 초고온 영역에서는 질소–산소 혼합물이 상당한 수준으로 N과 O 원자종으로 해리된다. 이에 따라 우주선의 대기권 진입 시 형성되는 초고온 공기 환경에 대한 화학반응 해석 모델을 제시한 C. Park의 연구[13]를 참고하여, 해당 모델의 반응들 중 3개의 삼체 해리/재결합 반응(N2 + M ↔ N + N + M, O2 + M ↔ O + O + M, NO + M ↔ N + O + M)을 reaction library에 추가하였다.
마지막으로, 압력 의존 반응들의 영향을 평가하기 위해 모델에는 압력 의존 반응기가 포함되었다. 압력 의존 반응 계산에서는 modified strong collision 근사로 마스터 방정식을 풀어 온도·압력 의존 반응 속도 상수이 산출된다[14]. 압력 의존 반응은 300 K에서 5000 K까지 8개의 구간, 0.01 bar에서 100 bar까지 6개의 구간에서 계산되었고, 계산된 반응 속도는 6개의 온도, 4개의 압력 포인트에서 보간되어 Chebychev 다항식으로 표현되었다. 생성된 메커니즘은 최종 yaml 형식으로 저장되었다.
3. 연구 결과 및 고찰
메커니즘 생성시 충돌 한계 위반(collision limit violation)은 발생하지 않았으며, 최종 메커니즘은 33개의 화학종(Ar, He, Ne, N2 2종 O2 2종, N 1종, O 2종, NO 2종, NO2 4종, N2O 4종, NO3 1종, N2O2 12종)과 292개의 반응(반응 라이브러리에서 포함된 삼체반응 4개, 기초반응 12개, 압력 의존 반응 계산으로 생성된 276개 반응)으로 구성되며, 부록의 웹 저장소에 제공하였다. 해당 메커니즘은 Kang et al. 연구[5]에서 수행된 대기압 마이크로웨이브 열플라즈마 기반 NOx 합성 결과에 대해 검증하였으며, 구체적으로, 반응기 후단(Surfaguide로부터 하류 61 cm)에서 포집·측정한 FT-IR 실험 결과를 생성한 반응 메커니즘을 입력으로 하는 반응기 네트워크 모델의 해석 결과와 비교함으로써 달성되었다. 마이크로웨이브 플라즈마는 Fig. 2와 같이 국소적으로 형성된 플라즈마가 주변 흐름과 혼합되면서 반응이 진행된다. 이에 따라 반응기 네트워크 모델은 Python 기반 Cantera(ver 3.2.0)를 사용하였으며, 반응기 내 플라즈마 유동의 점진적 냉각 과정을 모사하기 위해 플라즈마 흐름, 중간 흐름, 우회 흐름의 세 영역으로 구분하였고, 플라즈마 흐름은 원통형, 중간 및 우회 흐름은 중공 원통형으로 설정하였다. 각 흐름은 높이 2 cm의 연속교반반응기(CSTR, continuous stirred tank reactor)들을 축방향으로 연결하여 표현하였고, 동일 높이의 흐름 계면에서는 확산에 의한 열 및 물질 전달이 일어나도록 설정하였다. 실험 조건과 동일하게 반응 해석은 FT-IR 측정 샘플링이 진행된 62 cm 하류까지 진행되었고, 전력은 1.5 kW로 고정하였으며, N2:O2 비율은 8:2에서 2:8까지, 유량은 20 slpm부터 50 slpm까지 달리하였다. 확산도와 방사율은 이전 연구에서 사용한 것과 동일한 값을 사용하였으며, 자세한 값은 선행 연구[5]에 나타나 있다.
Fig. 3(a)는 RMG로 생성한 상세 메커니즘을 사용해 계산한 NOx 농도를 FT-IR로 측정한 NOx 농도와 비교한 결과이고, Fig. 3(b)는 GRI-Mech3.0-N과 C. Park 메커니즘[13]을 조합한 메커니즘(선행 연구[5]의 메커니즘)을 사용해 계산한 NOx 농도를 FT-IR로 측정한 NOx 농도와 비교한 결과이다. Fig. 3(a)에서, 20 slpm에서 N2:O2 비율이 8:2에서 2:8로 변화할 때 NOx 농도는 2.37%, 2.92%, 2.93%, 2.80%, 2.14%로 나타났으며, 50 slpm에서는 0.99%, 1.22%, 1.18%, 1.10%, 0.80%로 나타났다. 최대 NOx 농도는 N2:O2 = 6:4 및 5:5 조건에서 나타났고, 8:2 및 2:8 조건에서는 감소하는 경향을 보였다. 또한 유량이 증가할수록 NOx 농도는 감소하였으며, 이는 실험 결과와 일치한다. 선행 연구[5]의 메커니즘과 RMG 생성 메커니즘의 계산 결과 차이는 모든 조건에서 최대 약 0.04 vol%로, 더 많은 반응을 포함함에도 예측 결과는 거의 동일하였다. 한편, 실험값과 시뮬레이션 간 차이는 유량이 증가할수록 커졌다. 이는 반응 경로의 누락보다는, 반응기 네트워크를 3개 영역으로 구성하였음에도 모델 단순화로 인해 고온 플라즈마 유동의 냉각 과정을 온전히 반영하지 못했기 때문으로 판단된다.
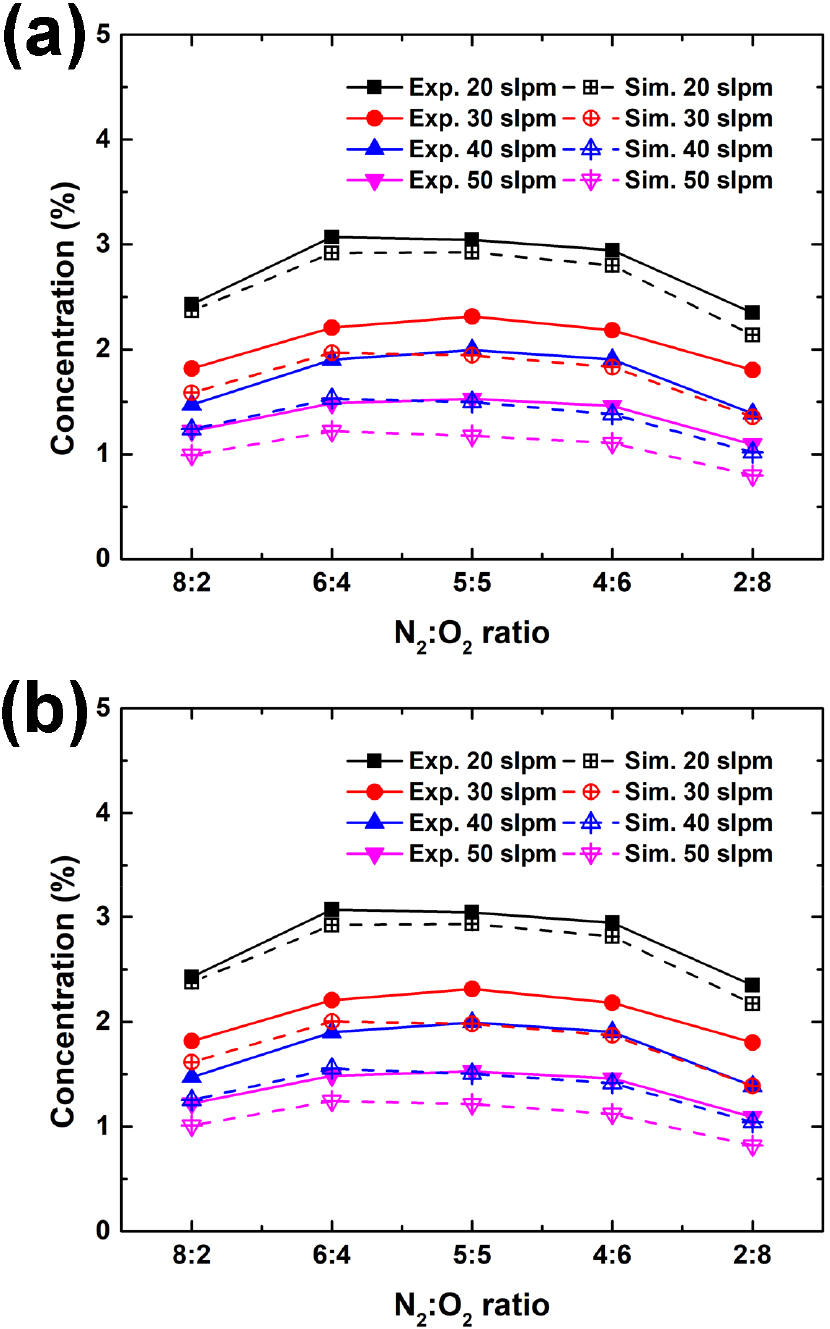
Fig. 3.
Comparison of calculated and measured NOx mole fractions at 0.61 m downstream from the Surfaguide for N2–O2 mixtures with N2:O2 ratios varying from 8:2 to 2:8: (a) using the mechanism generated by RMG, and (b) using the mechanism from Kang et al.[5].
선행 연구[5]의 메커니즘보다 더 많은 반응 경로를 포함하는 본 연구의 메커니즘에서 세부 반응 과정을 확인하기 위해, 대기압 마이크로웨이브 열플라즈마 기반 NOx 합성에 대한 반응 경로 분석을 수행하였다. NOx 합성 반응은 대부분 20 cm에서 종료되었다. 따라서, 각 흐름의 CSTR 반응기의 높이는 2 cm이므로, 반응 경로 분석은 총 10개의 반응기의 반응 속도를 공간 적분하여 진행하였다. 이때, 플라즈마 흐름과 우회 흐름은 서로 다른 부피를 가지므로, 정량 비교를 위해 반응 속도는 서로 다른 부피 크기를 반영하여 식 (1)부터 (4)까지로 표현되었다.
여기서 Vp와 Vs1, Vs2는 각각 플라즈마 흐름과 중간 흐름, 우회 흐름을 구성하는 개별 CSTR 의 부피를 나타낸다. 각각 j는 반응기 순번, m은 반응 순번, Ai는 화학종 i의 몰농도, νi와 νi'는 각각 화학종 i에 대한 반응물과 생성물의 화학양론 계수, N은 전체 화학종의 수를 나타낸다. 우회 흐름 전체의 반응 속도는 중간 흐름과 우회 흐름의 흐름별 반응 속도를 합산하여 계산하였다.
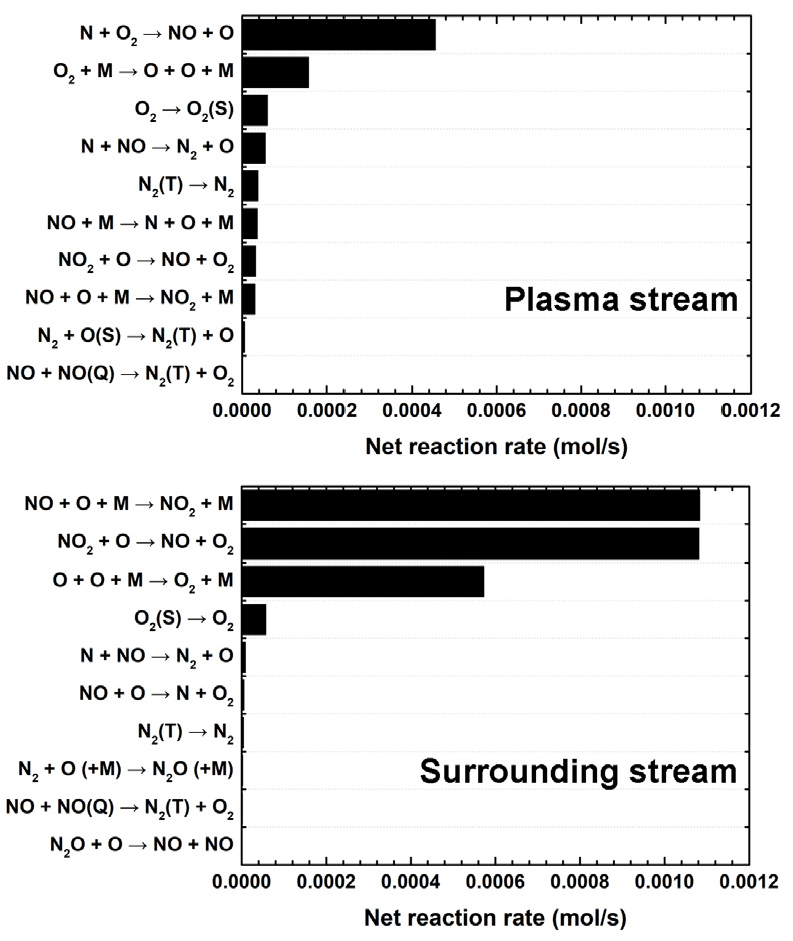
전력 1.5 kW, 유량 20 slpm, N2:O2 = 5:5 조건에서 플라즈마 흐름과 우회 흐름 영역의 주요 반응 경로를 대표적인 예로 Fig. 4에 나타내었다. 수백 개의 반응을 모두 제시하기 어려우므로, 반응 속도가 가장 큰 상위 10개 반응만 나타내었다. 플라즈마 흐름에서는 젤도비치 반응이 가장 활성화되었다. NO는 N + O2 → NO + O 반응으로 생성되었으며, N + NO → N2 + O 반응으로 소멸되었다. 또한 높은 온도로 인해 O2와 NO의 삼체 해리반응(O2 + M → O + O + M, NO + M → N + O + M)이 나타났다. 추가적으로, 압력 의존 반응 계산으로 도출된 2개의 전자 여기종의 충돌 여기-완화 반응도 플라즈마 흐름에서 주요하게 나타났다. 플라즈마 코어에서 생성된 triplet N2(N2(T))는 플라즈마 흐름에서 충돌 완화를 통해 기저상태 N2로 전환된 반면, O2는 충돌 여기되어 singlet O2(O2(S))로 전환되었다. NIST Chemistry WebBook을 기반으로 계산한 O2(a1Δg)와 N2(A3Σu⁺)의 여기에너지가 각각 0.98 eV와 6.22 eV임을 고려하면[15], 플라즈마 흐름 조건에서 O2의 전자여기 상태가 N2(T)보다 상대적으로 더 쉽게 형성될 수 있음을 시사한다. 한편, 우회 흐름에서는 Zeldovich 반응의 기여는 미미했으며, NO + O + M → NO2 + M, NO2 + O → NO + O2, O + O + M → O2 + M과 같이 O 원자가 관여하는 반응이 가장 활성화되었다. 플라즈마 흐름에서 생성된 O 원자는 우회 흐름으로 확산되어 유입되며, 서로 결합하여 다시 O2를 형성하였다. 또한 O 원자는 NO와 반응하여 NO2를 생성하지만, NO2 + O 반응을 통해 다시 NO로 전환되었다. 이는 우회 흐름이 플라즈마 흐름보다 온도가 낮음에도 불구하고, 여전히 NO2가 안정적으로 존재하기 어려운 조건임을 보여준다. 추가적으로, 우회 흐름에서는 O2(S) → O2 반응이 나타났으며, 플라즈마 흐름에서 생성된 O2(S)는 우회 흐름으로 확산된 뒤 충돌 완화를 거쳐 대부분 기저상태 O2로 전환되었다. 이는 전자 여기종은 NOx 형성에 기여하기보다는 대부분 기저 상태로 전환됨을 보여준다. 전자 여기종 관련 반응을 제외하면, 주요 반응 경로들은 선행 연구[5]에서 제시된 경로들과 일치하였다. RMG로 생성한 메커니즘을 이용한 반응 경로 분석으로부터, 선행 연구[5]에서 사용된 메커니즘이 주요 반응들을 모두 포함하고 있고, 따라서 선행 연구[5]의 해석 결과가 본 연구의 해석 결과와 크게 다르지 않음을 확인하였다. 비록 전자 여기종의 여기–완화 경로가 존재하였으나, 본 실험 조건의 온도 범위에서는 해당 여기종이 NOx 생성에 미치는 영향이 크지 않았고 대부분 기저 종으로 전환되어 NOx 농도 예측에 대한 영향도 제한적인 것으로 나타났다.
4. 결 론
본 연구에서는 RMG를 이용하여 고온 환경 NOx 합성 해석에 적합한 상세 화학반응 메커니즘을 생성하고, 이를 선행 연구[5]의 실험 결과 및 시뮬레이션과 비교하여 분석하였다. 반응 메커니즘은 대기압 마이크로웨이브 플라즈마 반응기의 온도 범위를 고려하여 2000 K부터 5000 K까지의 넓은 온도 범위에서 생성하였으며, 압력 의존 반응기를 포함하여 압력 의존 반응의 영향도 함께 검토하였다. 최종 상세 메커니즘은 33개의 화학종과 292개의 반응으로 구성되었다. 생성된 메커니즘을 마이크로웨이브 플라즈마 반응기를 모사한 차원 축소 화학반응기 네트워크 모델에 적용하여 실험 결과와 비교한 결과, 실험과 시뮬레이션 모두에서 NOx 농도는 N2:O2 = 6:4 및 5:5 조건에서 최대값을 나타내었다. 한편, 유량이 증가할수록 시뮬레이션 예측값과 실험값의 편차가 증가하였는데, 이는 실제 고온 플라즈마 유동의 냉각 과정을 온전히 모사하지 못한 반응기 네트워크 모델의 단순화에 기인한 것으로 판단된다. 추가적으로, 플라즈마 흐름과 우회 흐름에서의 세부 반응 과정을 확인하기 위해 반응 경로 분석을 수행하였다. 플라즈마 흐름에서는 Zeldovich 반응을 통한 NO 생성 반응과 O2 및 NO의 해리 반응이 지배적으로 나타났다. 우회 흐름에서는 O2로의 재결합 반응과 NO + O + M → NO2 + M, NO2 + O → NO + O2 반응이 주요하게 나타났으며, 이들 반응 경로는 선행 연구[5]에서 제시된 주요 반응 경로와 일치하였다. 본 연구에서 생성한 반응 메커니즘은 향후 열플라즈마 기반 질소산화물 합성 해석에 유효하게 적용될 수 있음을 확인하였다.