1. 서 론
2. 상세화학반응모델
2.1. 상세화학반응모델 개발
2.2. 상세화학반응모델 검증
3. 결과 및 고찰
3.1. H2/CO 예혼합화염에서 NO 형성
3.2. NO 형성에 대한 압력 영향
4. 결 론
1. 서 론
최근 엄격한 배출 규제로 인해 대체연료와 새로운 연소기술 등에 관한 관심이 높아졌다. 대기 오염물질 배출 저감을 위한 대체연료 또는 연료 첨가제로 함산소계 연료에 관한 연구가 활발하게 진행 중이다[1]. 오염물질 배출 제어를 위해 화석 연료의 연소로 발생하는 주요 오염물질로 대기 중 광화학 스모그를 발생시키거나 오존층 파괴에 기여하는 것으로 알려진 매연 및 질소 산화물(NOx) 등의 생성 특성에 관한 연구 또한 매우 활발하다. 따라서 이러한 오염물질 배출 제어는 현대 엔진 개발에 핵심 요소가 되었다. 대체연료에 관한 연구 이외에 최근 내연기관의 저온연소나 가스터빈 연소기 내 연료희박 예혼합연소 등과 같은 새로운 연소 기법에 관한 관심이 많이 증가하였다. 일례로 최근 Khdir 등[2]은 가스터빈의 NOx 및 CO 배출량을 줄이기 위하여 무화염(flameless) 연소와 관련한 연구를 진행하였다. 연료희박 예혼합화염은 고온 환경을 회피하여 연료 소모 및 NOx 생성을 줄이는 등의 장점이 있지만, 연소기 내 연소 불안정성을 유발하여 연소기 성능 저하 및 손상을 일으킬 수도 있다[3]. 일반적으로 가스터빈 연소기 내 확산화염이 예혼합화염보다 훨씬 많은 NO 생성을 한다고 알려져 있다[4].
최근 가스터빈 연소기의 연소 및 NOx 배출 특성을 파악하기 위하여 광범위한 연구가 활발하게 진행 중이다. Van 등[5]은 가스터빈 NOx 배출 저감을 위해 RML(Rich- burn/Mild/Lean-burn) 연소기의 타당성을 연구하였다. Lee 등[6]은 연소기 내 스윌유동 특성이 화염에 미치는 영향을 실험적으로 파악하였다. 또한, Kim 등[7]은 저온 플라즈마가 인가된 예혼합화염의 운전 영역 확장에 대한 실험을 수행하였다.
높은 효율과 낮은 NOx 배출 특성 등으로 주목받고 있는 석탄가스화 복합발전(IGCC, Integrated Gasfication Combined Cycle)은 가스터빈 연료의 다변화 및 친환경 석탄발전 미래기술로 상용화에 박차를 가하고 있다. IGCC에서 사용하는 합성가스는 수소와 일산화탄소를 주성분으로 하여 기존의 메탄이 주연료인 천연가스와 조성이 다르기 때문에 연소기 조건에서 H2/CO 혼합물의 연소 및 NO 생성 특성을 이해할 필요가 있다. 따라서 Lee 등[8]은 부분 예혼합연소기를 이용하여 합성가스의 연소 및 배출 특성을 살펴보았다. 또한, 최근 Kim과 Lee[9]는 연소 시스템에서 합성가스를 연료로 부상된 충돌 제트 화염의 연소 불안정성에 대한 특성을 파악하였다.
가스터빈 개발에 있어 연소기 내 화염 온도, 압력 및 체류 시간은 NOx 배출에 중요한 핵심 요소이다. 일반적으로 가스터빈의 NOx 배출은 대기압에서 측정된 데이터로부터 고압 조건의 배출을 예측하기 때문에 압력 변화에 따른 NO 생성 특성을 정확히 파악하는 것이 매우 중요하다. 따라서 본 연구는 상세화학반응모델을 이용하여 가스터빈 운전 조건에 해당하는 조건의 층류 예혼합화염을 분석하여 압력 변화에 따른 H2/CO 합성가스의 NO 배출 특성에 대한 이해를 도모하고자 한다.
2. 상세화학반응모델
2.1. 상세화학반응모델 개발
본 연구에서 사용된 상세화학반응모델은 C1-C4 탄화수소계 연료의 개선된 연소 해석을 위해 개발된 AramcoMech 3.0[10]을 기본 메커니즘으로 연료의 연소로 인해 생성되는 질소 산화물을 예측하기 위해서 Glaborg et al.[11]이 제안한 질소 산화물 생성과 관련한 반응식 부분을 추가하였다. AramcoMech 3.0 모델은 알칸계 C1-C4연료 및 주요한 중간 생성물(C2H4, C2H2, C3H6, iso-C4H8, 1,3-C4H6)의 점화지연시간, 화염전파속도, 반응기 내 화학종 몰분율 등 광범위한 실험 데이터와 비교 검증되었으며 단순한 변경을 통해 다양한 연료를 추가할 수 있다. 본 연구에 적용된 질소산화물 생성 메커니즘은 질소와 관련된 화학종들의 열화학 정보뿐만 아니라 정확한 NO 생성을 예측하기 위한 주요 반응들의 반응 상수들이 업데이트되었으며 수정없이 기본 메커니즘에 추가되었다. 본 연구가 제안한 모델은 총 663종의 화학종과 3798개의 반응을 포함한다. 본 메커니즘은 메탄/공기 혼합물의 화염전파, 점화지연과 같은 기본적인 연소 특성 및 예혼합화염의 NO 생성 특성과 관련하여 다양한 조건의 실험과 비교되었으며 합리적으로 실험 결과를 예측하였다[12].
2.2. 상세화학반응모델 검증
압력 변화에 따른 H2/CO 예혼합화염의 NO 생성 특성을 논의하기 전에 H2/CO 혼합물의 층류화염전파속도, 점화지연 시간 및 압력에 따른 LCVG(Low Calorific Value Gas) 예혼합화염의 NO 생성 결과와 비교하여 메커니즘 유효성을 검증하였다. 본 연구에서 H2/CO 혼합물의 연소 특성에 관한 모든 시뮬레이션은 CHEMKIN-PRO [13]를 사용하여 수행하였다.
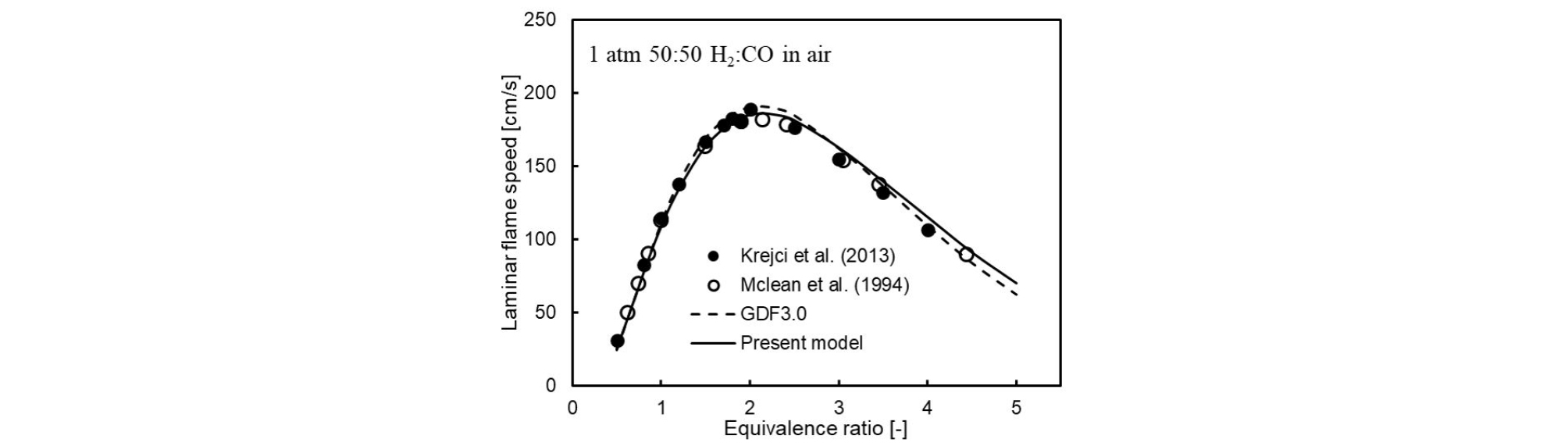
H2/CO 혼합물의 층류화염전파속도와 계산 결과와의 비교를 Fig. 1에 나타내었다. 층류화염전파속도 계산은 CHEMKIN-PRO PREMIX 코드를 사용하였으며 미연가스 조건은 1 atm, 300K로 실험 데이터[14], [15]와 비교하였다. H2/CO 혼합물은 탄화수소계 연료와 달리 수소의 화염전파 특성과 유사한 결과를 보였다. 비교를 위해 사용된 GDF 3.0 메커니즘[16]과 본 연구가 제시한 메커니즘 모두 최대 화염전파속도 및 당량비(Φ)에 따른 화염전파 특성을 정확히 예측하였다. 압력 상승에 대한 화염전파 특성을 살펴보기 위하여 5, 10 atm에서 측정된 H2/ CO/O2/HE 혼합물의 화염전파속도를 시뮬레이션하여 Fig. 2에 비교하였다. 압력이 증가함에 따라 H2/CO 혼합물의 화염전파속도는 감소하는데 현재 메커니즘은 실험적으로 관찰된 경향 및 각 압력에서 최대 화염전파속도를 정확히 예측하였다. 하지만 연료과잉 영역에서 화염전파속도를 조금 과하게 예측하는 것을 확인할 수 있었다.
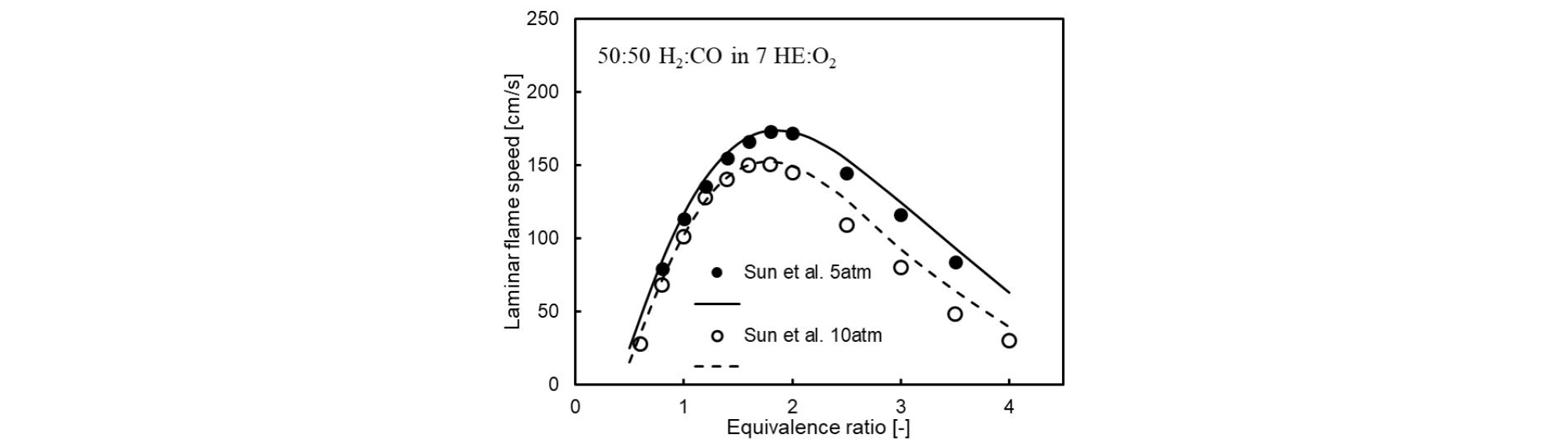
Fig. 2.
Laminar flame speeds of 50/50 H2/CO in 1/7 O2/HE at unburnt temperature of 300 K and different pressures. Calculations (lines) are compared with experimental data (symbols) from Ref[17].
현재 모델이 다양한 압력 조건에서 H2/CO의 기본적인 연소 특성을 정확하게 예측하는지 확인하기 위해 Keromnes 등[18]이 shocktube를 이용해 측정한 H2/CO/ O2/Ar 혼합물의 점화지연 특성을 Fig. 3에 비교하여 나타내었다. 혼합물의 당량비(Φ)는 0.5이며 1, 4, 16 atm에서 측정된 점화 지연시간을 CHEMKIN-PRO Homogeneous Batch Reactor를 이용하여 시뮬레이션하였다. 저온 영역에서 점화지연 시간은 압력 상승에 따라 증가하나 온도가 상승함에 따라 이러한 경향이 역전되는 특징을 보이며 현재 모델은 계산된 압력 및 온도 구간에서 H2/CO 혼합물의 점화지연시간을 합리적으로 잘 예측하였다. 하지만 GDF 3.0 메커니즘은 고압 조건에서 상당한 오차를 보여 현재 모델이 다양한 압력 조건에서 H2/CO 혼합물의 연소 특성을 해석하는데 적당하다고 판단된다.
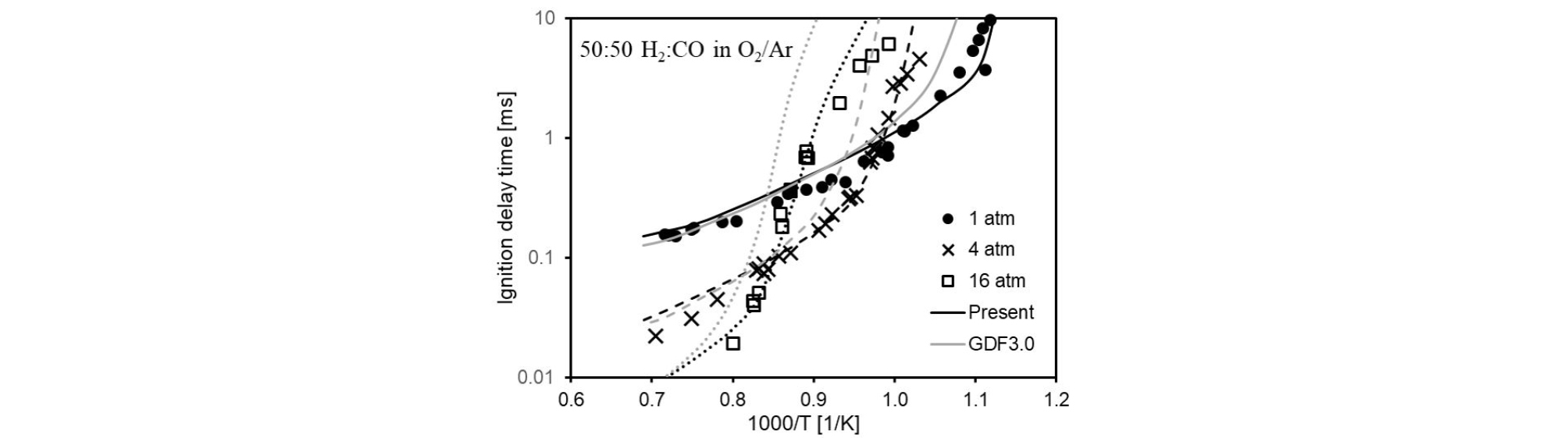
Fig. 3.
Ignition delay times of 50/50 H2/CO at various pressures. Calculations (lines) are compared with experimental data (symbols) from Ref[18].
추가로 메커니즘의 NO 예측 능력을 파악하기 위해 다양한 압력 조건에서 메탄과 LCVG 혼합물의 예혼합화염을 계산하였다. 연료는 메탄이 2.8%를 차지하며 LCVG는 0.212/0.175/0.122/0.491 CO/H2/CO2/N2로 구성되어 있다. Fig. 4는 당량비(Φ) 0.8인 예혼합화염의 축방향 길이에 대한 NO 몰분율을 나타낸 것으로 1, 9.15 atm의 실험 데이터와 비교하였다. 계산은 실험에 사용된 입력 조건을 사용하여 CHEMKIN-PRO의 Burner stabilized flame code의 에너지 방정식을 푸는 방법으로 수행하였다. 화염의 최대 온도는 1, 9.15 atm에서 각각 1685, 1705 K이다. 현재 메커니즘은 버너 축방향 길이에 대해 다른 압력 조건에서 화염의 NO 몰분율을 합리적으로 예측하였으나 GDF 3.0 메커니즘의 경우 대기압 조건의 화염에 비해 고압에서 NO 몰분율을 과대 예측하였다. 따라서 압력 변화에 따른 H2/CO 예혼합화염의 NO 생성 특성을 연구하는 데 있어 본 연구가 제시한 메커니즘이 알맞다고 판단된다.
3. 결과 및 고찰
3.1. H2/CO 예혼합화염에서 NO 형성
가스터빈 NOx 배출에 있어 화염 온도, 압력 및 연소기 내 체류시간은 영향이 매우 큰 인자로 압력 변화에 의한 NOx 생성 특성을 이해하는 것은 고압 조건에서 NOx 배출을 예측하는 데 필수적이다. 따라서 석탄가스화 복합발전(IGCC)과 관련하여 합성가스를 사용하는 산업용 가스터빈 연소기의 NOx 배출에 대한 압력 효과를 파악하기 위해 가스터빈 연소기의 운전 조건과 유사한 환경(1890~1990 K, 1~20 atm)에서 자유롭게 전파하는 H2/CO 혼합물의 층류 예혼합화염의 NO 생성 특성을 분석하였다. 연료인 합성가스는 50%의 H2와 50%의 CO를 포함하며 미연가스 온도는 673 K로 1, 5, 10, 15, 20 기압에서 당량비(Φ) 0.45와 0.5 조건으로 CHEMKIN-PRO의 PREMIX code를 사용하여 계산하였다.
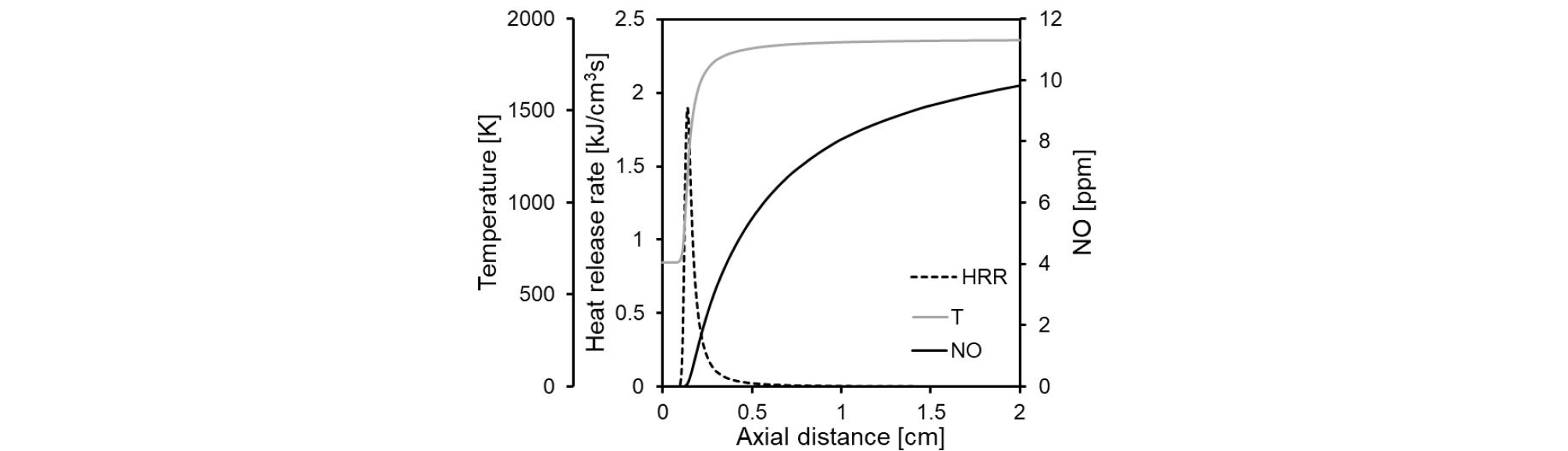
Fig. 5는 H2/CO/air 예혼합화염(Φ=0.45)의 화염 온도, 열방출율 및 NO 몰분율을 나타낸다. NO는 반응지역에서 형성을 시작하여 화염 후류로 갈수록 선형에 가깝게 증가하는 것을 볼 수 있다. 일반적으로 NO는 주로 다음의 네가지 메커니즘을 통해 생성된다.
(1) Zeldovich NO 생성 메커니즘은 고온 가스 연소에서 중요한 NO 생성 경로로 N2와 O원자와 반응(N2 + O = NO + N)으로 시작되며 질소 원자는 OH 또는 O2와의 반응(N + OH/O2 = NO + H/O)으로 NO를 형성한다.
(2) Prompt NO는 CH 라디칼과 N2와의 반응을 기점으로 형성되며 본 연구가 사용한 메커니즘은 Moskaleva 등 [20]이 제안한 NCN 생성 경로(CH + N2 = NCN + H, NCN + O = NO + CN))를 포함하고 있다.
(3) NO는 N2와 O 라디칼의 결합으로 형성된 N2O와 O/H 라디칼의 반응(N2O + O/H = NO +NO/NH)을 통해 생성될 수 있다.
(4) N2와 H 라디칼의 결합으로 형성된 NNH와 O 라디칼의 반응(NNH + O = NO + NH)을 통해 NO가 형성된다. N2O 메커니즘의 경우 고압 조건의 연료희박 화염에서 NO 생성에 중요한 역할을 할 수 있으며 NNH 메커니즘은 확산화염에서 중요성이 강조된다고 알려져 있다.
3.2. NO 형성에 대한 압력 영향
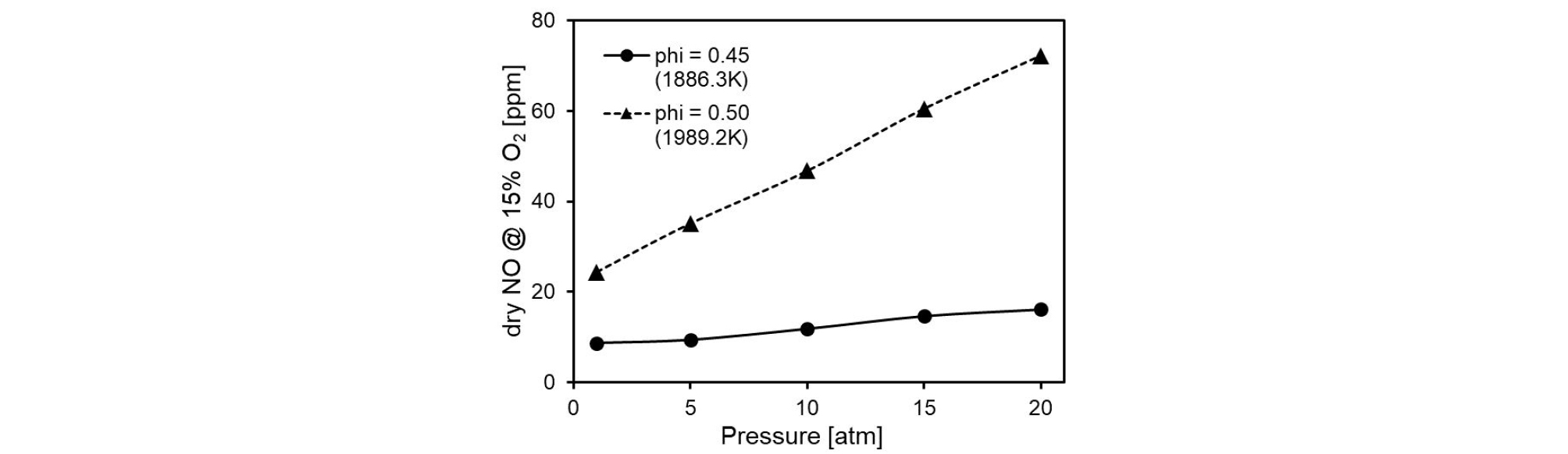
Fig. 6은 다양한 압력 조건에서 H2/CO 예혼합화염의 NO 생성 특성을 비교하기 위하여 각각의 압력 조건에서 화염의 체류시간(20 ms)이 동일할 때 15% dry O2 조건의 NO 몰분율을 비교하였다. 비교한 화염의 최고 온도는 당량비(Φ)가 0.45, 0.5일 때 각각 약 1886.3, 1989.2 K이다. 가스터빈 연소기 내 연소가스의 체류시간은 대략 20 ms로 알려져 있으며 자유 전파 화염의 체류시간은 축방향 길이와 속도를 이용하여 계산하였다. 각 압력 조건의 화염을 효과적으로 비교하기 위해 열방출율이 최대인 지점을 체류시간 1 ms로 지정하였다. 계산 결과 동일한 당량비를 가진 화염은 압력증가에 따라 생성되는 NO 몰분율이 증가하는 경향이 관찰되었다. 또한 화염의 온도가 높아짐에 따라 압력 증가에 따른 NO 증가폭이 현저하게 늘어나는 것을 볼 수 있다. 이러한 결과를 통해 H2/CO 예혼합화염의 NO 생성은 가스터빈 운전 조건에서 양의 압력 의존성을 갖는 것으로 판단된다.
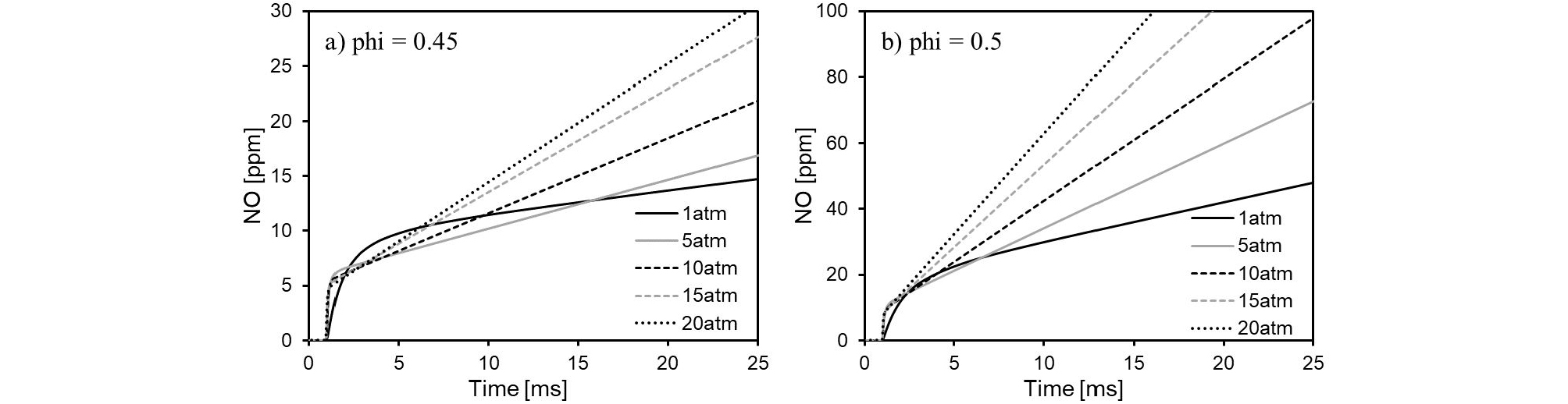
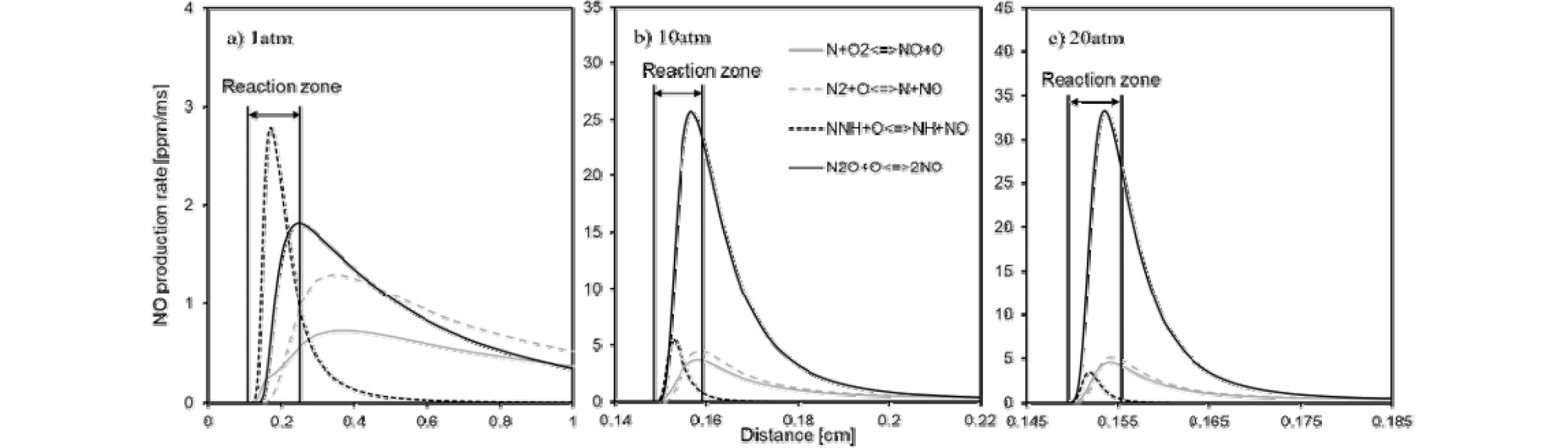
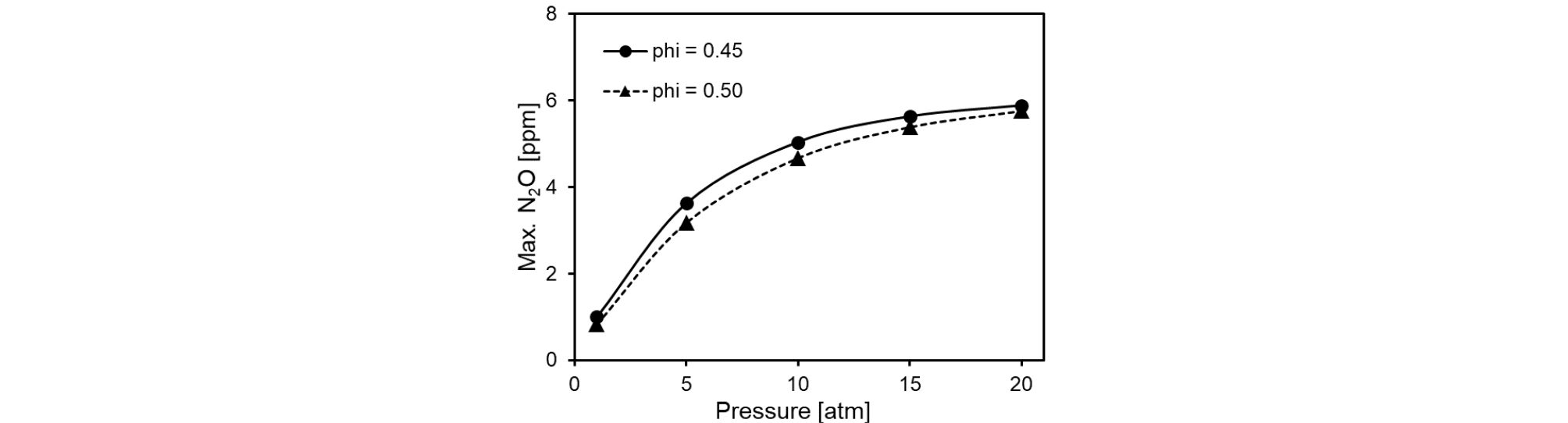
NO 형성에 대한 압력 효과를 보다 자세하게 파악하기 위하여 시간에 대한 NO 몰분율 변화를 Fig. 7에 나타내었다. 그 결과 당량비(Φ)에 관계없이 5~20기압의 압력 범위에서 화염 후류의 NO 농도 증가폭은 압력 증가에 비례하나 열방출율이 최대인 지점으로 반응영역인 1 ms 부근에서 생성된 NO 농도는 압력 증가에 반비례 특성을 보인 메탄/공기 화염과 다르게 압력증가에도 큰 차이가 없는 것으로 보인다. 압력 변화에 따라 반응영역에서 형성되는 NO의 생성 경로 특성을 확인하기 위하여 앞서 언급한 주요한 NO 메커니즘의 생성률을 Fig. 8에 나타내었다. 반응영역에서 NNH 메커니즘을 통해 NO 생성이 시작되며 압력이 증가함에 따라 반응영역과 화염 후류지역 사이에서 N2O 메커니즘을 통한 NO 생성이 두드러지게 증가하는 것을 볼 수 있다. CH 라디칼의 부재로 인해 반응영역에서 prompt NO 생성 경로를 통한 NO 생성은 나타나지 않았다. Fig. 9는 압력증가에 따른 N2O의 최대 몰분율 변화를 나타내었다. N2와 O 라디칼의 결합으로 형성된 N2O는 반응영역 내 열방출이 종료되는 지점 부근에서 최대 생성율을 보인다. 하지만 반응영역 내 압력변화에 민감하지 않은 다른 경로를 통한 NO 생성률과 압력 증가로 인해 좁아지는 반응영역으로 인하여 Fig. 7과 같이 반응영역 내 생성되는 총 NO 농도는 10~20 atm 압력 범위에서 큰 변화가 없는 것으로 나타났다.
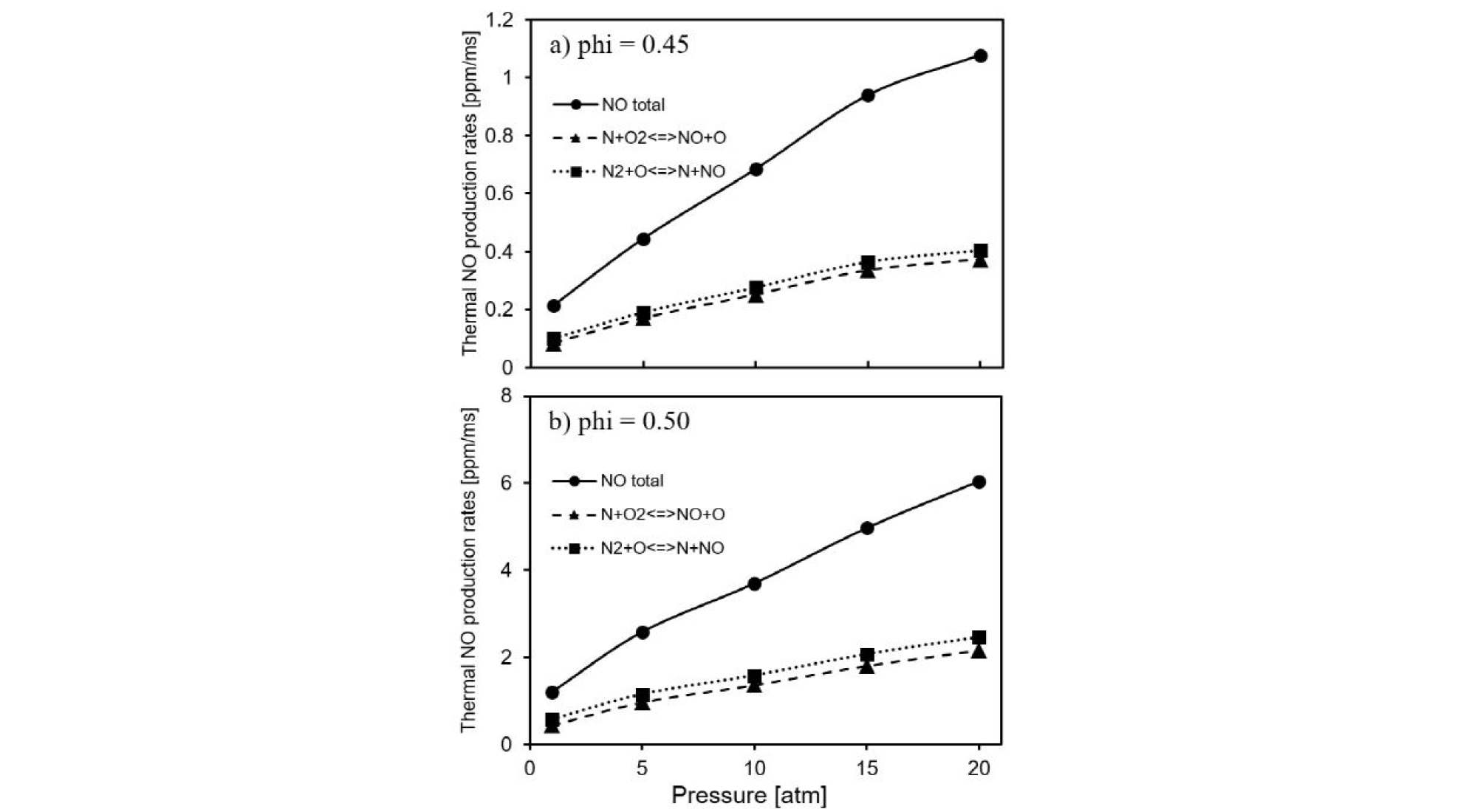
기존의 메탄/공기 화염의 연구 결과[12] 연료희박 화염의 경우 화염 후류지역인 고온 영역에서 NO 생성은 압력 증가에 양의 의존성을 보이며 Zeldovich 메커니즘이 NO 생성을 주도하였다. 따라서 화염 후류지역에서 압력 증가에 따른 H2/CO 예혼합화염의 NO 생성 특성을 파악하기 위하여 체류시간 20ms일 때 전체 NO 생성률과 Zeldovich 메커니즘(Thermal NOx)에 의한 NO 생성률을 Fig. 10에 나타내었다. 체류시간 20ms에 해당하는 지역은 화염의 후류로 이 때 온도는 화염의 최고 온도와 같다. 전반적으로 압력이 증가함에 따라 NO 생생률이 증가하며 N2 + O = NO + N 반응과 N + O2 = NO + O 반응이 NO 생성에 주도적인 역할을 한다. 연료희박화염의 경우 화염 후류지역에 존재하는 O2와 N2로 인해 압력증가에 따른 화학평형조성 변화로 thermal NO 생성률은 압력 증가에 양의 의존성을 보인다. 또한, 당량비가 상대적으로 높은 화염(Φ = 0.5)의 경우 증가된 화염의 온도로 인하여 압력 상승에 의한 thermal NO 생성률이 증가하였다. 가스터빈 연소기 조건과 유사한 상황에서 층류 예혼합화염을 이용한 본 연구의 계산 결과 화염 후류의 NO 농도는 압력 상승에 따라 선형에 가깝게 증가하는 것으로 나타났다.
4. 결 론
본 연구는 상세화학반응모델을 사용하여 H2/CO 예혼합화염의 NO 생성 특성을 연구하였다. 반응모델은 H2/CO 혼합물의 주요 연소 특성 및 예혼합화염에서 NO 농도를 비교하여 검증하였다. 가스터빈 연소기 조건과 유사한 화염온도(1886~1986 K)를 갖는 자유롭게 전파되는 예혼합화염을 압력 범위 1~20기압에서 계산하여 압력 변화에 따른 NO 생성 특성을 연구하였다.
1) NO는 반응지역에서 형성이 시작되며 화염 후류지역에서 선형에 가깝게 증가하였다.
2) 가스터빈 연소기의 연소가스 체류시간에 대응하는 시간(20ms)에 NO (15% dry O2 조건) 농도는 양의 압력 의존성을 가지며 화염온도가 증가할수록 높은 NO 증가율을 보였다.
3) 화염의 반응영역 부근에서 N2O 메커니즘을 통한 NO 생성이 압력 변화에 민감하지만 좁은 반응영역으로 인해 생성된 NO 농도는 압력 변화에 큰 변화가 없었다.
4) 화염 후류영역인 고온 영역에서 압력이 증가함에 따라 NO 발생률이 증가하며 Zeldovich 메커니즘에 의해 생성되는 NO 생성이 가장 중요하였다.