1. 서 론
2. E-Fuel 소개
2.1 E-Fuel의 개념 및 관련 용어
2.2 E-Fuel의 생산 과정
2.3 대체연료 간 비교
3. E-Fuel 연구 사례
3.1 FT 생산 공정의 연구 사례
3.2 E-Fuel 플랜트 소개
4. 결 론
1. 서 론
오늘날 기후변화는 인류의 생존에 대한 실질적인 위협이 되고 있다. 국제사회는 1992년 브라질리우회의에서 유엔기후변화협약(United Nations Framework Convention on Climate Change, UNFCCC)을 채택하여 기후변화의 억제를 결의했다. 이후 1997년 일본에서 열린 제3차 유엔기후변화협약 당사국총회(COP3)에서 교토의정서를 채택하고, 2015년 제21차 총회(COP21)에서 파리협정을 채택하는 데에 이르렀다.
산업화 이전 대비 온도 상승 폭을 2°C보다 훨씬 작도록 제한하는 것을 골자로 하는 파리협정은, 앞선 리우협약과 교토의정서와는 달리 구속력이 있는 국제법으로 인정된다. 이에 따라 대한민국을 포함한 당사국들은 단기적으로 2030년까지 실현 가능한 국가별 온실가스 감축 목표(Nationally Determined Contribution, NDC)를, 장기적으로 2050년 전후를 목표로 탄소 순배출량 0의 탄소중립 실현을 위한 로드맵을 제시해야 한다.
이에 발맞추기 위해 대한민국을 포함한 세계 각국에서 탄소중립 및 에너지 전환 관련 법안이 비준되고 있다.
미국은 트럼프 행정부에서 파리협정에서 탈퇴하였으나 2020년 바이든 행정부로 정권이 교체되면서 협정에 재가입했다. 바이든 행정부는 2050년 탄소중립을 목표로 2030년까지 탄소 공해 없는 전기만을 이용할 것을 선언했으며, 2035년 이후에는 순배출량 0의 차량만을 판매할 것을 계획 중이다[1].
유럽연합은 2050년 탄소중립을 목표로 설정하는 것을 골자로 하는 ‘European Green Deal’ 정책 패키지를 2019년에 발표하였고, 2030년까지 탄소 배출량을 1990년 수준에 비해 55% 이상 감축하기 위한 구체적인 방법들을 제시한 ‘Fit for 55’ 입법 패키지를 2020년에 발표했다. 특히 항공 및 해양 운송 분야에서 지속가능 연료(sustainable fuel)의 혼유를 의무화할 계획이며, 바이오연료(biofuel) 및 e-Fuel 등의 탄소중립연료에 대해 인센티브를 부여할 예정이다[2].
일본은 친환경 암모니아를 차세대 연료 및 수소 캐리어로 선정하여 현재 활발히 연구하고 있다. 2030년까지 2013년 대비 온실가스를 46%까지 감축할 계획이며, 2050년 탄소중립을 목표로 하고 있다.
대한민국 역시 기후변화협약 당사국으로 파리협약에 따라 2030년까지 2018년 배출량 기준 온실가스 총배출량 대비 40% 감축할 계획이며, 궁극적으로 2050년까지 탄소중립을 실현하는 것을 목표로 하고 있다[3]. 2021년 10월, ‘2050 탄소중립 시나리오안’을 발표하면서 국내 탄소 순배출량을 0으로 하는 두 개 시나리오를 제시했다. A안은 LNG 등의 화력 발전을 전면 배제하고 100% 신재생에너지를 활용하는 시나리오인 반면, B안은 화력 발전이 잔존하는 대신 이산화탄소 포집·활용·저장(Carbon capture, utilization, and storage, CCUS) 기술을 적극적으로 활용하는 계획이다[4].
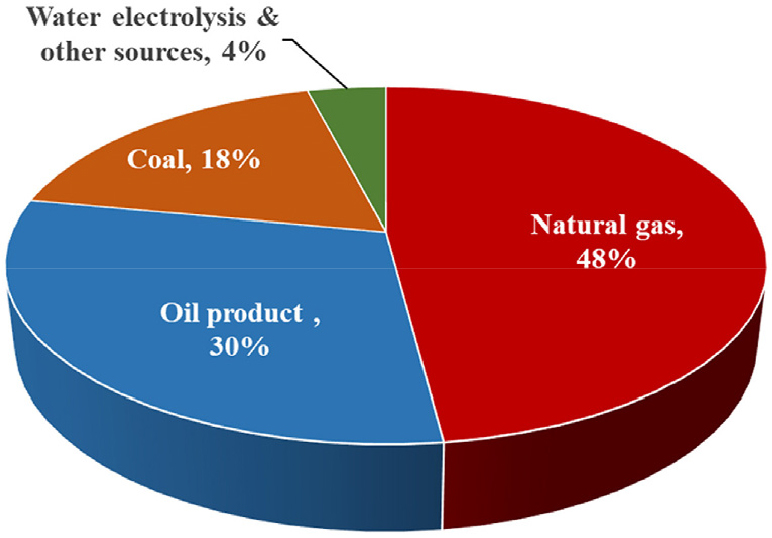
탄소중립을 실현하려면 현재의 화석연료 기반 에너지 체제에서 벗어나 재생에너지를 적극적으로 활용하는 체제로의 급진적인 에너지 전환(energy transition)이 이루어져야 한다. 화석연료를 대체할 미래 에너지원의 후보로 수소가 많은 관심을 받고 있다. 수소는 높은 질량당 에너지를 갖고 있으며, 무탄소 연소를 통해 가스터빈의 연료로 사용될 수 있고, 연료전지를 통해 전기화학적 방법으로 에너지를 생산할 수도 있다. 그러나 Fig. 1에서 확인할 수 있듯 현재 수소 생산량의 96%가 석탄 및 천연가스 등 화석연료의 개질을 통해 생산되고 있으며[5], 개질 과정에서 다량의 이산화탄소가 발생하기 때문에 현재의 수소 생산 기술은 탄소중립과는 다소 거리가 있다. 화석연료에 기인한 그레이 수소를 대신하여 풍력 및 태양과 같은 재생에너지를 활용해 수소를 생산하는 방식이 주목받고 있다. 생산 과정에서 탄소 배출이 없는 수소를 그린 수소라 하며, 전기에너지를 이용해 수전해를 유발하여 물로부터 수소와 산소를 얻는 기술이 활발히 연구되고 있다.
수소는 탄소중립 사회의 실현을 위한 핵심 물질로 손꼽히고 있지만, 현재 활용되고 있는 수소 저장 기술은 부피당 에너지가 높지 않아 효율적인 저장 및 운송이 어렵다는 단점이 있다. 현재는 에너지 저장 밀도를 높이기 위해 700 bar 고압 압축 혹은 20 K 극저온 액화 방식이 널리 쓰이고 있으며, 이러한 물리적인 방법 외에도 저장 밀도를 극대화하기 위해 수소 캐리어를 사용하는 화학적인 방법이 고려되고 있다. 수소로부터 암모니아 및 각종 탄화수소계 연료를 합성할 수 있으며, 이렇게 얻어진 연료를 e-Fuel이라 칭한다.
E-Fuel은 기존의 석유 기반 연료와 본질적으로 동일한 물성을 갖고 있어, 현존하는 연소기 및 내연기관에 그대로 적용하여 탄소중립적인 방식으로 화석연료를 대체할 수 있는 미래 연료이다. 국내의 ‘2050 탄소중립 시나리오안[4]’과 유럽연합의 ‘Fit for 55[2]’ 입법안 패키지에서도 e-Fuel을 차세대 대체연료로 지목한 바 있다. 독일과 북유럽 국가들의 경우 현재 e-Fuel의 대단위 플랜트의 건설 계획을 발표하였거나 공사를 진행하고 있으며, 일본 자동차 업체 3사 역시 e-Fuel의 연구개발을 진행하고 있는 것으로 알려졌다[6].
본 논문의 목적은 미래 연료로 각광받고 있는 e-Fuel을 소개하고 이의 연구개발 동향을 살펴보는 데에 있다. 2장에서는 e-Fuel의 개념과 관련 용어를 소개하며, 구체적인 생산 과정을 서술한 후, 미래 대체연료의 후보군과 e-Fuel을 비교한다. 3장에서는 e-Fuel의 생산 과정을 다룬 선행 연구와 e-Fuel 플랜트의 사례를 살펴본다.
2. E-Fuel 소개
2.1 E-Fuel의 개념 및 관련 용어
2.1.1 E-Fuel의 개념
E-Fuel, 혹은 electrofuel은 전기 기반 연료(electricity- based fuel)의 줄임말로, 그린 수소로부터 합성된 탄소중립연료를 의미한다.
탄소중립연료는 현존하는 액체연료 중심의 인프라에 그대로 적용 가능하며(drop-in fuel), 동시에 탄소 순배출량 0을 달성할 수 있다는 점에서 수송 분야의 탈석유화에 기여할 수 있는 연료로 고려되고 있다[7].
항공 및 해운 분야의 경우 유상하중의 극대화를 위해 높은 에너지 밀도의 연료가 필요하다. 현세대의 리튬 이온 배터리의 비에너지는 약 0.25 kWh/kg 수준으로[8], 일반적인 화석연료의 비에너지인 12 kWh/kg에 비해 매우 낮다. 유상하중 확보의 관점에서 기체의 경량화가 요구되는 항공기와 선박은 일반적으로 수소 혹은 배터리를 이용한 전동화가 어렵다고 여겨지며, 바이오연료 등의 대체연료를 적극적으로 고려하고 있다.
2011년 기준 항공 분야는 인간 활동에 기인한 복사강제력의 3.5%를 차지하고 있으며[9], 향후 항공 수송의 수요가 증가하면서 지구 온난화에 대한 기여도 역시 증가할 것으로 보인다. 국제항공운송협회(International Air Transport Association, IATA)에서는 화석연료에 의존하는 현재의 항공연료를 대체할 지속가능 항공유(Sustainable Aviation Fuel, SAF) 개념을 제시했다. SAF는 현존하는 제트 연료와 거의 동일한 화학 조성 및 물성을 갖고 있어, 항공기 혹은 엔진의 개조 없이 혼용될 수 있어야 한다[10]. Drop-in fuel인 e-Fuel은 IATA가 제시하는 SAF의 기준을 충족하여 차세대 항공유로 사용될 수 있다.
해운 분야는 인간에 의해 발생한 온실가스 배출량의 3%를 차지하고 있다. 전 세계적인 탈탄소화에 대응하기 위해 국제해사기구(International Maritime Organization, IMO)는 2050년까지 온실가스 배출량을 2008년 대비 배출량의 50% 수준으로 감축목표를 설정했다[11]. 우리나라 정부도 이에 발맞추어 제1차 친환경선박 개발·보급 기초계획을 발표하였다. 해당 계획에 따라 메탄올, 암모니아, 수소 및 기타 에너지로부터 동력을 얻는 친환경에너지 추진선박 개념을 정립하고 친환경선박으로의 체계적인 전환을 추진할 예정이다[12].
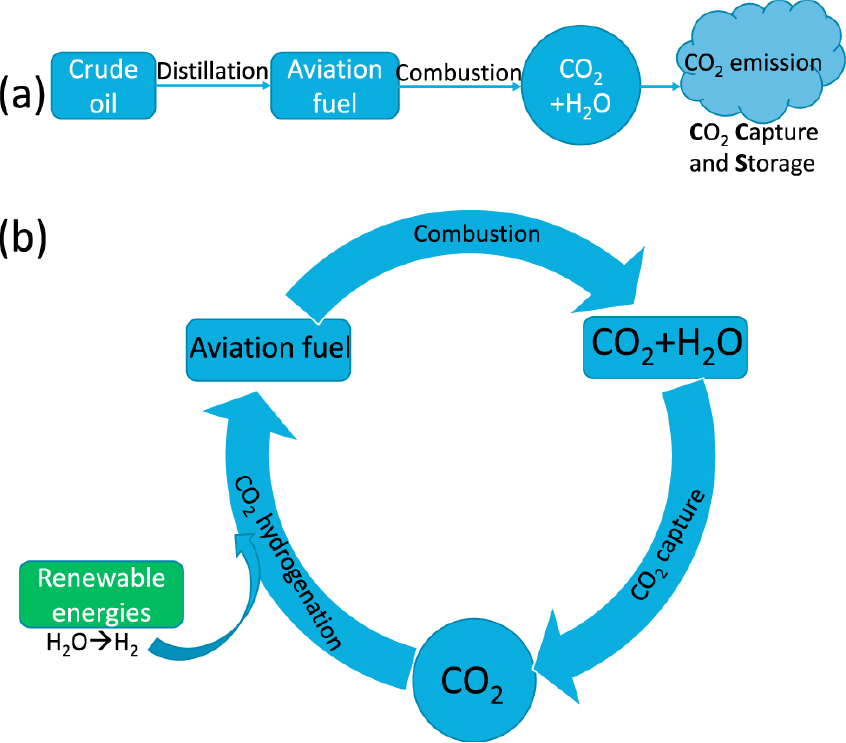
탄소중립연료는 일반적으로 탄화수소계 연료이기 때문에 연소 시 이산화탄소를 배출하지만, 생산 과정에서 연도가스(flue gas)나 대기로부터 이산화탄소를 포집하기 때문에 전과정평가(life cycle assessment)의 관점에서 순배출량은 0에 가깝다. 특히 대기 중 직접 포집(Direct Air Capture, DAC) 기술을 통해 선박 및 항공 등의 소형 배출원으로부터 발생하는 이산화탄소를 포집하여 연료로 재합성하는 것으로 순배출량 0의 폐쇄형 탄소 사이클(closed carbon cycle)을 구현할 수 있다[13]. Fig. 2에서 화석연료 기반 개방형 탄소 사이클과 탄소중립연료를 통하여 구현된 폐쇄형 탄소 사이클의 개념도를 확인할 수 있다.
2.1.2 탄소중립연료 관련 용어
본 단락에서는 국내외의 여러 연구에서 제시하고 있는 e-Fuel과 탄소중립연료 관련 기술 용어의 용례를 검토하였다.
E-Fuel, 혹은 electrofuel이라는 용어가 비교적 최근에 탄생한 신조어이기 때문에 그 정의와 물질의 범주가 연구에 따라 다르다[15]. 선행 연구에서의 용례를 검토해 본 결과 e-Fuel은 크게 두 가지 의미로 사용되고 있었다.
첫 번째로, 그린 수소와 포집 이산화탄소로부터 생산된 합성연료 개념의 용례가 있다. 해당 용례로 e-Fuel을 사용한 연구는 화석연료를 대체할 FT 연료(Fischer-Tropsch fuel)로 그 범위를 한정하였거나[16,17,18,19], 보다 넓은 의미로 사용되어 메탄올, 메테인, 디메틸에테르(dimethyl ether, DME) 및 폼산과 같은 다양한 탄화수소계 물질을 모두 다루고 있었다[20,21,22,23,24,25,26,27].
두 번째로, 재생에너지를 수전해를 통해 물질 형태로 저장하는 에너지 캐리어 개념의 용례가 있다. 이 경우 그린 수소와 그린 수소로부터 파생된 다양한 물질들을 e-Fuel의 범주에 포함하고 있었으며, 앞서 언급한 탄화수소계 연료 외에도 그린 수소 자체와 그린 암모니아 등을 e-Fuel의 범주에 포함하고 있었다[28,29,30,31,32,33,34,35,36,37].
국내에서 e-Fuel은 주로 ‘탄소중립연료[38]’, ‘이퓨얼[39]’ 혹은 ‘재생합성연료’ 등으로 번역되고 있으며, 주로 내연기관에서 현재의 화석연료를 대체할 수 있는 합성석유 기반 연료를 의미한다. 국내 2050 탄소중립 시나리오안에서 e-Fuel의 개념을 대기중 탄소를 포집하여 연료화한 것으로 제시하였으며, 안에 따르면 잔여 내연기관차에 e-Fuel 등 대체연료를 활용하여 직접공기포집을 통해 연소 배출물을 상쇄하여 대기 중 이산화탄소 농도의 순 증가를 방지하게 된다[4].
재생에너지 저장의 관점에서 e-Fuel을 합성하는 과정을 ‘power-to-fuel(PtF)’이라 표현하며[40], 이는 에너지를 다양한 형태의 캐리어로 가공하여 저장·활용하는 ‘power- to-X(PtX)’ 개념에서 파생된 단어이다[41]. 액상 합성연료인 e-Fuel 외에도 PtX 개념은 합성 천연가스(SNG) 혹은 그린 수소 같은 기체상 생성물일 때의 ‘power-to-gas(PtG)’, 액체 생성물일 때의 ‘power-to-liquid(PtL)’을 포함한다[42].
PtX 과정을 통해 부문간 연계, 즉 섹터커플링(sector coupling)을 실현할 수 있다. 섹터커플링이란 인프라와 저장가능한 에너지를 활용하여 발전, 난방 및 수송 등의 여러 부문을 연결하는 시스템을 말한다[43]. 섹터커플링은 개념은 독일의 에너지 전환(Energiewende) 정책에서 처음 제시되었으며[44], 섹터커플링이 실현되면 시간 변동성이 큰 재생에너지의 잉여전력을 효율적으로 활용할 수 있고, 이를 통해 전반적인 전력 계통의 유연성을 확보할 수 있다[45]. 또한, 잉여전력을 PtX를 통해 물질의 형태로 전환한 후, 수송, 농업, 제조 등 탈화석연료가 어려운 분야에서 PtX 생성물을 활용하여 산업 전반에 대해 탈탄소화의 시차를 줄이고 결과적으로 탄소중립의 실현을 앞당길 수 있다.
요약하면, 탄소중립을 실현하기 위해서는 전방위에 걸친 탈탄소화가 이루어져야 하며, 부문간 연계(섹터커플링)을 구현하여 각 부문 간의 시차를 최소화해 탄소중립의 실현을 가속화할 수 있다. PtX 과정을 통해 비교적 탈탄소화가 빠른 발전 부문과 전동화가 어려운 항공·해운 수송 부문이 연계될 수 있으며, PtX의 생산물 중 하나로 화석연료와 유사한 물성과 화학 조성을 가진 e-Fuel 개념이 주목받고 있다.
2.2 E-Fuel의 생산 과정
Table 1에서 다양한 e-Fuel의 합성 경로를 확인할 수 있다. 모든 e-Fuel은 그린 수소로부터 합성되며, 이후 일련의 반응 경로를 거쳐 최종 생성물로 합성된다.
Table 1.
E-Fuel pathways
암모니아는 하버-보슈(Haber-Bosch) 과정 혹은 전기화학적 방법을 통해 생산한다. 하버-보슈 과정은 수소와 질소를 공급 원료로 받아 670 K, 10 MPa의 높은 온도와 압력 조건에서 반응이 일어난다(1). 하버-보슈 과정으로 하루에 2천-3천 톤의 암모니아를 생산하는 대규모 공장이 현재 작동 중이다[37]. 한편, 전기화학적 반응으로 암모니아를 합성하는 방법은 비교적 낮은 온도 및 압력 조건(100°C 및 10 bar 이하)에서 물과 질소로부터 암모니아를 생산하는 공정이다. 이론상 하버-보슈법에 비해 에너지 효율이 높으나 아직 기술 성숙도가 낮아 상용화된 사례가 부족하다[46].
메탄올은 포집 이산화탄소와 그린 수소 원료의 촉매 수소화(hydrogenation) 반응으로 생산된다. 구체적인 경로에 따라 이산화탄소로부터 직접 합성하거나(2), 역수성가스전환(Reverse Water Gas Shift, RWGS) 반응을 거쳐 이산화탄소를 합성가스로 전환한 후 일산화탄소로부터 합성하는(3) 방법이 있다[14].
메테인은 사바티에(Sabatier) 반응(4) 및 메테인화 반응(5)을 통해 생성된다[47]. 메테인을 합성하는 PtG 과정으로 폐쇄형 탄소 사이클을 구현할 수 있지만, 메테인은 그 자체가 이산화탄소보다 강력한 온실가스라는 문제가 있다[48].
DME를 연료로 하는 압축착화 엔진은 디젤에 비해 미세먼지, CO2, NOx의 감소 효과가 있다고 알려져 있다[49]. DME의 생산 과정은 합성가스로부터 메탄올을 생산한 후 탈수 반응(dehydration)(6)을 일으켜 전환하는 간접합성법과 합성가스로부터 직접 생산하는 직접합성법으로 나누어지며, 현재는 공정의 효율이 높은 간접합성법이 산업적으로 널리 사용되고 있다[49].
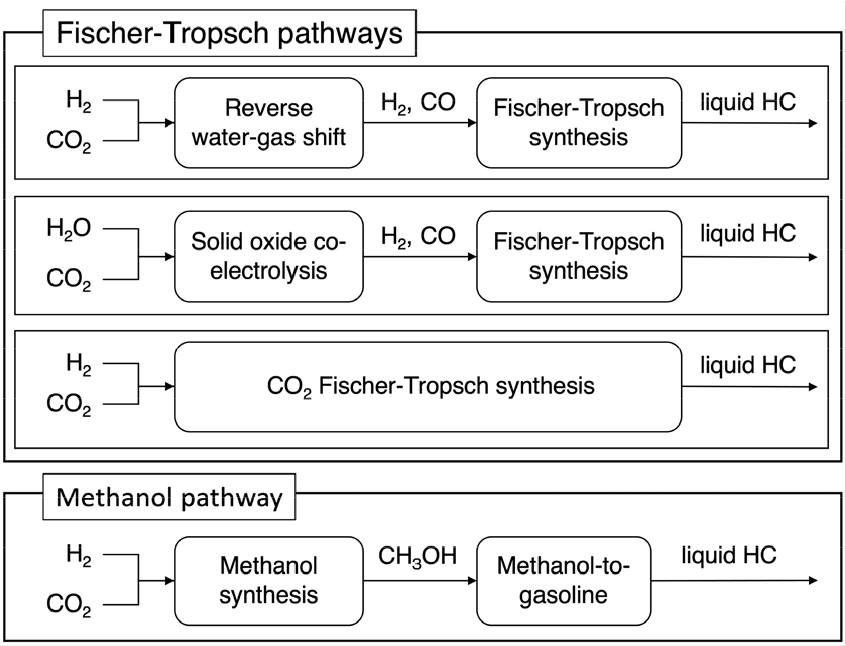
마지막으로 합성석유의 생산 경로는 주요 공정에 따라 크게 FT(Fischer-Tropsch) 경로와 MtG(Methanol-to- Gasoline) 경로로 나누어진다.
일반적인 FT 경로는 수소와 이산화탄소를 공급받은 후, RWGS 반응을 통해 합성가스(syngas)를 생산한 후, 피셔-트롭쉬 합성(Fischer-Tropsch synthesis)을 통해 넓은 탄소수 범위의 합성석유를 생산하는 일련의 과정을 거친다[50,51]. FT 합성 생성물은 이후 고도화 및 분리를 거쳐 종래의 가솔린, 케로신, 디젤 등의 화석연료와 유사한 탄소수 분포를 가진 FT 연료로 가공된다.
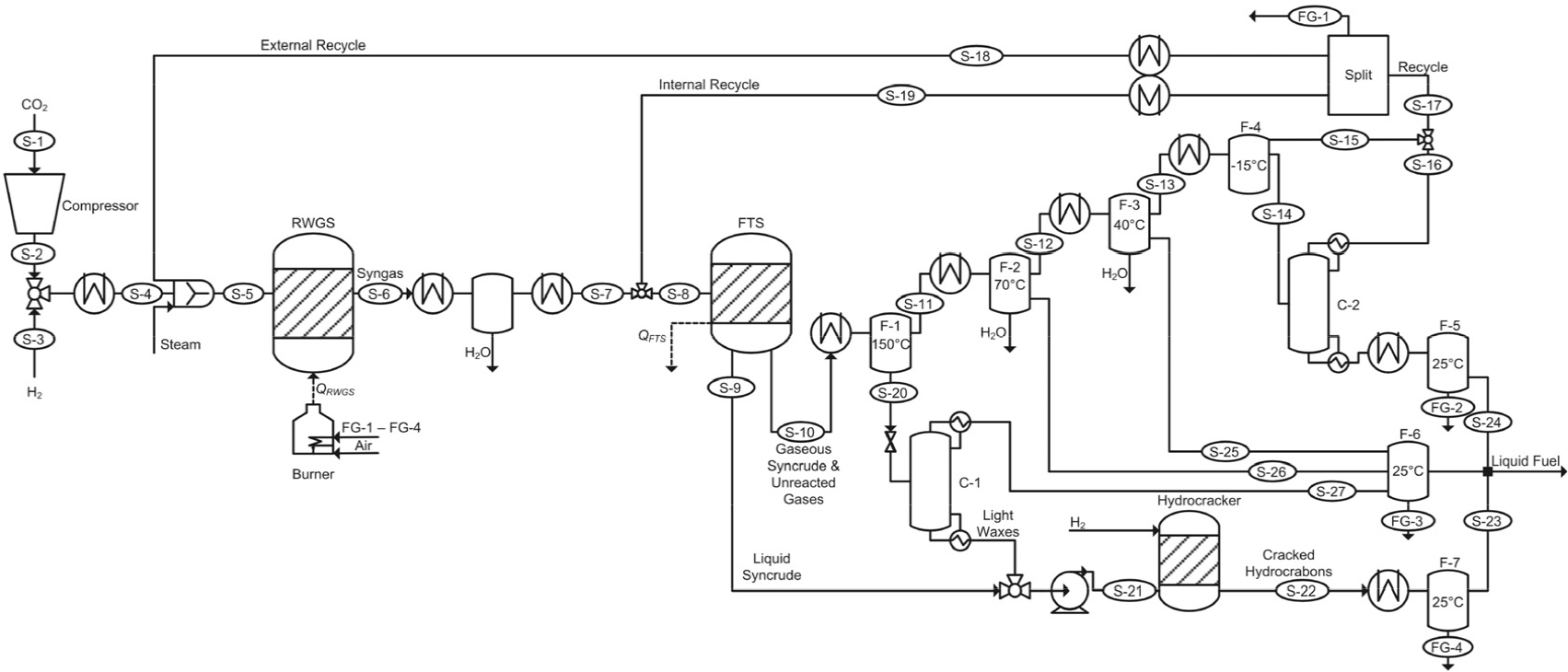
Fig. 3에서 FT 경로 및 MtG 경로로 생산된 합성석유의 생산 공정을 확인할 수 있다. 수전해와 이산화탄소 포집, RWGS, FT 반응 등 FT 연료의 구체적인 합성 과정을 후술한다.
2.2.1 수전해
수전해는 물을 전기분해하여 고순도의 수소와 산소를 얻는 과정이다. 석탄 혹은 메테인으로부터 수소를 추출하는 방식과 달리, 생산 과정에서 탄소배출이 없는 수전해는 수소 기반 청정에너지 사회의 필수 기술로 여겨진다.
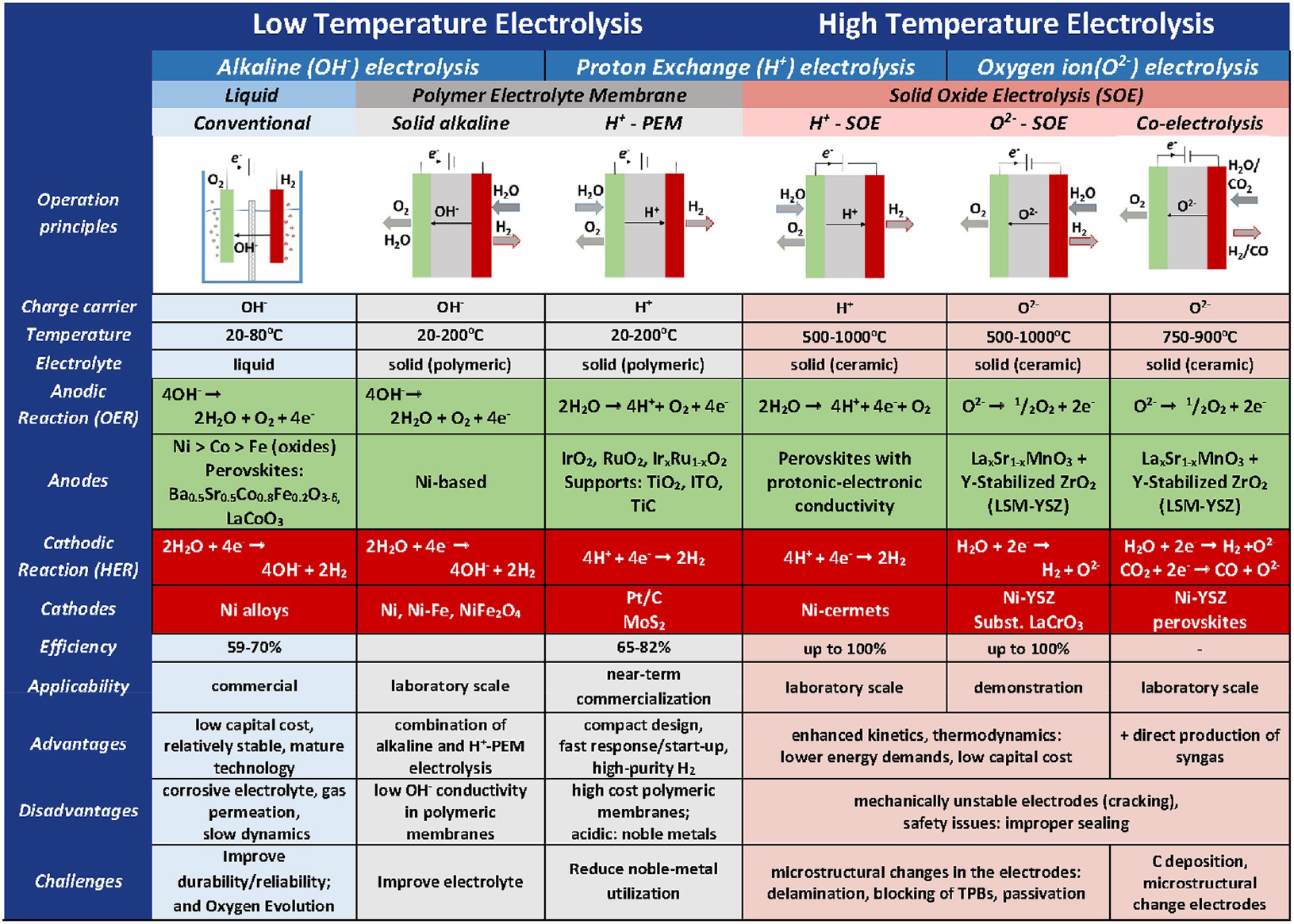
현재 수전해 설비의 전해질로 알칼리(Alkaline), 양성자 분리막(Proton Exchange Membrane, PEM) 및 고체 산화물(Solid Oxide, SO)이 널리 사용되고 있다[52]. Fig. 4에서 알칼리, PEM 및 SO 등의 전해질에 대한 일반적인 특성과 장단점 등을 확인할 수 있다.
알칼리 전해조(AEC)는 두 개의 전극과 알칼리성 수용액 전해질(주로 KOH 혹은 NaOH)로 구성되며, 전해질을 통해 수산화이온(OH-)이 음극(cathode)에서 양극(anode)으로 이동한다. 추가로 전극에서 생성된 수소와 산소를 격리하기 위한 격막이 수용액 내부에 설치된다. 알칼리 수전해 기술은 현재 산업에서 대단위 규모로 활발하게 사용되고 있는 기술이며, 전극 촉매로 귀금속이 아닌 니켈, 코발트, 은과 같은 전이금속이 사용되어 가격이 저렴하다는 장점이 있다. 그러나 염기성 전해액에 의한 전극과 촉매 등의 부식 문제가 있으며, PEM 및 SO 전해질에 비해 효율이 낮은 편이다[53,54].
양성자 분리막 전해조(PEMEC)는 전극과 고분자 전해질막으로 구성되어 있다. 양이온(H+)은 고분자 전해질막을 통해 양극에서 음극으로 이동한다. PEMEC는 AEC에 비해 시스템을 컴팩트하게 구성할 수 있으며, 작동 범위가 넓다는 장점이 있다. 또한 공급물질의 유량 변화에 대한 반응 속도가 빠르며, 전류 밀도가 높아 운영비용(operating cost)의 절감에 도움이 된다. 그러나 전극 촉매로 부식에 강한 백금 혹은 이리듐 계열의 귀금속이 사용되기 때문에 알칼리 수전해 방식에 비해 높은 비용이 소요된다는 단점이 있다[55,56].
고체 산화물 전해조(SOEC)는 전극과 고체 산화물 전해질로 구성되며, 700°C 이상의 높은 작동온도를 유지하기 위한 열교환기가 필요하다. PEMEC와 AEC에 비해 높은 효율을 보이며, 이론상 100%의 에너지 변환 효율을 가질 수 있다. 또한, 전력을 공급받아 수소를 생산하거나, 반대로 수소로부터 전기 에너지를 생산할 수 있는 가역 연료전지(reversible fuel cell)[57] 혹은 이산화탄소와 물을 공급받아 합성가스를 생산하는 공전해(co-electrolysis)[58]가 가능하다. 그러나 높은 작동 온도에 의해 시간이 지남에 따라 셀의 열화가 진행된다는 점, 그리고 생성물 수소와 증기의 혼합물로부터 고순도의 수소를 추출하는 별도의 공정을 요구한다는 점 때문에 현재 연구 단계에 머무르고 있다[59,60].
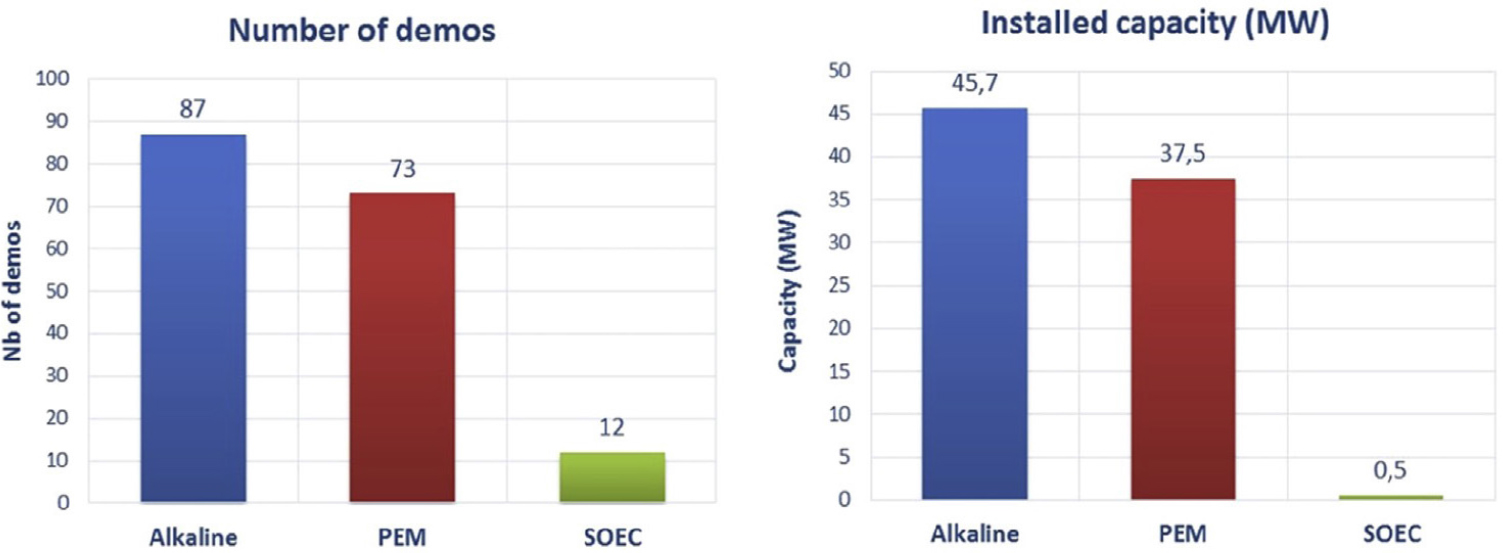
Fig. 5는 현재까지 보고된 PtX 실증 플랜트의 전해질 종류별 플랜트 수와 용량을 보여준다. 32개국 192개 실증 플랜트 대부분에 알칼리 및 PEM 전해조가 적용되어 있으며, 고체산화물 전해조는 이에 비해 플랜트 사례가 적다[61].
현재 수전해 기술을 이용한 수소의 생산 비용은 6,000- 7,500원/kgH2 수준이며[62,63], 대한민국 정부는 제1차 수소경제 이행 기본계획(2020.11.)에서 그린 수소 생산 규모를 2030년에 생산단가 3,500원/kgH2로 25만 톤급까지, 2050년에 2,500원/kgH2로 300만 톤급까지 확대해 나갈 계획이다[64].
2.2.2 이산화탄소 포집
순배출량 0의 폐쇄형 탄소 사이클을 구현하기 위해서는 높은 효율의 이산화탄소 포집 기술이 필수적이다. 탄소 포집 기술은 발전소와 공장과 같은 점배출원에 추가적인 공정을 적용하는 방식과 대기 중의 이산화탄소를 포집하기 위한 독립적인 포집 시설을 설치하는 방식으로 나뉜다.
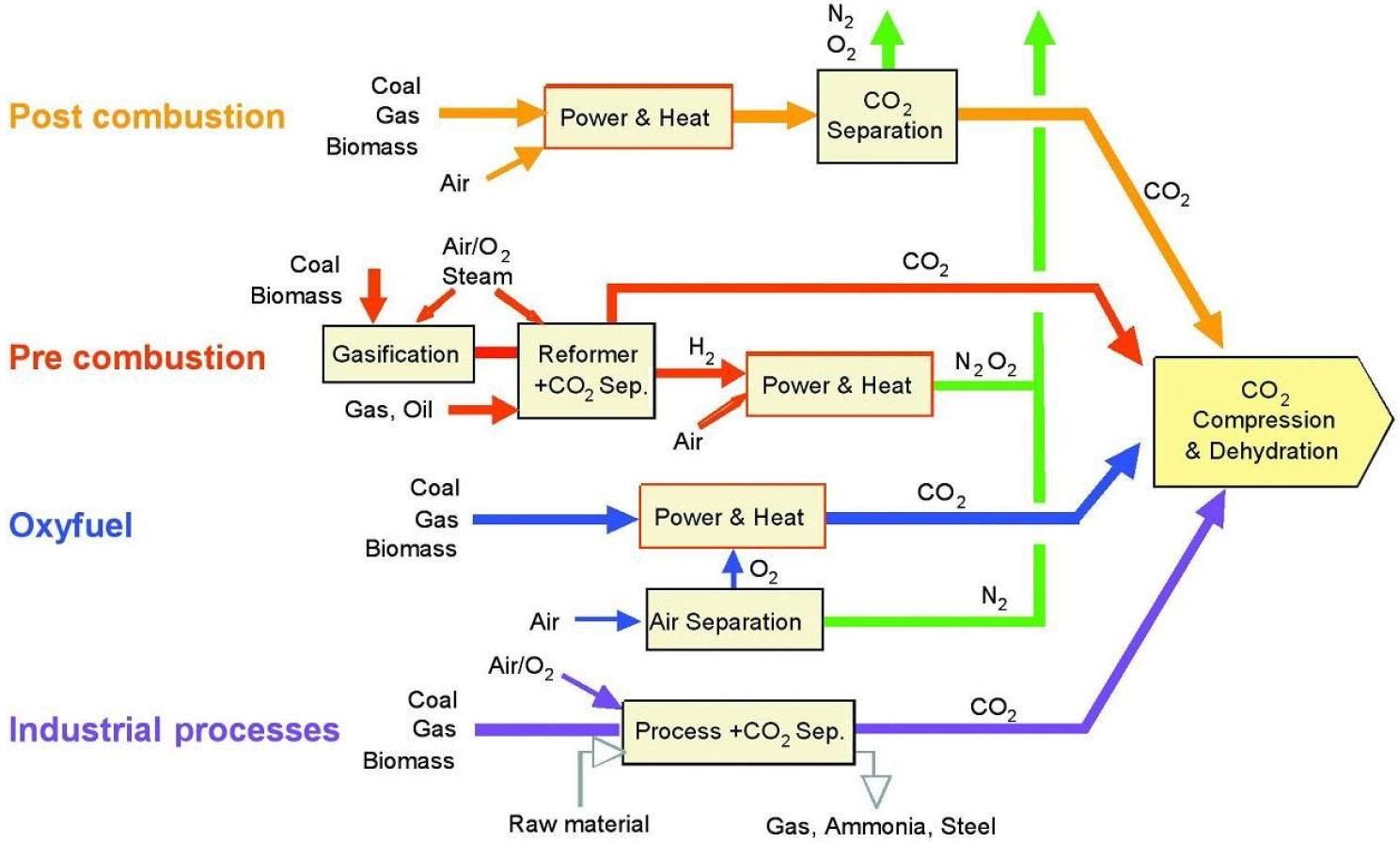
Fig. 6에서 제시하는 바와 같이 점배출원의 이산화탄소 포집 기술은 포집 시점에 따라 연소후 포집(post-combustion), 연소전 포집(pre-combustion), 그리고 순산소연소(oxy-fuel combustion)로 구분된다. 연소후 포집은 연소 후 배출된 배기가스를 추가적인 공정을 거치게 해 탄소를 분리하는 과정이다. 연소전 포집은 석탄 등의 연료를 이산화탄소/일산화탄소와 수소 및 증기로 분해한 후 탄소를 흡수한다. 마지막으로 순산소연소는 산화제로 공기 대신 산소만을 사용해 연소한다. 배기가스로 증기와 이산화탄소만이 배출되는데, 이때 비등점 차이를 이용하여 이산화탄소를 증류해 내는 과정이다.
이 중 연소후 포집이 산업에서 널리 쓰이고 있다. 연소후 포집은 세부적으로 흡수(absorption), 흡착(adsorption), 막분리(membrane separation) 및 극저온 분리(cryogenic separation)로 구분된다.
연소후 포집 기술 중 모노에탄올아민(MEA) 등의 아민 수용액을 이용한 흡수법인 아민 스크러빙(amine scrubbing)이 현재 가장 널리 쓰이고 있다[66]. 아민 스크러빙은 기존의 발전소에 쉽게 적용할 수 있으며, 수용액이 100-120°C의 증기에 의해 재생되어 반복 재사용이 가능하다는 장점이 있다[67]. 그러나 연도가스의 SO2, NO2 등에 의해 아민의 성능 열화가 발생하며, 고온 증기를 이용한 MEA의 재생을 위해 열교환기에 많은 에너지를 투입해야 한다는 단점이 있다[68].
한편 점배출원에서의 포집 기술 외에도 공기를 직접 포집하는 DAC 기술이 활발하게 연구되고 있다. 특히 수송 분야의 경우 선박 및 항공기와 같은 소형 배출원에 연소후 포집 기술의 적용이 불가능하므로, 대규모 플랜트에 의한 직접 공기 포집을 통해 순배출량을 0으로 만들어야 한다[69]. E-Fuel을 통한 폐쇄형 탄소 사이클의 구현에 있어 DAC는 필수적인 기술이라 할 수 있다.
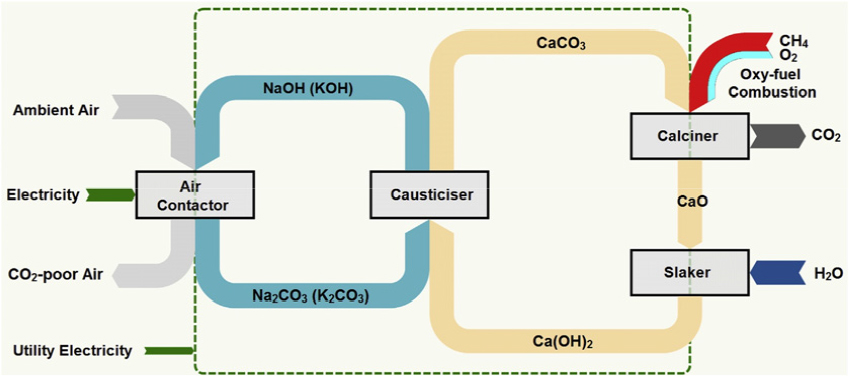
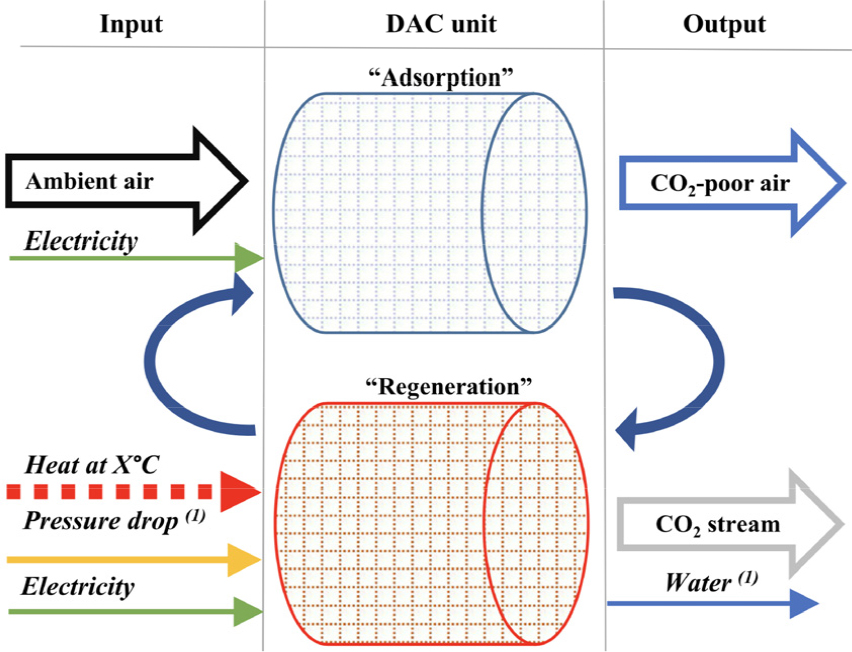
DAC는 작동 조건 및 흡수제에 따라 900°C에서 작동하는 고온 수용액법(high temperature aqueous solution)과 100°C 이하에서 작동하는 저온 건식흡수제법(low temperature solid sorbent)으로 분류된다[70]. Fig. 7과 Fig. 8에 고온 수용액법과 저온 건식흡수제법의 개략도를 도시하였다.
고온 수용액법에서 수산화나트륨(NaOH) 및 수산화칼륨(KOH)이 널리 사용된다. 수산화나트륨이 적용된 경우, 수산화나트륨이 이산화탄소와 반응하여 탄산나트륨(Na2CO3)의 형태로 이산화탄소를 흡수한 후, 탄산나트륨이 다시 수산화칼슘(CaCO3)과 결합하여 수산화나트륨이 재생된다. 이때 수산화칼슘의 탄소가 탄산칼슘(CaCO3)의 형태로 변하며, 탄산칼슘은 900°C의 고온에서 산화칼슘(CaO)과 이산화탄소로 분리되어 최종적으로 이산화탄소가 포집된다. 산화칼슘은 다시 수소와 반응하여 수산화칼슘으로 재생된다[69]. 이는 다음과 같이 화학식으로 표현할 수 있다.
이산화탄소 포집 단계에서 900°C 이상의 높은 온도가 요구되는 고온 수용액법과는 달리, 저온 건식흡수제법은 고체 흡수제를 이용하여 공기로부터 이산화탄소를 흡수한 후, 저압 조건에서 90-100°C의 열을 가해 고순도의 이산화탄소를 추출하면서 흡수제를 재생하게 된다[69]. 흡수반응기 및 재생반응기 각각에서 일어나는 반응은 다음과 같다[71].
국제에너지기구(International Energy Agency, IEA)에 따르면 연간 탄소 포집량은 2020년 현재 40 Mt에서 2030년 1,670 Mt, 2050년 7,600 Mt로 늘어날 것이며, 특히 DAC를 이용한 포집 용량은 2020년 실질적으로 없는 상태에서 2030년 90 Mt, 2050년 985 Mt까지 늘어날 것으로 예측했다[72]. 기후 위기의 타개책으로 주목받고 있는 CCUS 기술에 전 세계적으로 많은 이목이 모이고 있는 만큼, DAC 시장은 탄소중립화에 발맞추어 빠르게 커질 것으로 보인다.
2.2.3 역수성가스전환(RWGS)
이산화탄소는 이중 결합(O=C=O) 두 개로 이루어진, 반응성이 아주 낮은 안정한 물질이다. 이산화탄소의 이중 결합을 해리하는 데에 많은 에너지가 요구되기 때문에, 이산화탄소가 직접 반응에 참여하는 경우는 드물다. 대신, 이산화탄소를 보다 반응성이 높은 일산화탄소로 전환하여 이후 공정에서 사용하는 것이 유리하다고 알려져 있다. 일반적으로 역수성가스전환(Reverse Water-Gas Shift, RWGS) 반응을 통해 이산화탄소로부터 합성가스를 생산하게 된다.
이산화탄소의 해리 과정은 아래 식과 같다.
한편, RWGS 반응과 함께 부반응인 사바티에 반응(Sabatier reaction)이 동시에 일어난다.
Fig. 9에서 온도에 따른 생성물의 몰농도 분포를 확인할 수 있다. Le Châtelier 법칙에 따라 높은 온도에서 흡열반응인 RWGS가 더 활발하게 일어나는 반면, 온도가 낮을 때에는 발열 반응인 WGS 및 메테인화 반응이 활발해진다. 이 때문에 일산화탄소 선택도를 높이기 위해서는 높은 온도에서의 운전이 바람직하다[73]. 현재 고온의 RWGS 반응에서 구리, 백금 및 로듐이 금속 담지 촉매로 널리 쓰이며[74], 이때 지지체로는 SiO2, Al2O3, zeolite, TiO2, CeO2, ZrO2 등이 쓰인다[75].

Fig. 9.
Equilibrium composition of the gaseous products of RWGS reactions at 0.1 MPa with H2 : CO2 molar ratio 1 : 1[75].
탄화수소계 e-Fuel 생성 시 에너지 전환 효율을 높이기 위해 합성가스를 거쳐 생산되기 때문에 PtX 과정에서 RWGS 과정 역시 비중 있는 역할을 맡을 것으로 보인다. RWGS 반응의 경제성을 높이기 위해서는 높은 일산화탄소 선택도를 보이는 저온 RWGS 촉매의 연구가 필요하다.
한편, 합성가스 생산을 위한 RWGS 반응을 생략하는 공전해(co-electrolysis) 경로 및 CO2-FT 경로가 관심을 받고 있다. SOEC 수전해 과정에서 공전해 기술을 이용할 수 있는데, 이를 통해 물과 이산화탄소로부터 합성가스를 직접 생산할 수 있다. 또한, 이산화탄소와 수소를 직접 공급물질로 사용하여 CO2-FT 경로로 FT 연료를 생산하는 방법 역시 연구가 이루어지고 있다[76].
2.2.4 피셔-트롭쉬 공정(FT Process)
합성석유 생산의 핵심 공정이라 할 수 있는 피셔-트롭쉬 공정(Fischer-Tropsch process, FT 공정)은 합성가스로부터 탄화수소계 연료를 합성하는 공정이다. 1920년대에 소개된 이후[77] 지금까지 산업계에 널리 쓰이고 있으며, 특히 국외의 경우 석탄으로부터 액체 합성연료를 생산하는 대단위 플랜트가 현재 작동 중인 만큼[44] FT 공정은 상용화가 완료된 성숙한 기술이라 할 수 있다.
FT 공정을 통해 합성가스는 연쇄성장반응(chain growth reaction)을 통해 넓은 탄소수 범위의 선형 파라핀계 탄화수소로 전환된다[78].
FT 공정을 통해 합성된 탄화수소 화합물을 합성석유(syncrude)라 말한다[79]. 이때 생성물인 합성석유의 탄소수 분포는 일반적으로 ASF 분포(Anderson-Schulz-Flory distribution)로 표현된다[80].
이때 xn은 특정 탄소수의 몰분율, α는 사슬성장확률(chain growth probability), n은 탄소수이다. Fig. 10에 사슬성장확률에 따른 생성물의 분포를 도시하였다.
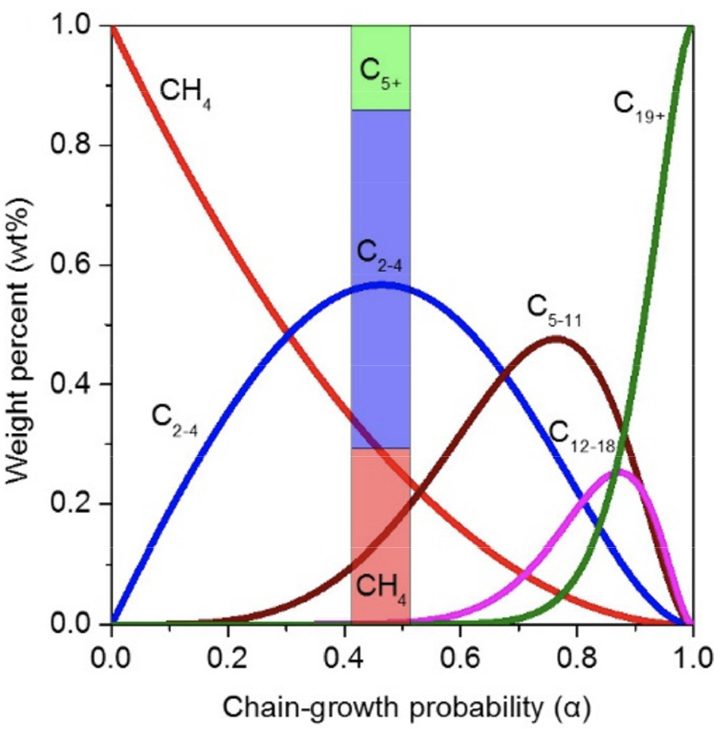
Fig. 10.
Fischer-Tropsch production distribution according to the ASF model, vertical bar shows distribution for α of 0.46[82].
FT 공정의 작동 조건 및 촉매에 따라 생성물별 선택도가 달라진다. 선택적 합성반응으로 특정 생성물이 상대적으로 높은 비율로 합성반응을 일으킬 수 있도록 하는 기술들이 개발되어 현재 상용화되었다[81]. Table 2에서 작동 조건 별 선택도 변화 경향을 확인할 수 있다.
Table 2.
conditions on product selectivity while increasing parameters[82]
일반적으로 350°C 전후에서의 FT 합성을 고온 FT 합성(HTFT)이라 하며, 190-250°C 온도 범위에서의 FT 합성을 저온 FT 합성(LTFT)이라 한다. 수소화 및 촉매 표면에서의 탈착이 잘 일어나는 HTFT에서 탄소수 10 이하의 가벼운 탄화수소의 비중이 높으며, 반대로 LTFT일 경우 무거운 탄화수소의 합성량이 증가한다[82].
산업체에서 FT 합성의 촉매로 철 혹은 코발트 계열이 가장 널리 사용되고 있다. 촉매의 종류에 따라 생성물의 조성에 차이가 있으며, 비교적 수소화가 덜 일어나는 철계 촉매를 이용하면 올레핀 계열 및 함산소계 탄화수소 비율이 높은 반면, 코발트계 촉매를 이용하면 생성물 대부분이 포화 탄화수소가 된다[82]. 촉매의 종류에 따라 적합한 작동 온도가 달라지는데, 철 계열 촉매는 넓은 작동 조건을 갖고 있기에 저온 반응(Fe-LTFT) 및 고온 반응(Fe-HTFT) 조건에서 모두 활용되는 반면, 코발트 계열 촉매는 저온 반응(Co-LTFT)에서만 사용된다[82].
합성가스의 성분비 역시 생성물 조성에 영향을 주는데, 일반적으로 H2:CO 비가 높아지면 수소화가 활발히 일어나면서 사슬성장확률 및 알켄과 함산소계의 선택도가 낮아진다[82].
FT 공정으로 얻은 합성석유는 이후 고도화 및 분리 과정을 거치게 된다. 수소화분해(hydrocracking)을 통해 왁스(>C20)와 같은 장쇄 탄화수소와 수소를 반응시켜 가벼운 단쇄 탄화수소로 크래킹하고, 합성석유를 분자량에 따라 증류하여 종래의 석유 기반 연료들과 유사한 탄소수 분포 및 밀도를 가진 FT 합성연료가 생산된다.
2.3 대체연료 간 비교
화석연료의 자리를 이어받을 대체연료의 후보로 무탄소 연료인 수소, 암모니아와 생산 과정에 탄소 포집이 포함된 e-Fuel, 바이오연료가 거론된다. Table 3에서 보여지는 바와 같이 대체연료 후보 간의 물성과 연소 특성에 뚜렷한 차이가 있으며, 연료 생산 과정과 공급물질 역시 상이하다. 탄소중립 사회에서 특정 연료가 우세하여 나머지 후보들이 도태되기보다는 시기와 장소, 그리고 용도에 따라 적절한 연료를 취사선택하게 될 것이다. Table 4에서 수소, 암모니아, e-Fuel, 그리고 바이오연료의 일반적인 장단점을 확인할 수 있다.
Table 3.
Table 4.
Advantages and disadvantages of alternative fuels
본 절에서는 대체연료 후보들의 전반적인 특징과 연구 동향을 검토하고, 각 후보와 e-Fuel을 비교하여 장단점을 서술한다.
2.3.1 수소
수소는 연소 생성물로 수증기만이 생성되는 무탄소 연료로, 대표적인 차세대 에너지원의 후보로 여겨지고 있다. 수소는 연료로 사용될 수 있을 뿐만 아니라, 연료전지를 통해 전기 에너지를 생산할 수 있다.
수소의 중량당 에너지는 33.3 kWh/kg로 가솔린(12.9 kWh/kg)에 비해 2배 이상 높다는 장점이 있지만, 상온 상압 조건에서 부피당 에너지가 매우 낮으므로 일반적으로 압축 혹은 액화를 통해 밀도를 높인 후 저장하거나 운송한다. 상온에서 수소를 700 bar로 압축할 시 에너지 밀도는 1.25 kWh/L이며 액체 수소의 에너지 밀도는 2.36 kWh/L이다. 가솔린의 에너지 밀도가 9.5 kWh/L인 데에 비하면 수소의 에너지 밀도는 여전히 낮은 편이며, 특히 저장 시스템의 중량을 고려하면 에너지 저장 효율은 화석연료에 비해 매우 낮다. 또한 700 bar 압축 과정에서 수소 에너지의 20%에 해당하는 에너지가 소모되며, 액화하는 과정에서 수소 에너지의 40%에 해당하는 에너지가 소모되어 시스템 차원에서의 효율 저하가 발생한다[85].
최근 국내외에서 수소 연소에 관한 연구가 활발히 진행되고 있다. 수소는 화석연료에 비해 넓은 연소범위와 높은 자연발화온도를 보이며, 일반적으로 압축 점화 엔진보다 스파크 점화 엔진에 적합한 것으로 알려져 있다[85]. 수소 엔진의 기술적 난관으로 수소의 낮은 발화에너지(ignition energy) 및 넓은 연소범위에 의한 역화(backfire)와 조기 점화(pre-ignition)의 가능성이 있다. 또한 이산화탄소의 배출은 없지만 높은 단열화염온도에 의해 질소산화물(NOx)의 배출이 많다는 점도 문제이다. NOx 배출량 문제의 경우 수소의 넓은 연소범위를 활용해 낮은 당량비 조건(φ = 0.2)에서 연소하여 NOx 배출량을 최소화할 수 있는 것으로 알려져 있다[85,86].
2.3.2 암모니아
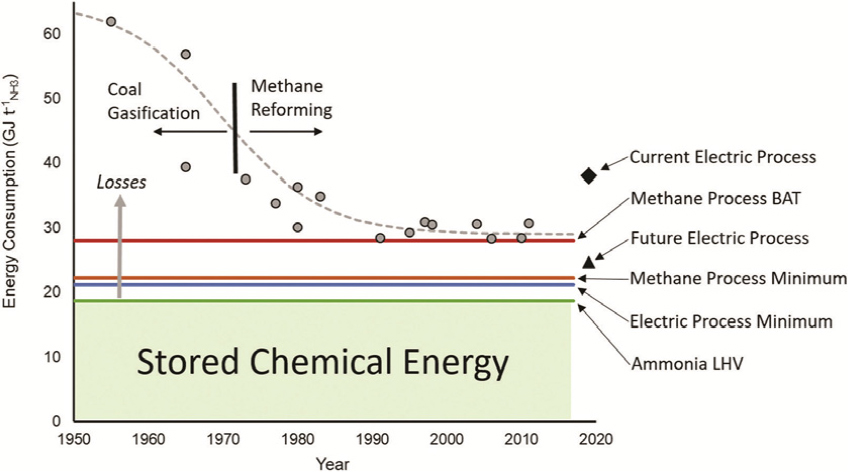
비료 생산의 주원료로 사용되는 암모니아는 매해 전 세계에서 1억 7,600만여 톤이 생산되고 있으며[87], 현재 전 세계적으로 생산량 및 소비량이 가장 많은 화학 물질이다. 현재 생산되는 암모니아 대부분은 화석연료 기반의 그레이 수소를 기반으로 하며, 그레이 암모니아 생산 과정에서 배출되는 이산화탄소가 세계 총배출량의 약 1.8%를 차지한다[87]. Fig. 11에서 1950년대부터 2020년대까지 암모니아 생산 공정의 효율이 향상되어 온 과정을 확인할 수 있으며, 천연가스 개질을 통해 암모니아를 생산하는 기술이 충분히 성숙하였음을 알 수 있다[88].
무탄소 에너지원 기반의 그린 수소를 공급물질로 받아 합성된 그린 암모니아는 생산 및 소비 과정에서 탄소배출이 전혀 없으며, 최근 무탄소 연소 연료 혹은 고체 산화물 연료전지(Solid Oxide Fuel Cell, SOFC)의 공급물질로 직접 이용하는 기술에서 큰 진전이 있다[46].
이러한 직접이용기술 외에 최근에는 수소 캐리어로서의 간접이용기술이 떠오르고 있다. 상대적으로 수송 및 저장 기술 수준이 낮은 수소에 비해 암모니아의 수송 및 저장 인프라는 활발한 생산 및 소비와 국제 무역으로 인해 아주 잘 갖추어져 있다. 또한 암모니아는 17.6 wt%의 높은 수소 저장 효율을 보이며, 이는 일반적으로 10 wt% 미만의 수소를 함유하는 금속 수소화물(metal hydride)에 비해 수소 캐리어로서 장점이라 할 수 있다.
잘 갖추어진 인프라와 수소 캐리어로서의 암모니아의 역할이 조명되면서 2010년대 이후 암모니아에 대한 국내의 관심이 높아지고 있다. 제1차 수소경제 이행 기본계획에서 액화 플랜트 구축과 함께 암모니아-수소 변환 기술의 확보가 수소 인프라 구축의 핵심 중 하나로 언급되었다[64]. 특히 해운 분야에서 암모니아 선박이 활발히 연구되고 있는데, 암모니아의 직접이용방식과 개질을 통한 수소로의 간접이용방식 모두를 염두하고 있다[12].
그러나 암모니아의 연소 특성 역시 수소와 마찬가지로 일반적인 연료와 차이가 있다. 암모니아는 화염속도가 느리고 자연발화온도 및 발화에너지가 높으며 연소범위가 15-25%로 좁다. 이 때문에 암모니아 단독 연소 엔진은 부하가 아주 작거나 클 때 연소 조건이 불안정하다는 문제점이 있다. 이렇듯 암모니아는 단독 연소보다는 반응성을 높이기 위해 dual-fuel 엔진에서 수소나 가솔린 등의 보조 연료와 함께 사용하는 것이 바람직하다[89]. 또한 암모니아의 연소 시 질소 성분이 산화되는 fuel-NOx 메커니즘에 의해 다량의 질소산화물이 생성된다는 문제도 있다[83].
이 외에도 암모니아는 구리 등 일부 금속과 고무 및 플라스틱에 대해 부식성이 있는 것으로 알려져 있으며, 이에 따라 연료 시스템 부품들의 수명 및 부식 방지에 대한 검토가 필요하다[90]. 또한 암모니아는 인체에 대해 독성을 띠므로 취급에 유의해야 한다.
2.3.3 바이오연료
폐쇄형 탄소 사이클을 구현하는 방안으로 생물 기반의 에너지원인 바이오매스(biomass)를 고려할 수 있다. 바이오매스는 성장 과정에서 광합성을 통해 이산화탄소를 흡수하기 때문에, 바이오연료의 연소 과정에서 발생하는 이산화탄소는 바이오매스 생산 과정에서 상쇄될 수 있다.
식물유의 에스터화를 통한 1세대 바이오디젤 생산 공정은 현재 상용화된 상태이다. 대한민국에서도 2015년부터 신재생에너지 연료 혼합의무화제도(Renewable Fuel Standard, RFS)가 시행되고 있으며, 이에 따라 수송용 연료 공급자는 3%의 바이오연료 혼유(BD3)를 공급해야만 한다[91].
그러나 1세대 바이오디젤은 당류 및 녹말류와 같은 식량 자원을 공급원료로 요구하기 때문에 식량과 연료 중에서 자원의 용도를 취사선택해야 하는 윤리적·사회적 문제가 제기될 수 있다. 이러한 문제를 해결할 방법으로 비식량자원인 리그노셀룰로오스(lignocellulose)를 활용하는 2세대 바이오매스와 조류(algae)에서 기인한 3세대 바이오매스가 제안되었다[92]. 2·3세대 바이오매스 기반 바이오연료는 현재 탄소중립연료의 대표 후보로 거론되고 있다.
그러나 2세대 바이오연료 생산 공정의 전처리 과정에서 에너지로 사용될 수 없는 리그닌(lignin)과 헤미셀룰로오스(hemicellulose)를 분리하는 데에 많은 에너지가 소요되며, 3세대 바이오연료는 현재 연구 단계에 머물고 있어 실용화까지는 시간이 걸릴 것으로 보인다[93].
바이오매스는 연료화 이전의 공급물질 단계에서 별도의 에너지 공급 없이 저장될 수 있으며, 덕분에 여타 재생에너지와는 달리 출력 조절이 가능(dispatchable)하다는 특성이 있다[93]. 반면에, e-Fuel 공정의 공급물질인 수소와 이산화탄소는 에너지 밀도가 낮은 기체이기 때문에 공급물질 단계에서 효율적으로 저장하기 위해서는 추가적인 에너지를 공급하여 압축하거나 액화해야 한다. 재생에너지 생산량의 큰 변동 폭을 고려했을 때, 저장 및 활용의 유연성 측면에서 바이오매스의 출력 조절 가능성은 두드러지는 장점이다.
반면, 바이오매스 생산 과정에서 많은 담수와 넓은 대지를 요구한다는 문제점이 있다. FT 경로로 생산된 e-Fuel의 경우 0.04 m3/GJ의 물을 요구하는 반면, 바이오연료의 경우 14-574 m3/GJ의 물이 필요하다[94]. 태양 에너지를 이용하여 합성석유를 생산하면 2.7 kW를 생산하는 데에 300 m2의 사막 면적이 필요한 데에 반해, 바이오연료의 경우 5,400 m2의 경작지를 요구한다[95]. 이 외에 에너지 작물에 의한 토양 산성화와 물의 부영양화 등의 문제를 고려할 시 오히려 화석연료보다 바이오연료가 친환경이지 못할 수 있다[96].
3. E-Fuel 연구 사례
3.1 FT 생산 공정의 연구 사례
Table 5에 그린 수소를 이용한 FT 합성 공정을 시뮬레이션한 사례를 정리하였다.
Table 5.
Literature survey on simulation of e-Fuel production
| Authors | Pathway |
Production rate | Efficiency |
Production cost |
| Becker et al. (2012) [59] |
SO co-electrolysis (800°C, 1.6 bar) CO-FT (240°C, 40 bar, α = 0.9) | 73,500 L/d | PtF* 51.0% | 1.16 $/GLE**** |
| König et al. (2015) [79] |
PEM electrolysis RWGS CO-FT (225°C, 2.5 bar, α = 0.85) | 5.5 t/d |
PtF 43.3% CC** 73.7% | 2.89 $/L |
| Cinti et al. (2016) [97] |
SO co-electrolysis (750°C, 1 atm) CO-FT (Co-based, 230°C, 20 bar, α = 0.94) | 159 L/d | PtF 57.2% | - |
| Albrecht et al. (2017) [98] |
PEM electrolysis (800°C, 25 bar) RWGS (900°C) CO-FT (Co-based, 230°C, 25 bar, α = 0.85) | 11 t/h |
PtF 50.6% CC 98% | 2.56 €/L |
| Zhang et al. (2019) [42] | CO2-FT (Fe-based, 300°C, 25 bar) | 450 kL/d | PtF 49.2% | 1.38 $/L |
|
Albrecht and Nguyen (2020) [30] |
PEM electrolysis RWGS (900°C, 2.7 MPa) CO-FT (Co-based, Low temperature, α = 0.95) | 0.96 t/d |
PtF 48.7% CC 98% | 2.01 €/L |
| Zang et al. (2021) [25] |
RWGS (600°C, 24.5 bar) CO-FT (Co-based, 220°C, 24.3 bar, α = 0.9) | 351 t/d | CCE*** 57.5% | 1.43-1.56 $/L |
| Isaacs et al. (2021) [35] |
Pathway 1: PEM electrolysis → RWGS → CO-FT Pathway 2: SO co-electrolysis → CO-FT CO-FT (Co-based, Low temperature) | 158,987 L/d |
1) CC 87% 2) CC 96% |
1) 2.89 $/L 2) 3.06 $/L |
| Herz et al. (2021) [99] |
Pathway 1: PEM electrolysis → RWGS → CO-FT Pathway 2: SO co-electrolysis → CO-FT CO-FT (200°C, 20 bar, α = 0.9) |
1) 2.5 t/h 2) 2.9 t/h |
1) PtF 41.5% 2) PtF 51.3% |
1) 0.26 €/kWh 2) 0.20 €/kWh |
| Sherwin (2021) [23] |
Pathway 1: HT DAC → RWGS → CO-FT Pathway 2: LT DAC → RWGS → CO-FT | 1,203,534 L/d | - |
1) 1.68-1.76 2) 0.95-0.99 ($2050/GLE) |
| Ordóñez et al. (2021) [18] |
Pathway 1: PEM electrolysis → RWGS → CO-FT Pathway 2: SO co-electrolysis → CO-FT CO-FT (Co-based, α = 0.85) |
1) 55.43 t/h 2) 51.16 t/h | - |
1) 0.97 $/GLE 2) 1.01 $/GLE |
공정 시뮬레이션은 크게 공급물질의 준비, 합성석유 생산, 그리고 고도화 및 분리의 3단계로 이루어져 있다. 시뮬레이션 공정 계통도의 예시를 Fig. 12에 도시하였다.
이산화탄소의 포집은 주로 연도가스로부터의 연소후 포집을 적용한 사례가 대부분이었으며, Isaacs 등의 사례[35] 및 Sherwin의 사례[23] 등 최근 수행된 일부 연구에서는 DAC를 통한 탄소 포집을 적용했다. Fig. 5에서 확인할 수 있듯 현존하는 PtX 플랜트에서는 AEC의 채용률이 높은 데에 비해, FT 연료 생산 공정을 시뮬레이션한 사례들에서는 AEC를 적용한 사례가 없었다. SOEC의 경우 AEC 및 PEMEC에 비해 잠재적으로 높은 에너지 효율을 보이며, 또한 공전해 반응을 통해 합성가스를 직접 생산하여 시스템 전반의 효율을 증대시킬 수 있다[18]. 이러한 특성 때문에 FT 연료 생산 공정을 모사한 연구에서 AEC에 비해 잠재적 성능과 효율이 우수한 PEMEC 및 SOEC이 자주 채용된다.
합성가스를 합성석유로 전환하는 FT 과정에서 주로 코발트 기반 촉매를 사용한 저온 과정이 채택되었으며, 이 경우 사슬 성장 확률은 0.85-0.95의 범위 안에 있었다. 코발트 기반 촉매를 적용하였을 경우 사슬형 포화 탄화수소인 알케인계(CnH2n+2)가 생성물의 다수를 차지한다.
FT 경로를 따라 생성된 합성석유는 이후 고도화 및 분리의 과정을 거쳐 FT 연료로 전환되어 최종적으로 산출된다.
공정의 평가 요소로 크게 세 가지 효율 지표가 쓰인다. 투입된 전력 대비 생성된 연료의 열량을 나타내는 PtL 효율(ηPtL), 투입한 수소의 열량 대비 생산된 연료의 열량을 의미하는 CCE 효율(ηCCE)및 이산화탄소의 탄소 몰수 대비 합성연료의 탄소 몰수를 의미하는 탄소 전환 효율(ηCC)을 다수 문헌에서 공통적으로 채용했다.
Becker 등은 고온 SOEC를 이용한 공전해 기술과 FT 공정을 통해 합성연료를 생산하는 시스템을 설계하였다. 그 후 공정의 기술경제성 평가를 통해 합성연료의 가격을 분석하고 기술적·경제적인 지표들에 대한 민감성 분석을 수행했다. 연소후 포집을 통해 얻은 이산화탄소와 물을 SOEC 공전해를 통해 합성가스로 전환하고, 저온 코발트 계열 촉매를 활용한 FT 합성을 통해 80% 파라핀과 20% 올레핀의 합성원유가 생산된다. 합성원유는 이후 추가적인 가공 공정을 거쳐 가솔린과 디젤로 각각 전환된다. 기술경제성 분석 결과 전기의 가격, 공정의 작동률, SOEC의 초기 비용과 FT 공정의 CO 전환율이 연료 가격에 큰 영향을 주는 것으로 나타났다[59].
König 등은 포집 이산화탄소와 수소로부터 연료를 생산하는 공정의 실현 가능성을 검토하기 위한 공정 시뮬레이션을 진행했다. 철강 및 시멘트 공장에서 배출되는 이산화탄소를 포집하는 것으로 가정하였으며, PEM 수전해를 이용하여 수소를 생산한 후, RWGS 반응을 통해 합성가스를 생산하였다. 합성가스는 코발트 기반 촉매를 활용한 저온 FT 반응기에서 합성원유로 전환된다. 생산된 기체상 합성원유는 비등점에 따라 냉각되어 증류되고, 액체상 합성원유는 수소화분해를 거쳐 경질 액체연료로 전환된다. 시간당 5.5톤의 생산량을 갖는 공정을 설계했으며, 이때 PtF 효율은 43.3%로 계산되었다[79].
Cinti 등은 SOEC 공전해 기술 및 FT 합성 공정의 시뮬레이션을 진행하였다. SO 전해조의 성능은 실험 데이터에 기반하여 설계하였고, FT 공정의 경우 문헌을 참고하여 모델링했다. FT 기체 생성물의 재처리 방식에 따라 세 종류의 공정을 설계했으며, 하루에 1 BBL(159 L)를 최대 57.2%의 효율로 생산하는 것으로 계산되었다[97].
Albrecht 등은 대체연료간의 공정한 비교를 위한 방법론을 제시하였다. 일반적인 PtL 경로 외에 바이오매스로부터 얻은 합성가스로 FT 합성을 진행한 BtL 경로와 포집 탄소 및 바이오매스 기반 합성가스를 동시에 활용한 PBtL 경로를 각각 연구하였다. PtL 경로의 경우 PEM을 이용한 수전해와 900°C에서의 RWGS를 통해 합성가스를 생성하였으며, 세 경로 모두 코발트 기반 촉매를 적용한 저온 FT 합성을 모사했다. BtL, PBtL, 그리고 PtL 각각에 대하여 XtL 효율은 36.3%, 51.4%, 50.6%로, 탄소 전환율은 24.9%, 97.7%, 그리고 98%로 계산되었다. PBtL 및 PtL의 경우 수전해로 얻은 산소를 활용한 순산소연소를 공정에 활용하여 탄소 전환율을 높일 수 있었다. 연료의 총 생산 비용(NPC)은 2.24-2.81 €/L로 PBtL이 가장 저렴하였으며 PtL이 가장 비싼 것으로 나타났다[98].
Zhang 등은 PtL/PtG 하이브리드 공정을 시뮬레이션했다. 수소와 이산화탄소를 공급받아 직접 FT 반응기에 투입한 후, 기체상의 부산물과 미반응물 일부를 재활용하는 대신 메테인화 반응(Sabatier 반응)에 사용하여 액상의 FT 합성석유와 합성 천연가스(SNG)를 동시에 생산하는 공정을 구성하였으며, 이때 재활용 비율에 따른 공정 투입 및 산출에 대한 영향성을 비교했다. 합성가스가 아닌 이산화탄소를 FT 반응에 사용했기 때문에, CO2-FT 반응을 위해 설계된 철 기반 촉매를 사용했다. 재활용 비율이 높을수록 합성석유의 생산량은 증가하고 반대로 SNG의 생산량은 감소하는데, 에너지 효율 및 CO2 저감 효과가 낮아지는 것으로 계산되었다. 재활용 비율 100%로 합성석유만 생산 시, 일 평균 450 kL의 생산량을 보였으며 에너지 효율은 49.2%, 생산 비용은 약 1.38 $/L로 계산되었다[42].
Albrecht와 Nguyen은 덴마크의 풍력 에너지에 기반한 e-Fuel 생산 공정의 실현 가능성과 덴마크의 친환경에너지 계획에서 e-Fuel의 기여도를 검토해 보고자 시뮬레이션을 수행했다. 해상풍력발전단지로부터 시간당 600 MW의 전기를 공급받아 PEM 수전해와 RWGS, 그리고 코발트 기반 촉매를 이용한 저온 FT 합성을 거쳐 e-Fuel을 생산하는 공정을 설계했다. 600 MW의 전기 공급량은 현재 덴마크의 해상풍력발전 생산량의 50%에 해당하는 에너지인 반면, 이를 통해 생산된 e-Fuel은 연간 5.12 PJ에 불과했다. 해당 생산량은 덴마크의 2050년 예상 대체연료 수요(연간 75-218 PJ)의 2-7% 선이며, 따라서 저자들은 덴마크가 목표로 하는 대체연료 수요를 만족시키기 위해서 재생에너지의 생산량을 크게 늘려야 한다고 주장했다[30].
Zang 등은 수소와 이산화탄소 가격의 변동에 따른 최소연료판매가격(Minimum Fuel Selling Price, MFSP)의 변화를 분석했다. 공정에 투입된 수소와 이산화탄소는 RWGS 과정에서 합성가스로 전환되고, 이후 코발트 기반 촉매의 저온 FT를 통해 액체 및 기체 생성물이 생산된다. 기체 생성물 중 수소는 PSA(Pressure Swing Adsorption) 과정을 통해 일부 분리되어 반응물로 다시 투입되고, 이외 성분 및 잔여 수소는 전력 생산에 사용된다. 액체 생성물 중 왁스(> C20)는 수소화분해를 거쳐 단쇄 탄화수소로 분해되며, 이후 분별증류를 통해 나프타, 항공유 및 디젤이 최종적으로 생산된다. 에너지 효율에 대한 민감성 분석 결과, 수소의 재사용률, RWGS 과정에서의 CO2 전환율 및 반응 온도, FT 과정에서의 CO 전환율 등이 효율에 큰 영향을 주는 것으로 나타났다. E-Fuel의 MFSP는 1.43-1.56 $/L로 계산되었다[25].
Isaacs 등은 PEM 수전해 및 RWGS 과정을 포함한 PtL, SO 공전해 과정을 포함한 PtL, 바이오매스 가스화로 탄소를 공급하는 BtL, 그리고 그린 수소와 바이오매스 기반 탄소를 활용하는 PBtL의 네 종의 연료 생산 과정을 모사하였고, 이를 바탕으로 환경성 및 경제성 평가를 수행했다. 풍력 에너지로 생산된 전기를 사용할 시, BtL 연료가 가장 저렴하나 이산화탄소 배출량이 가장 높은 것으로 나타났다. 공전해 PtL의 MFSP는 3.06 $/L, 수전해-RWGS PtL은 2.89 $/L로 공전해 기술의 낮은 성숙도에 의해 가격에 차이가 있었다. 이산화탄소 배출량 역시 공전해 PtL이 6 gCO2/MJ로 수전해-RWGS PtL의 2 gCO2/MJ에 비해 높았다. 한편 PBtL 방식의 MFSP는 1.64 $/L로 가장 저렴했다[35].
Herz 등은 PEM 수전해-RWGS 과정을 통한 FT 연료 공정과 SO 공전해를 통한 FT 연료 공정을 비교했다. SOEC 공전해 방식의 높은 작동 온도를 유지하기 위해서는 에너지 투입이 필요하다. 그러나 높은 작동 온도에서 전해조의 과전압(overpotential)에 의한 손실이 감소하기 때문에 시스템의 전반적인 효율이 개선된다는 장점이 있다. 또한, RWGS 과정에 비해 합성가스 내 CO2와 CH4의 생성량이 적다는 장점이 있다. 또한 공정 과정에서 발생하는 폐열을 재생하여 SOEC의 온도를 높이는 데에 사용할 수 있다. 2020년 현재 PEMEC를 통해 생산된 e-Fuel의 총 생산 비용은 0.434 €/kWh로 SOEC의 0.460 €/kWh에 비해 저렴하지만, 2050년에는 이 추이가 역전되어 PEMEC의 경우 0.262 €/kWh로, SOEC의 경우 0.203 €/kWh로 SOEC의 경제성이 우수할 것으로 예측했다[99].
Sherwin은 e-Fuel 생산 과정의 기술경제성 평가를 위한 프레임워크를 제안했다. DAC를 이용해 포집된 이산화탄소와 재생에너지로부터 일간 120만 리터의 제트 연료를 생산하는 공정을 모사했으며, 2020년, 2030년 및 2050년 시점 각각에서 기술경제성 연구를 수행했다. 생산된 연료의 가격은 2020년 기준 4.41-4.46 $/GLE(가솔린 등가 리터)에서 2050년 시점에서는 0.95-0.99 $/GLE로 큰 폭으로 줄어들 것으로 예측했다. 현재의 제트 연료 수요를 100% e-Fuel로 공급하기 위해서는 미국 국토의 잠재적 태양 에너지의 1%에 해당하는 에너지가 필요하며, 이를 생산하기 위한 대지로 30,000-45,000 km2의 사막 면적(미국 국토의 0.3-0.5%)이 요구된다. 한편, 바이오연료는 동일한 에너지를 생산하기 위해서는 410,000 km2의 농경지가 필요하며, 이는 미국 경작지의 26%에 대응하는 면적이다[23].
Ordóñez 등은 연료 생산 과정에 대한 기술경제성 평가 및 환경에 대한 영향의 전과정평가(LCA)를 수행했다. 풍력 에너지 기반의 FT 연료의 총 생산 비용은 PEM 수전해 이용 시 4.68 $/GLE, SO 공전해 이용 시 4.98 $/GLE으로 나타났다. SO 공전해의 경우 인체의 건강 및 생태계에 대한 영향성이 PEM 수전해에 비해 낮은 것으로 나타났는데, 이는 SO 공전해의 높은 효율에 의해 공급물질 소모량 대비 전기/냉각수/냉매의 소모량이 적기 때문이다. 또한 연료 생산량 대비 공해 배출량 역시 SO 공전해의 경우가 낮은 것으로 계산되었다[18].
3.2 E-Fuel 플랜트 소개
현재 포집 이산화탄소와 그린 수소를 기반으로 한 메테인 혹은 메탄올을 생산하는 대단위 플랜트가 현존한다. 반면 FT 연료 플랜트의 경우 현재 계획 발표 혹은 착공 단계에 머물러 있으며, 2020년대 중반부터 본격적인 가동이 예상된다. Table 6에 현재 작동 중이거나 계획이 발표된 e-Fuel 플랜트를 정리하였다.
Table 6.
| Location | Year | Institution or company | Type of fuel | Plant size | Current status |
| Werlte, Germany | 2013 | Audi[100] | Methane | 1,000 t/year | Operating |
| Svartsengi, Iceland | 2015 | Carbon Recycling International[101] | Methanol | 4,000 t/year | Operating |
| Anyang, China | 2022 | Carbon Recycling International[101] | Methanol | 110,000 t/year | Under construction |
| Herøya, Norway | 2024 | Nordic Electrofuel[104] | Jet fuel | 10M L/year | Announced |
| Patagonia, Chile | 2026 | Siemens Energy, Porsche AG[102] | Gasoline | 550M L/year | Under construction |
| Herøya, Norway | 2026 | Norsk e-Fuel[103] | Renewable fuel | 100M L/year | Announced |
독일의 Audi사는 2013년부터 포집 이산화탄소와 6 MW급 알칼리 전해조로 얻어진 수소를 활용하여 e-gas라는 이름의 메테인을 연간 1천 톤씩 생산하고 있다[100].
아이슬란드에 위치한 Carbon Recycling International사는 2012년부터 연소후 포집으로 얻어진 이산화탄소를 이용하여 연간 4천 톤의 메탄올을 생산하는 George Olah 플랜트를 운영하고 있으며, 2022년까지 중국에 11만 톤의 메탄올 플랜트를 건설할 것으로 계획하고 있다[101].
독일의 Siemens Energy사와 Porsche사는 칠레의 Patagonia 지역에 연간 5억 5천만 리터의 e-Gasoline을 생산하는 대규모 플랜트 건설 계획을 발표하고 2021년에 착공하였다. Haru Oni 플랜트라 명명된 프로젝트는 3단계로 구성되어 있으며, 단계별로 2022년까지 연간 13만 리터, 2024년까지 5,500만 리터를 생산할 예정이고, 2026년 목표 생산량을 달성할 것을 계획하고 있다[102].
Sunfire사, Climeworks사, Paul Wurth사 및 Vanilor사의 합작 기업인 Norsk e-Fuel사는 노르웨이의 Herøya 지역의 산업단지에 재생가능 연료(renewable fuel) 플랜트의 건설 계획을 발표했다. 2023년까지 연간 1천만 리터 규모의 실증을 마친 후, 2026년에 연간 1억 리터 규모의 재생가능 연료를 DAC 및 SOEC 공전해 기술을 활용하여 생산할 계획이다[103].
Nordic Electrofuel사 역시 노르웨이 Herøya 지역에 e-Fuel 플랜트를 건설해 2024년까지 연간 1천만 리터의 SAF 제트 연료를 생산할 계획이다. 이후 2032년까지 10 TWh의 전력을 공급받아 연간 10억 리터 규모의 생산 설비를 확충하는 것을 목표로 하고 있다[104].
4. 결 론
본 논문에서는 미래 연료의 후보군 중에서 근래에 들어 관심을 받기 시작한 탄소중립연료를 소개하고, 합성 과정과 연구 사례를 살펴보았다.
기후변화의 억제를 위해 탄소중립의 실현과 에너지 체제의 전환이 요구된다. 그린 수소와 포집 이산화탄소로부터 합성되는 탄소중립연료는 현존 화석연료와 유사한 물성 및 화학 조성을 갖기 때문에 항공 및 해운 분야 등 현재 기술로 전동화가 어려운 부문의 탈탄소화에 기여할 수 있을 것으로 여겨진다.
재생에너지로부터 PtX 과정을 거쳐 탄소중립연료를 합성하여 에너지의 활용성을 증대하는 것으로 섹터커플링을 실현할 수 있다. 이 중에서도 PtF 과정은 연도가스 혹은 대기로부터 이산화탄소를 포집하고 수전해를 통해 수소를 생산한 후, RWGS 및 FT 공정을 통해 화석연료와 유사한 물성의 연료인 FT 연료를 합성하게 된다. FT 연료의 생산 비용은 1-3 $/L 범위로 예상되었으며, 에너지 변환 효율은 41-57%로, 탄소 전환 효율은 74-98%로 각각 계산되었다.
현재는 대규모 수전해를 위한 전해조와 탄소 포집 설비가 충분하지 않으며, 재생가능 전기 에너지의 가격이 매우 높으므로 탄소중립연료의 가격 경쟁력이 화석연료에 비해 떨어진다. 그러나 최근 유럽연합에서 ‘Fit for 55’ 정책 패키지를 통해 탄소배출량에 따라 일종의 관세를 차등적으로 부과하는 탄소국경조정메커니즘(carbon border adjustment mechanism)의 도입을 예고하는 등 온실가스 배출 규제가 강화되면서 화석연료의 입지가 좁아지고 있다. 동시에 재생에너지의 생산량이 많아지고 높은 효율의 e-Fuel 생산 플랜트의 가동이 시작되는 등 규모의 경제가 실현되면 특히 수송 분야에서 탄소중립연료가 현재의 화석연료를 대체할 수 있을 것으로 기대한다.
탈화석연료 이후 탄소중립시대의 에너지 체제는 하나의 솔루션으로 일원화되기보다는 각 국가의 상황과 시기, 그리고 지리적 위치 등에 따라 다양한 체제가 공존하는 방향으로 진보할 것이며, 이에 대응하기 위해 다각적이고 광범위한 에너지 포트폴리오를 마련하고 구체적인 활용성을 검토할 필요가 있다. 대한민국은 지정학적 여건에 의해 국제 무역의 절대다수를 전동화가 어려운 해양 및 항공 운송에 의존하고 있으며, 한반도의 지리적 특성 상 사계절의 변화에 따른 기후의 차이가 뚜렷하여 재생가능 에너지의 연간 변동폭이 큰바, e-Fuel을 포함하는 PtX 및 섹터커플링 기술의 효용이 클 것으로 사료된다.
최근 국내에서 수소 기술을 위시한 무탄소화에 대한 논의가 활발하게 이루어지면서 e-Fuel에 직간접적으로 연관된 기술들이 연구되고 있다. 그린 수소의 생산을 위한 수전해 기술의 경우 2021년 현재 풍력에너지가 풍부한 제주도를 기준으로 메가와트 규모의 수전해 설비의 실증이 다수 예정되는 등 많은 관심을 받고 있다. 이에 반해 e-Fuel 생산 및 온실가스 배출 흡수(negative emission) 기술의 핵심이라 할 수 있는 직접공기포집 기술의 경우 국내에서 검토 및 연구개발을 수행한 사례가 드물며, e-Fuel의 실현 가능성 및 생산 공정에 대한 논의 역시 전무한 실정이다. 최근 국내외 에너지 전환 정책 및 로드맵에서 e-Fuel이 언급되는 빈도가 늘어나는 등 e-Fuel에 대한 국내외에서의 관심이 커지고 있는바, 관련 연구의 필요성을 제안한다.